Carboplatino
| Carboplatino | ||
|---|---|---|
 | ||
 | ||
| Nombre (IUPAC) sistemático | ||
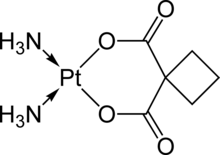
| cis-diamino(ciclobutano-1,1-dicarboxilato-O,O')platino(II) | ||
| Identificadores | ||
| Número CAS | 41575-94-4 | |
| Código ATC | L01XA02 | |
| PubChem | 498142 | |
| DrugBank | APRD00466 | |
| Datos químicos | ||
| Fórmula | C6H12N2O4Pt | |
| Peso mol. | 371.249 g/mol | |
| Farmacocinética | ||
| Biodisponibilidad | completa | |
| Unión proteica | Muy baja | |
| Vida media | 30 horas | |
| Excreción | Hepática | |
| Datos clínicos | ||
| Cat. embarazo | Evidencia de riesgo para el feto, aunque el beneficio potencial de su uso en embarazadas puede ser aceptable a pesar del riesgo probable solo en algunas situaciones. Queda a criterio del médico tratante. (EUA) | |
| Estado legal | Sólo Rx | |
| Vías de adm. | Intravenosa | |
El carboplatino es un medicamento basado en el platino, y usado en quimioterapia para el tratamiento de varios tipos de cáncer (principalmente en tumores de ovarios, pulmones, cuello y cerebro). Fue introducido a finales de la década de los 80, y ha ganado popularidad en el tratamiento clínico debido a los pocos efectos secundarios que posee en comparación con el compuesto paterno cisplatino. Tanto el cisplatino como el carboplatino y el oxaliplatino, interactúan con el ADN, siguiendo un mecanismo similar al de los agentes alquilantes.
Historia[editar]
El carboplatino se descubrió y se desarrolló en el Instituto de investigación contra el cáncer de Londres. En marzo de 1989 Bristol-Myers Squibb obtuvo la aprobación de la Agencia de Alimentos y Medicamentos estadounidense (FDA) para comercializar el carboplatino bajo el nombre Paraplatin. A partir de octubre del 2004 comenzaron a estar disponibles las versiones genéricas del medicamento.
Farmacología[editar]
Química[editar]
El carboplatino difiere del cisplatino en el hecho de poseer un ligando bidentado de dicarboxilato (CBDCA) como grupo exterior en vez de los ligandos cloro. Posee una reactividad menor y una cinética de unión al ADN inferior, aunque forma los mismos productos de reacción in vitro con dosis equivalentes a las del cisplatino. A diferencia del cisplatino, el carboplatino puede ser susceptible de poseer mecanismos alternativos. Algunos resultados muestran que tanto el cisplatino como el carboplatino causan distintos cambios morfológicos en la línea celular MCF-7 cuando ejercen su comportamiento citotóxico. La reactividad inferior limita la creación de complejos proteicos de carboplatino, los cuales deben ser eliminados por el organismo. El carboplatino posee una tasa de excreción menor, por lo que el cuerpo retiene una cantidad mayor y sus efectos son más duraderos (una vida media de retención de 30 horas para el carboplatino, comparada con las 1,5-3,6 horas en el caso del cisplatino).
Forma de acción[editar]
Existen dos teorías que explican los mecanismos de actuación del carboplatino con el ADN:
- Actuación, o hipótesis similar al cisplatino.
- Activación, o hipótesis contraria al cisplatino.
La primera es más aceptada debido a la similitud de los grupos químicos con su sucesor, mientras que la segunda contempla un mecanismo de activación para liberar los grupos Pt2+.
Efectos secundarios[editar]
Comparado con el cisplatino, el mayor beneficio del carboplatino es su menor incidencia de efectos secundarios, en especial en lo referente a los efectos nefrotóxicos. Las náuseas y los vómitos son menos severos y más fácilmente controlables. Por otro lado, el carboplatino ha demostrado su efectividad contra determinados cánceres que no responden ante el cisplatino, como tumores de células germinales, tumores de pulmón de células pequeñas y no pequeñas, de ovario y leucemias.
El principal efecto adverso del carboplatino es su efecto mielosupresor. Esto causa que las células sanguíneas y las plaquetas producidas por la médula ósea decrezcan dramáticamente, en ocasiones a niveles del 10% de los niveles normales. El nadir de la mielosupresión suele acontecer entre los días 21-28 tras el primer tratamiento, momento tras el que las células y plaquetas de la sangre se estabilizan, llegando a alcanzar niveles cercanos a los originales. Esta disminución de leucocitos (neutropenia) puede causar complicaciones, por lo que suele ser tratada con medicinas como el filgrastim. La complicación más notable de la neutropenia es el incremento de la probabilidad de infección de organismos oportunistas, lo que puede llevar a un ingreso hospitalario y a un tratamiento con antibióticos.
Comparada con el cisplatino, la potencia del carboplatino es menor: dependiendo del tipo de cáncer, el carboplatino puede ser entre 1/8 y 1/45 menos efectivo que el cisplatino. Por ello, la dosis clínica estándar de carboplatino es de unas cuatro veces mayor. La estabilidad del carboplatino es un arma de doble filo: tras la administración del medicamento, su vida media es mayor, aunque esta falta de actividad hace que la droga se disperse por todo el cuerpo humano, recuperándose un 90 % del carboplatino en la orina.
Se puede aumentar la efectividad del carboplatino incubándolo en una solución de cloruro sódico (NaCl). Tras 24 horas, se realizó un análisis de la disolución separando los compuestos por un cromatógrafo de capas finas (TLC). El TLC aisló cisplatino, carboplatino, y diversos compuestos de platino en la solución. Se realizaron varias pruebas que mostraron que la tasa de supervivencia de E. coli disminuía dramáticamente cuando la molaridad del NaCl en la solución aumentaba. Las bacterias también mostraron decrementos de fosfatasa alcalina, un indicador proteico ligado al tamaño celular. Este hecho sugiere que cuando esta solución se le administraba a las células, éstas comenzaban a disminuir de tamaño y morir, aparentemente debido al mecanismo del cisplatino.
Quimioterapia GemCarbo para el cáncer de pulmón[editar]
La quimioterapia GemCarbo (consistente en gemcitabina, también conocida como Gemzar, y carboplatino) se usa para tratar distintos tipos de cáncer, aunque suele ser primordial en el tratamiento de cáncer de pulmón.[1] Esta quimioterapia suele administrarse en un tratamiento diario, tras un análisis sanguíneo el día anterior. El régimen GemCarbo se administra en un ciclo de 21 días en el que en el primer día de tratamiento se administra al paciente gemcitabina y carboplatino. En el mismo día de la siguiente semana (día ocho) se le administra una dosis de gemcitabina. Acto seguido se efectúa un período de descanso de dos semanas para completar un ciclo de quimioterapia. El siguiente ciclo de tratamiento se administra tras el período de descanso, tres semanas tras la primera inyección. Un tratamiento completo suele estar compuesto por 4-6 ciclos administrados en el transcurso de 3-4 meses. El tratamiento suele prevenir la diseminación del cáncer y en ocasiones reducir el tamaño del tumor entre el 20-80 % en función del individuo.
Eventos recientes[editar]
Un estudio reciente en ratones con mutaciones sugiere que en el subconjunto de mujeres con cáncer de mama ocasionado por los genes BRCA1 y BRCA2 (causantes de una variedad familiar de cáncer de mama) el carboplatino puede ser 20 veces más efectivo que los tratamientos anticancerígenos estándares.[2] Sin embargo, todavía no se han obtenido datos similares en humanos.
El carboplatino también se ha utilizado para tratar a pacientes con seminomas de fase 1. Las investigaciones recientes ponen de manifiesto que este tratamiento es más efectivo y tiene menos efectos colaterales que la radioterapia adyuvante.[3][4][5] Resulta tan efectivo como la radioterapia para prevenir el desarrollo del seminoma en el testículo restante.[6]
Falsas alarmas[editar]
Desde el año 2015 circula por las redes sociales un bulo[7] de este medicamento, difundida ampliamente en Perú, Colombia, México, Estados Unidos, Argentina, España y Venezuela.
Hola como andas. Me podes difundir este msj? Un bebe de 2 años padece de cancer necesita un medicamento : carboplatino 450 mg … + 584244636611. Mary hernandez xr favor pasen la cadena es urgente… Tomate solo 1 min !!! Es un bebe … Gracias
La campaña suele mantener el nombre de la supuesta madre y en algunos casos, cambiando la ciudad de origen y el número de teléfono, el cual ha sido rastreado, detectándose que pertenece a otro abonado. Mayormente, se trata de una línea telefónica de Venezuela y su titular nada sabe de tal campaña solidaria como tampoco del supuesto niño enfermo. Según las verificaciones realizadas en Internet, esta campaña se trataría de un caso falso que solo pretende conseguir contactos para luego ser utilizados con fines comerciales de promoción de productos o servicios.[8]
Referencias[editar]
- ↑ Macmillan GemCarbo chemotherapy
- ↑ Mark Henderson, "Lung cancer drug may fight breast tumour in women", (May 1, 2006) Times Online http://www.timesonline.co.uk/tol/news/uk/article711744.ece
- ↑ «Copia archivada». Archivado desde el original el 11 de febrero de 2009. Consultado el 19 de marzo de 2010.
- ↑ http://news.bbc.co.uk/2/hi/health/4700755.stm
- ↑ http://www.timesonline.co.uk/tol/life_and_style/health/article4887854.ece
- ↑ http://www.medscape.com/viewarticle/575825
- ↑ VK2. «Se necesita carboplatino 450 para un bebé inexistente». Consultado el 10 de octubre de 2019.
- ↑ Flores, Angel (22 de septiembre de 2018). «El falso mensaje viral de un pedido de ayuda para un niño con cáncer que circula en La Rioja». El Federal OnLine. Archivado desde el original el 10 de octubre de 2019. Consultado el 10 de octubre de 2019.
Referencias adicionales[editar]
- Natarajan, G., et al. Increased DNA-binding activity of carboplatin in the presence of nucleophiles and human breast cancer MCF-7 cell cytoplasmic extracts: activation theory revisited. Biochem. Pharmacol. 58, 1625-1629 (1999). PMID 10535754.
- Knox, RJ et al. Mechanism of cytotoxicity of anticancer platinum drugs: evidence that cis-diamminedichloroplatinum(II) and cis-diammine-(1,1-cyclobutanedicarboxylato)platinum(II) differ only in the kinetics of their interaction with DNA. Cancer Res. 1986 Apr;46 (4 Pt 2):1972-9. PMID 3512077
- Canetta R, Rozencweig M, Carter SK. Carboplatin: the clinical spectrum to date. Cancer Cancer Treat Rev. 1985 Sep;12 Suppl A:125-36. PMID 3002623
- Overbeck, T, et al. A comparison of the genotoxic effects of carboplatin and cisplatin in Escherichia Coli. Mutation Research/DNA Repair. Volume: 362, Issue: 3, April 2, 1996, pp. 249-259.
- Schnurr, B., Gust, Ronald. Investigations on the decomposition of carboplatin in infusion solutions. Mikrochimica Acta. Volume: 140, Issue: 1-2, August, 2002, pp. 69-76.
- Xiang, Wang. Structural studies of atom-specific actions on DNA. Pharmacology & Therapeutics. Volume: 83, Issue: 3, September, 1999, pp. 181-215.
- Lois B. Travis, M.D., Sc.D., Eric J. Holowaty, M.D., Kjell Bergfeldt, M.D., Charles F. Lynch, M.D., Ph.D., Betsy A. Kohler, M.P.H., Tom Wiklund, M.D., Ph.D., Rochelle E. Curtis, M.A., Per Hall, M.D., Ph.D., Michael Andersson, M.D., Ph.D., Eero Pukkala, Ph.D., Jeremy Sturgeon, M.D., Marilyn Stovall, Ph.D., Hans Storm, M.D., E. Aileen Clarke, M.D., John D. Boice, Sc.D., and Mary Gospodarowicz, M.D. Risk of Leukemia after Platinum-Based Chemotherapy for Ovarian Cancer. (http://content.nejm.org/cgi/content/full/340/5/351)
