Diferencia entre revisiones de «Datación radiométrica»
m Revertidos los cambios de 85.50.150.136 (disc.) a la última edición de Miaow Etiqueta: Reversión |
Amplio traduciendo el artículo completo de la wiki inglesa |
||
| Línea 1: | Línea 1: | ||
La '''datación radiométrica''', '''datación radioactiva''' o '''datación por radioisótopos''' es una técnica utilizada para [[datación cronológica|datar]] materiales como [[rocas]], [[mineral]]es y restos orgánicos ([[carbono]]), en los que se incorporaron de manera selectiva [[impureza]]s radiactivas cuando se formaron. El método se basa en la comparación de la abundancia de un [[isótopo radiactivo|radionucleido]] de ocurrencia natural dentro del material con la abundancia de sus [[decaimiento radioactivo|productos de descomposición]], que se forman a una[[periodo de semidesintegración|tasa constante de desintegración conocida]].<ref>{{GoldBookRef|title=radioactive dating|file=R05082}}</ref> El uso de la datación radiométrica fue publicado por primera vez en 1907 por [[Bertram Boltwood]]<ref>{{ cite journal | author = Boltwood, Bertram | year = 1907 | title = The Ultimate Disintegration Products of the Radio-active Elements. Part II. The disintegration products of uranium | journal = American Journal of Science | series = 4 | volume = 23 | issue = 134 | pages = 77–88 | doi=10.2475/ajs.s4-23.134.78}}</ref> —avanzado por [[Ernest Rutherford]] en 1905— y ahora es la principal fuente de información sobre la [[datación absoluta|edad absoluta]] de las rocas y otras [[geología|características geológicas]], incluida la edad de las [[paleontología|formas de vida fosilizadas]] o la propia [[edad de la Tierra]], y también se puede utilizar para datar una amplia gama de materiales naturales y [[artefacto (arqueología)|artefacto]]s.<ref>[http://pubs.usgs.gov/gip/geotime/radiometric.html] Geologic Time: Radiometric Time Scale". United States Geological Survey.</ref> |
|||
La '''datación radiométrica''' es un procedimiento técnico empleado para determinar la edad absoluta de [[roca]]s, [[mineral]]es y restos orgánicos ([[Paleontología|paleontológicos]]).<ref>{{Cita libro|apellidos=M|nombre=CAMPOS , JUAN|título=EL PATRIMONIO HISTÓRICO Y CULTURAL EN EL PARAJE NATURAL MARISMAS DEL ODIEL: UN ENFOQUE DIACRÓNICO Y TRANSDISCIPLINAR|url=https://books.google.es/books?id=hxAQDgAAQBAJ&pg=PT98&dq=dataci%C3%B3n+radiom%C3%A9trica++procedimiento++determinar+edad+absoluta&hl=es&sa=X&ved=0ahUKEwia3LCO-LHZAhVHbhQKHZnDAckQ6AEIJzAA#v=onepage&q=dataci%C3%B3n%20radiom%C3%A9trica%20%20procedimiento%20%20determinar%20edad%20absoluta&f=false|fechaacceso=19 de febrero de 2018|fecha=6 de febrero de 2017|editorial=Servicio de Publicaciones de la Universidad de Huelva|isbn=9788416872015|idioma=es}}</ref> El método se basa en las proporciones de un [[isótopo]] «[[padre]]» y de uno o más descendientes de los que se conoce su [[semivida]] o [[periodo de semidesintegración]], contenidos en la muestra que se va a estudiar.<ref>{{Cita libro|apellidos=coordinador|nombre=JOSÉ CARRIÓN|título=CINCO MILLONES DE AÑOS DE CAMBIO FLORÍSTICO Y VEGETAL en la Península Ibérica e Islas Baleares|url=https://books.google.es/books?id=JEh1CQAAQBAJ&pg=PA519&dq=dataci%C3%B3n+radiom%C3%A9trica+basa+en+las+proporciones+de+un+is%C3%B3topo+%C2%ABpadre&hl=es&sa=X&ved=0ahUKEwjq9baz-LHZAhWCVxQKHUcDDsoQ6AEIJzAA#v=onepage&q=dataci%C3%B3n%20radiom%C3%A9trica%20basa%20en%20las%20proporciones%20de%20un%20is%C3%B3topo%20%C2%ABpadre&f=false|fechaacceso=19 de febrero de 2018|fecha=25 de mayo de 2015|editorial=JOSÉ CARRIÓN|isbn=9788461736911|idioma=es}}</ref> Los isótopos propicios para analizar dependen del tipo de muestra y de la presunta antigüedad de lo restos que se quieran datar. Ejemplos de estas técnicas son:<ref>[https://web.archive.org/web/20120412174150/http://web.usal.es/~guillermo/publications/Popularscience/MundoCientificoMayo1994RelojesNucleares.pdf Los isótopos radiactivos y nuestro pasado]</ref> [[Potasio|K]]/[[Argón|Ar]], [[Uranio|U]]/[[Plomo|Pb]], [[Rubidio|Rb]]/[[Estroncio|Sr]], [[Samario|Sm]]/[[Neodimio|Nd]], etcétera. |
|||
Junto con los [[Estratigrafía|principios estratigráficos]], los métodos de datación radiométrica se utilizan en [[geocronología]] para establecer la [[escala de tiempo geológica]].<ref>McRae, A. 1998. ''Radiometric Dating and the Geological Time Scale: Circular Reasoning or Reliable Tools?'' [http://www.talkorigins.org/faqs/dating.html Radiometric Dating and the Geological Time Scale [[TalkOrigins Archive]]]</ref> Entre las técnicas más conocidas están la [[datación potasio-argón]], la [[datación uranio-plomo]] y la [[datación por radiocarbono]] (basada en la desintegración del [[isótopo]] [[carbono 14]]), comúnmente utilizada para la datación de restos orgánicos relativamente recientes, de hasta {{unidad|60000|años}}.<ref>{{Cita libro|apellidos=EQUIPO|título=Diccionario de ciencias de la tierra|url=https://books.google.es/books?id=1XKXQqUGDnoC&pg=PA212&dq=dataci%C3%B3n+radiom%C3%A9trica++dataci%C3%B3n+por+carbono+radiactivo&hl=es&sa=X&ved=0ahUKEwj7xt7e-LHZAhUE7RQKHSCWDAcQ6AEIJzAA#v=onepage&q=dataci%C3%B3n%20radiom%C3%A9trica%20%20dataci%C3%B3n%20por%20carbono%20radiactivo&f=false|fechaacceso=19 de febrero de 2018|fecha=2000|editorial=Editorial Complutense|isbn=9788489784772|idioma=es}}</ref> (Otros dataciones posibles son [[Potasio|K]]/[[Argón|Ar]], [[Uranio|U]]/[[Plomo|Pb]], [[Rubidio|Rb]]/[[Estroncio|Sr]], [[Samario|Sm]]/[[Neodimio|Nd]], etc.<ref>[https://web.archive.org/web/20120412174150/http://web.usal.es/~guillermo/publications/Popularscience/MundoCientificoMayo1994RelojesNucleares.pdf Los isótopos radiactivos y nuestro pasado]</ref>) |
|||
Al permitir el establecimiento de escalas de tiempo geológicas, proporciona una importante fuente de información sobre las edades de los [[fósil]]es y las tasas deducidas de cambio evolutivo. La datación radiométrica también se utiliza para datar materiales [[arqueología|arqueológicos]], incluidos artefactos antiguos. |
|||
La datación radiométrica se viene realizando desde 1905, cuando este método fue desarrollado por [[Ernest Rutherford]] como un método por el cual determinar la edad de la Tierra. Desde entonces las técnicas han sido enormemente mejoradas y ampliadas.<ref>[http://pubs.usgs.gov/gip/geotime/radiometric.html] Geologic Time: Radiometric Time Scale". United States Geological Survey.</ref> |
|||
Los diferentes métodos de datación radiométrica varían según sea la escala de tiempo en la que son precisos y de los materiales a los que se pueden aplicar. |
|||
==Fundamentos== |
|||
== Ecuación de datación == |
|||
=== Desintegración radioactiva === |
|||
En el caso más simple, en el que un isótopo ''padre'' se desintegra en un isótopo ''hijo'' estable, se aplica una expresión matemática que relaciona los períodos de semidesintegración y el tiempo geológico tal que:<ref>{{Cita libro|apellidos=Fernandez|nombre=Maria Beatriz Carenas|título=Geología|url=https://books.google.es/books?id=g3a6AwAAQBAJ&pg=PA364&dq=Ecuaci%C3%B3n+de+dataci%C3%B3n&hl=es&sa=X&ved=0ahUKEwiB9PWg-bHZAhWHwxQKHcyEAJIQ6AEISDAG#v=onepage&q=Ecuaci%C3%B3n%20de%20dataci%C3%B3n&f=false|fechaacceso=19 de febrero de 2018|fecha=2014|editorial=Ediciones Paraninfo, S.A.|isbn=9788497328944|idioma=es|apellidos2=Robles|nombre2=Jorge Luis Giner|apellidos3=Yelamos|nombre3=Javier Gonzalez|apellidos4=Rodríguez|nombre4=Manuel Pozo}}</ref> |
|||
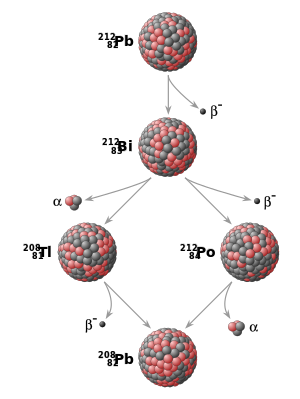
[[Image:Thorium decay chain from lead-212 to lead-208.svg|thumb|right|upright=1.35| Ejemplo de una [[cadena de desintegración]] radiactiva de plomo 212 (<sup>212</sup>Pb) a plomo 208 (<sup>208</sup>Pb). Cada nucleido padre se desintegra espontáneamente en un nucleido hijo (el [[producto de desintegración]]) a través de una [[desintegración alfa|desintegración α]] o de una [[desintegración beta|desintegración β]]. El producto final de desintegración, plomo 208 (<sup>208</sup>Pb), es estable y ya no puede sufrir desintegración radiactiva espontánea.]] |
|||
<center><math> t = \frac{1}{\lambda} {\ln \left(1+\frac{D}{P}\right)}</math></center> |
|||
Toda la [[materia]] ordinaria se compone de combinaciones de [[elementos químicos]], cada uno con su propio [[número atómico]], que indica el número de [[protones]] en el [[núcleo atómico]]. Además, los elementos pueden existir en diferentes [[isótopo]]s, con cada isótopo de un elemento difiriendo en el número de [[neutrones]] en el núcleo. Un isótopo particular de un elemento particular se llama [[nucleido]]. Algunos nucleidos son inherentemente inestables. Es decir, en algún momento en el tiempo, un átomo de tal nucleido sufrirá un [[decaimiento radioactivo]] y se transformará espontáneamente en un nucleido diferente. Esta transformación se puede lograr de varias maneras diferentes, incluida la [[desintegración alfa]] (emisión de [[partículas alfa]]) y la [[desintegración beta]] (emisión de [[electrones]], emisión de [[positrones]] o [[captura de electrones]]). Otra posibilidad es la [[fisión espontánea]] en dos o más nucleidos. |
|||
:<math> t = </math> edad de la muestra. |
|||
:<math> \lambda = </math> [[Periodo de semidesintegración|constante de desintegración radiactiva]] del isótopo ''padre''. |
|||
:<math> \ln = </math> [[logaritmo neperiano]] o [[Logaritmo natural|natural]]. |
|||
:<math> D = </math> número de [[Átomo|átomos]] del isótopo ''hijo'' existentes en la muestra (= n.º de átomos ''padre'' que han decaído radioactivamente). |
|||
:<math> P = </math> cantidad de isótopos ''padre'' presentes en la muestra. |
|||
Si bien el momento en el que un núcleo particular se desintegra es impredecible, una colección de átomos de un nucleido radiactivo [[decaimiento exponencial|decae exponencialmente]] a una tasa descrita por un parámetro conocido como [[vida media]], generalmente dada en unidades de años cuando se estudian las técnicas de datación. Después de que haya transcurrido una vida media, la mitad de los átomos del nucleido en cuestión se habrán desintegrado en un nucleido «hijo» o [[producto de desintegración]]. En muchos casos, el nucleido «hijo» en sí mismo es radioactivo, lo que resulta en una nueva [[cadena de desintegración]], que finalmente termina con la formación de un nucleido «hijo» estable (no radioactivo); cada paso en tal cadena se caracteriza por una vida media distinta. En estos casos, generalmente la vida media de interés en la datación radiométrica es la más larga de la cadena, que es el factor limitante de la velocidad en la transformación final del nucleido radioactivo en su «hijo» estable. Los sistemas isotópicos que han sido explotados para la datación radiométrica tienen vidas medias que van desde solo unos 10 años (por ejemplo, [[tritio]]) hasta los más de 100 mil millones de años (por ejemplo, el [[Anexo:Isótopos de samario|samario 147]]).<ref name="Bernard-Griffiths1989">{{cite book|last1=Bernard-Griffiths|first1=J.|last2=Groan|first2=G.|editor1-last=Roth|editor1-first=Etienne|editor2-last=Poty|editor2-first=Bernard|title=Nuclear Methods of Dating|date=1989|publisher=Springer Netherlands|isbn=978-0-7923-0188-2|pages=53 – 72|chapter=The samarium–neodymium method}}</ref> |
|||
Esta ecuación es válida siempre que el modo de decaimiento del isótopo ''padre'' sea único y que el isótopo ''hijo'' sea estable. Para otros casos se pueden obtener ecuaciones más complejas, en las cuales se tienen en cuenta múltiples decaimientos posibles. |
|||
Para la mayoría de los nucleidos radiactivos, la vida media depende únicamente de las propiedades nucleares y es esencialmente una constante. No se ve afectado por factores externos como la [[temperatura]], la [[presión]], el entorno químico o la presencia de un [[campo magnético]] o [[campo eléctrico|eléctrico]].<ref>{{Cite journal |doi = 10.1146/annurev.ns.22.120172.001121 |title=Perturbation of Nuclear Decay Rates |year=1972 |author=Emery, G T |journal=Annual Review of Nuclear Science |volume=22|issue=1 |pages=165–202|bibcode = 1972ARNPS..22..165E }}</ref><ref>{{Cite journal|doi=10.1038/264340a0 |title=Direct test of the constancy of fundamental nuclear constants |year=1976 |author=Shlyakhter, A. I. |journal=Nature |volume=264|issue=5584 |pages=340 |bibcode=1976Natur.264..340S}}</ref><ref>Johnson, B. 1993. ''How to Change Nuclear Decay Rates'' [http://math.ucr.edu/home/baez/physics/ParticleAndNuclear/decay_rates.html Usenet Physics FAQ]</ref> Las únicas excepciones son los nucleidos que se descomponen por el proceso de captura de electrones, como el [[Anexo:Isótopos de berilio|berilio 7]], el [[Anexo:Isótopos de estroncio|estroncio 85]] y el [[Anexo:Isótopos de circonio|circonio 89]], cuya tasa de decaimiento puede verse afectada por la densidad electrónica local. Para todos los demás nucleidos, la proporción del nucleido original en relación a sus productos de desintegración cambia de manera predecible a medida que el nucleido original decae con el tiempo. Esta previsibilidad permite que las abundancias relativas de los nucleidos relacionados se utilicen como un reloj para medir el tiempo desde la incorporación de los nucleidos originales en un material hasta el presente. |
|||
== Vida media y constante de semidesintegración == |
|||
===Precisión de la datación radiométrica=== |
|||
Se denomina [[vida media]] de un [[radioisótopo]] a la duración promedio de un isótopo radiactivo previa a su desintegración. Es igual a la inversa de la constante de desintegración radiactiva: <math>\tau = 1/\lambda \,\!</math>. |
|||
[[Image:Thermal ionization mass spectrometer.jpg|thumb|[[Espectrómetro de masas de ionización térmica]] utilizado en la datación radiométrica]] |
|||
La ecuación básica de la datación radiométrica requiere que ni el nucleido «padre» ni el producto «hijo» puedan entrar o salir del material después de su formación. Los posibles efectos de confusión de la contaminación de los isótopos «padre» e «hijo» deben considerarse, al igual que los efectos de cualquier pérdida o ganancia de dichos isótopos desde que se creó la muestra. Por lo tanto, es esencial contar con la mayor cantidad de información posible sobre el material que se está datando y verificar posibles signos de [[Metasomatismo|alteración]].<ref>{{Cite journal|doi=10.1016/0012-821X(96)00132-X |title=3-D, <sup>40</sup>Ar---<sup>39</sup>Ar geochronology in the Paraná continental flood basalt province |year=1996 |author=Stewart, K,, Turner, S, Kelley, S, Hawkesworh, C Kristein, L and Manotvani, M |journal=Earth and Planetary Science Letters |volume=143|issue=1–4 |pages=95–109 |bibcode=1996E&PSL.143...95S}}</ref> La precisión se mejora si las mediciones se toman en múltiples muestras de diferentes ubicaciones del cuerpo de roca. Alternativamente, si se pueden datar varios minerales diferentes de la misma muestra y se supone que fueron formados por el mismo evento y que estaban en equilibrio con el yacimiento cuando se formaron, deberían formar una isocrona. Esto puede reducir el problema de la [[contaminación]]. En la [[datación uranio-plomo]], se utiliza el [[diagrama de concordia]] que también disminuye el problema de la pérdida de nucleidos. Finalmente, la correlación entre los diferentes métodos de datación isotópica puede ser necesaria para confirmar la edad de una muestra. Por ejemplo, se determinó que la edad de los [[gneis]]es de Amitsoq, en el oeste de Groenlandia, era de {{Ma|3.60|millones de años (Ma)|error=0.05|round=2}} utilizando la datación plomo-uranio y de {{Ma|3.56|Ma|error=0.10|round=2}} utilizando la datación de plomo-plomo, resultados que coinciden entre sí.<ref>{{cite book|last1=Dalrymple|first1=G. Brent|title=The age of the earth|date=1994|publisher=Stanford Univ. Press|location=Stanford, Calif.|isbn=9780804723312}}</ref>{{rp|142–143}} |
|||
Al tiempo que transcurre hasta que la cantidad de [[Nucleido|núcleos]] radiactivos de un isótopo radiactivo se reduce a la mitad de la cantidad inicial se le denomina [[periodo de semidesintegración]], periodo, semiperiodo o semivida (no confundir con [[vida media]]): <math>T_{1/2} = ln(2)/\lambda \,\!</math>. |
|||
Una datación radiométrica precisa generalmente requiere que el «padre» tenga una vida media lo suficientemente larga como para que esté presente en cantidades significativas en el momento de la medición (excepto, como se describe a continuación, en la «Datación con radionucleidos extintos de vida corta»), que la vida media del «padre» se conozca con precisión y que se produzca suficiente cantidad del producto «hijo» para medirlo y distinguirlo de la cantidad inicial del «hijo» presente en el material. Los procedimientos utilizados para aislar y analizar los nucleidos «padre» e «hijo» deben ser precisos y seguros. Esto normalmente implica el uso de [[espectrometría de masas de relación isotópica]].<ref>{{cite book|last1=Dickin|first1=Alan P.|title=Radiogenic isotope geology|date=2008|publisher=Cambridge Univ. Press|location=Cambridge|isbn=9780521530170|pages=15–49|edition=2nd}}</ref> |
|||
Al fin de cada período de semidesintegración la radiactividad se reduce a la mitad (de la inicial). A cada radioisótopo corresponde un período de semidesintegración característico, en general diferente de los respectivos de otros isótopos. |
|||
La precisión de un método de datación depende en parte de la vida media del isótopo radioactivo involucrado. Por ejemplo, el carbono 14 tiene una vida media de {{unidad|5730|años}}. Después de que un organismo haya estado muerto desde hace {{unidad|60000|años}}, queda tan poco carbono 14 que no se puede establecer una datación precisa. Por otro lado, la concentración de carbono-14 cae tan abruptamente que la edad de los restos relativamente jóvenes se puede determinar con una precisión de unas pocas décadas.<ref>{{Cite journal |
|||
Ejemplos: |
|||
|vauthors=Reimer Paula J, etal |year=2004 |title=INTCAL04 Terrestrial Radiocarbon Age Calibration, 0–26 Cal Kyr BP |journal=Radiocarbon |volume=46 |issue=3 |pages=1029–1058 |url=https://journals.uair.arizona.edu/index.php/radiocarbon/article/view/4167/3592}}</ref> |
|||
{| class="wikitable" cellpadding="2" cellspacing="" style="border-collapse: collapse" bordercolor="#111111" |
|||
===Temperatura de cierre=== |
|||
{{AP|Temperatura de cierre}} |
|||
Si un material que rechaza selectivamente el nucleido hijo se calienta, cualquier nucleido hijo que se haya acumulado a lo largo del tiempo se perderá por difusión, lo que pondrá a cero el ''reloj'' isotópico. La temperatura a la que sucede esto se conoce como [[temperatura de cierre]] o temperatura de bloqueo y es específica de cada material en particular y sistema isotópico. Estas temperaturas se determinan experimentalmente en el laboratorio mediante el [[Petrología#Ramas|restablecimiento artificial de los minerales]] de muestra utilizando un horno de alta temperatura. A medida que el mineral se enfría, comienza a formarse la estructura cristalina y la difusión de los isótopos es menos fácil. A cierta temperatura, la estructura cristalina se ha formado lo suficiente como para evitar la difusión de isótopos. Esa temperatura es lo que se conoce como temperatura de cierre y representa la temperatura por debajo de la cual el mineral es un sistema cerrado para los isótopos. Por lo tanto, una roca o masa fundida ígnea o metamórfica, que se está enfriando lentamente, no comienza a mostrar una disminución radiactiva mensurable hasta que se enfríe por debajo de la temperatura de cierre. La edad que se puede calcular por datación radiométrica es, por lo tanto, el momento en que la roca o el mineral se enfriaron hasta la temperatura de cierre.<ref name=Faure>{{Cite book|first=Gunter |last=Faure |title=Principles and applications of geochemistry: a comprehensive textbook for geology students |publisher=[[Prentice Hall]] |location=[[Englewood Cliffs, New Jersey]] |year=1998 |pages= |edition=2nd |isbn=978-0-02-336450-1 |oclc=37783103}}{{Page needed|date=September 2010}}</ref><ref name=Rollinson>{{Cite book|first=Hugh R. |last=Rollinson |title=Using geochemical data: evaluation, presentation, interpretation |publisher=[[Longman]] |location=[[Harlow]] |year=1993 |pages= |isbn=978-0-582-06701-1 |oclc=27937350}}{{Page needed|date=September 2010}}</ref> La datación de diferentes minerales y/o sistemas de isótopos (con diferentes temperaturas de cierre) dentro de la misma roca puede, por lo tanto, permitir el seguimiento de la historia térmica de la roca en cuestión en el tiempo, y por lo tanto la historia de los eventos metamórficos puede ser conocida en detalle. Este campo se conoce como [[termocronología]] o termocronometría. |
|||
=== Ecuación de datación === |
|||
[[Image:Sm Nd Great Dyke Isochron.png|thumb|right|upright=1.5|Trazado de la isocrona [[datación samario-neodimio|Sm/Nd]] de muestras<ref name=Oberthuer>{{Cite journal|doi=10.1016/S0301-9268(01)00215-7 |title=Precise U–Pb mineral ages, Rb–Sr and Sm–Nd systematics for the Great Dyke, Zimbabwe—constraints on late Archean events in the Zimbabwe craton and Limpopo belt |year=2002 |author=Oberthür, T, Davis, DW, Blenkinsop, TG, Hoehndorf, A |journal=Precambrian Research |volume=113|issue=3–4 |pages=293–306|bibcode=2002PreR..113..293O }}</ref> del [[Great Dyke]], [[Zimbabwe]]. La edad se calcula a partir de la pendiente de la isocrona (línea) y la composición original de la intersección de la isocrona con el eje Y. ]] |
|||
La expresión matemática que relaciona la desintegración radioactiva con el tiempo geológico es:<ref name=Faure/><ref name="Cornell">{{Cite web|first=W. M. |last=White |year=2003 |title=Basics of Radioactive Isotope Geochemistry |publisher=[[Cornell University]] |url=http://www.geo.cornell.edu/geology/classes/Geo656/656notes03/656%2003Lecture04.pdf}}</ref> |
|||
{{ecuación|<math> D = D_0 + N(t)(e^{\lambda t} -1)</math>}} |
|||
o |
|||
{{ecuación|<math> t = \frac{1}{\lambda} {\ln \left(1+\frac{D}{D_0}\right)}</math>}} |
|||
siendo: |
|||
:<math> t = </math>, la edad de la muestra, |
|||
:<math> D = </math>, el número de átomos del isótopo «hijo» en la muestra, |
|||
:<math> D_0 = </math>, el número de átomos del isótopo «hijo» en la composición original (igual al n.º de átomos «padre» que han decaído radioactivamente), |
|||
: <math>N(t)</math>, el número de átomos del isótopo «padre» en la muestra en el momento t (el presente), dado por ''N''(''t'') = ''N<sub>o</sub>e''<sup>-''λt''</sup>, y |
|||
:<math> \lambda = </math>, la [[Periodo de semidesintegración|constante de desintegración radiactiva]] del isótopo «padre», igual a la inversa de la [[vida media]] —duración promedio de un isótopo radiactivo previa a su desintegración— del isótopo «padre»<ref name=usgs>{{Cite web|url=http://pubs.usgs.gov/gip/geotime/radiometric.html |title=Geologic Time: Radiometric Time Scale |publisher=[[United States Geological Survey]] |date=16 June 2001}}</ref> multiplicado por el [[logaritmo neperiano| logaritmo neperiano o natural]] (<math> \ln </math>) de 2. La vida media es igual a la inversa de la constante de desintegración radiactiva: <math>\tau = 1/\lambda \,\!</math>. Al tiempo que transcurre hasta que la cantidad de [[nucleido]]s se reduce a la mitad de la cantidad inicial se le denomina [[periodo de semidesintegración]], periodo, semiperiodo o semivida (no confundir con la vida media): <math>T_{1/2} = ln(2)/\lambda \,\!</math>. Al final de cada período de semidesintegración la radiactividad se reduce a la mitad (de la inicial). A cada radioisótopo le corresponde un período de semidesintegración característico, en general diferente de los respectivos de otros isótopos. |
|||
<div align=center> |
|||
{| class="toc" cellpadding=0 cellspacing=2 width=280px style="float:right; margin: 0.5em 0.5em 0.5em 1em; padding: 0.5e text-align:left;clear:all; margin-left:10px; font-size:90%" |
|||
| colspan=4 style="background:#f8f8f8; color:black;" align=center bgcolor#f8f8f8 |'''Principales dataciones''' |
|||
|- |
|||
! Isótopo !! Período !! Emisión |
! Isótopo !! Período !! Emisión |
||
|-bgcolor="#efefef" |
|||
|-align=center |
|||
| Radón 222 || {{unidad|3.82|días}} || Alfa |
|||
| Uranio-238 || 4 510 millones de años<ref>{{Cita libro|apellidos=Salazar|nombre=Salvador Mosqueira Pérez|título=Introducción a la Química y el ambiente|url=https://books.google.es/books?id=tJuEBgAAQBAJ&pg=PT88&dq=Uranio-238+per%C3%ADodo+de+semidesintegraci%C3%B3n+caracter%C3%ADstico,&hl=es&sa=X&ved=0ahUKEwiiiMrr-bHZAhVLbxQKHRAWCO0Q6AEIJzAA#v=onepage&q=Uranio-238%20per%C3%ADodo%20de%20semidesintegraci%C3%B3n%20caracter%C3%ADstico,&f=false|fechaacceso=19 de febrero de 2018|fecha=2000|editorial=Grupo Editorial Patria|isbn=9786077440659|idioma=es}}</ref> || Alfa |
|||
|-align=center |
|||
|- |
|||
| Carbono-14 || 5 730 años || Beta |
|||
| Cobalto 60 || {{unidad|5271|años}} || Gamma |
|||
|-align=center |
|||
| Cobalto-60 || 5,271 años || Gamma |
|||
|-bgcolor="#efefef" |
|||
|-align=center |
|||
| |
| Carbono 14 || {{unidad|5730|años}} || Beta |
||
|- |
|||
| Uranio 238 || {{ma|4510|millones de años}}<ref>{{Cita libro|apellidos=Salazar|nombre=Salvador Mosqueira Pérez|título=Introducción a la Química y el ambiente|url=https://books.google.es/books?id=tJuEBgAAQBAJ&pg=PT88&dq=Uranio-238+per%C3%ADodo+de+semidesintegraci%C3%B3n+caracter%C3%ADstico,&hl=es&sa=X&ved=0ahUKEwiiiMrr-bHZAhVLbxQKHRAWCO0Q6AEIJzAA#v=onepage&q=Uranio-238%20per%C3%ADodo%20de%20semidesintegraci%C3%B3n%20caracter%C3%ADstico,&f=false|fechaacceso=19 de febrero de 2018|fecha=2000|editorial=Grupo Editorial Patria|isbn=9786077440659|idioma=es}}</ref> || Alfa |
|||
|} |
|} |
||
</div> |
|||
La ecuación se expresa mejor en términos de la cantidad medida <math>N(t)</math> en lugar del valor inicial constante <math> N_0</math>. |
|||
La ecuación anterior hace uso de la información sobre la composición de los isótopos «padre» e «hijo» en el momento en que el material que se está probando se enfrió por debajo de su temperatura de cierre. Esto está bien establecido para la mayoría de los sistemas isotópicos.<ref name=Rollinson/><ref>{{Cite journal|doi=10.1016/0012-821X(75)90088-6 |title=Approximation of terrestrial lead isotope evolution by a two-stage model |date=June 1975 |first=J. S. |last=Stacey |author2=J. D. Kramers |journal=Earth and Planetary Science Letters |volume=26 |issue=2 |pages=207–221 |bibcode=1975E&PSL..26..207S}}</ref> Sin embargo, la construcción de una isocrona no requiere información sobre las composiciones originales, utilizando simplemente las relaciones actuales de los isótopos «padre» e «hijo» de un isótopo estándar. El trazado de una isocrona se utiliza para resolver gráficamente la ecuación de edad y calcular la edad de la muestra y la composición original. |
|||
Esta ecuación es válida siempre que el modo de decaimiento del isótopo «padre» sea único y que el isótopo «hijo» sea estable. Para otros casos se pueden obtener ecuaciones más complejas, en las que se tienen en cuenta múltiples decaimientos posibles. |
|||
==Métodos modernos de datación== |
|||
La datación radiométrica se conoce desde 1905, cuando fue ideada por [[Ernest Rutherford]] como un método por el cual se podría determinar la [[edad de la Tierra]]. En el siglo transcurrido desde entonces, las técnicas se han mejorado y ampliado enormemente.<ref name=usgs/> La datación se puede realizar ahora en muestras muy pequeñas, del orden de un nanogramo, usando un [[espectrómetro de masas]]. El espectrómetro de masas se inventó en la década de 1940 y comenzó a usarse en la datación radiométrica en la década de 1950. Opera generando un haz de átomos ionizados a partir de la muestra a prueba. Luego, los iones viajan a través de un campo magnético, que los desvía hacia diferentes sensores de muestreo, conocidos como «[[copas de Faraday]]», según sean su masa y nivel de ionización. Al impactar en las copas, los iones establecen una corriente muy débil que puede medirse para determinar la tasa de impactos y las concentraciones relativas de los diferentes átomos en los haces. |
|||
===Método de datación uranio-plomo=== |
|||
{{AP|Datación uranio-plomo}} |
|||
[[Image:Pfunze belt concordia.png|thumb|upright=1.8|Un diagrama de concordia como el utilizado en la [[datación uranio-plomo]], con datos de [[Pfunze Belt]], [[Zimbabwe]].<ref>{{Cite journal|doi=10.1016/S0899-5362(01)90021-1 |title=U-Pb zircon ages from a craton-margin archaean orogenic belt in northern Zimbabwe |year=2001 |first=M. L. |last=Vinyu |author2=R. E. Hanson |author3=M. W. Martin |author4=S. A. Bowring |author5=H. A. Jelsma |author6=P. H. G. M. Dirks |journal=[[Journal of African Earth Sciences]] |volume=32|issue=1 |pages=103–114|bibcode = 2001JAfES..32..103V }}</ref> Todas las muestras muestran pérdida de isótopos de plomo, pero la intersección del ''errorchron'' (línea recta a través de los puntos de muestra) y la concordia (curva) muestra la edad correcta de la roca.<ref name=Rollinson/>]] |
|||
La [[Datación uranio-plomo|datación radiométrica de uranio-plomo]] implica el uso de uranio 235 o uranio 238 para datar la edad absoluta de una sustancia. Este esquema se ha refinado hasta el punto de que el margen de error en las fechas de las rocas puede llegar a ser de menos de dos millones de años en dos mil quinientos millones de años.<ref name=Oberthuer/><ref>{{Cite journal|doi=10.1016/j.jafrearsci.2004.12.003 |title=The age and petrology of the Chimbadzi Hill Intrusion, NW Zimbabwe: first evidence for early Paleoproterozoic magmatism in Zimbabwe |year=2004 |first=Tawanda D. |last=Manyeruke |author2=Thomas G. Blenkinsop |author3=Peter Buchholz |author4=David Love |author5=Thomas Oberthür |author6=Ulrich K. Vetter |author7=Donald W. Davis |journal=Journal of African Earth Sciences |volume=40|issue=5 |pages=281–292|bibcode = 2004JAfES..40..281M }}</ref> Se ha logrado un margen de error de 2–5% en las rocas [[mesozoicas]] más jóvenes.<ref>{{Cite journal|doi=10.1016/S0009-2541(00)00394-6 |title=Precise <sup>206</sup>Pb/<sup>238</sup>U age determination on zircons by laser ablation microprobe-inductively coupled plasma-mass spectrometry using continuous linear ablation |year=2001 |first1=Xian-hua |last1=Li |first2=Xi-rong|last2=Liang|first3=Min|last3=Sun|first4=Hong|last4=Guan|first5=J. G.|last5=Malpas |journal=Chemical Geology |volume=175|issue=3–4 |pages=209–219|bibcode=2001ChGeo.175..209L}}</ref> |
|||
La datación de plomo y uranio a menudo se realiza en el [[zircón]] [[mineral]] (ZrSiO<sub>4</sub>), aunque se puede usar en otros materiales, como [baddeleyita]], así como [[monazita]] (ver: [[geocronología monazita]]).<ref>{{Cite journal|doi=10.2113/104.1.13 |title=SHRIMP baddeleyite and zircon ages for an Umkondo dolerite sill, Nyanga Mountains, Eastern Zimbabwe |year=2001 |first=M.T.D. |last=Wingate |journal=South African Journal of Geology |volume=104|issue=1 |pages=13–22}}</ref> El circonio y la baddeleyita incorporan átomos de uranio en su estructura cristalina como sustitutos del zirconio, pero rechazan el plomo. El circonio tiene una temperatura de cierre muy alta, es resistente a la intemperie mecánica y es muy inerte químicamente. El circonio también forma múltiples capas de cristal durante los eventos metamórficos, cada uno de los cuales puede registrar una edad isotópica del evento. El análisis de microhaz ''in situ'' se puede lograr mediante técnicas de láser [[ICP-MS]] o [[Secondary ion mass spectrometry|SIMS]].<ref>{{Cite journal|doi=10.1126/science.286.5448.2289 |title=Isotope Geochemistry: New Tools for Isotopic Analysis |date=December 1999 |first=Trevor |last=Ireland |journal=Science |volume=286 |issue=5448 |pages=2289–2290}}</ref> |
|||
Una de sus grandes ventajas es que cualquier muestra proporciona dos relojes, uno basado en la desintegración del uranio 235 a plomo 207 con una vida media de aproximadamente 700 millones de años, y otro basado en la desintegración del uranio 238 al plomo 206 con una semivida de alrededor de 4.500 millones de años, lo que proporciona una verificación cruzada incorporada que permite determinar con precisión la edad de la muestra, incluso si se ha perdido parte del plomo. Esto se puede ver en el diagrama de concordia, donde las muestras se trazan a lo largo de un crona de error (''errorchron'') (línea recta) que cruza la curva de concordia en la edad de la muestra. |
|||
===Método de datación samario-neodimio=== |
|||
{{AP|Datación samario-neodimio}} |
|||
Este método implica la [[desintegración alfa]] de [[Anexo:Isótopos de samario|<sup>147</sup>Sm]] a <sup>143</sup>Nd con una vida media de 1.06 x 10<sup>11</sup> años. Se pueden alcanzar niveles de precisión de veinte millones de años en edades de dos mil quinientos millones de años.<ref>{{Cite journal|doi=10.1016/S0012-821X(98)00228-3 |title=A multielement geochronologic study of the Great Dyke, Zimbabwe: significance of the robust and reset ages |date=December 1998 |first=S. B. |last=Mukasa |author2=A. H. Wilson |author3=R. W. Carlson |journal=Earth and Planetary Science Letters |volume=164 |issue=1–2 |pages=353–369 |bibcode=1998E&PSL.164..353M}}</ref> |
|||
===Método de datación potasio-argón=== |
|||
{{AP|Datación potasio-argón}} |
|||
Este método implica la [[captura de electrones]] o la descomposición de positrones de potasio-40 en argón-40. El potasio-40 tiene una vida media de 1.300 millones de años, por lo que este método es aplicable a las rocas más antiguas. El radiactivo potasio-40 es común en [[mica]]s, [[feldespato]]s y [[hornblenda]]s, aunque la temperatura de cierre es bastante baja en esos materiales, aproximadamente de 350 °C (mica) a 500 °C (hornblenda). |
|||
===Método de datación rubidio-estroncio=== |
|||
{{AP|Datación rubidio-estroncio}} |
|||
Este método se basa en la [[desintegración beta]] del [[Anexo:Isótopos de rubidio|rubidio 87]] a [[Anexo:Isótopos de estroncio|estroncio 87]], con una vida media de 50 mil millones de años. Este esquema se usa para datar [[rocas ígneas]] y [[rocas metamórficas|metamórficas]] antiguas, y también se ha usado para datar [[roca lunar|muestras lunares]]. Las temperaturas de cierre son tan altas que no son motivo de preocupación. La datación de rubidio-estroncio no es tan precisa como el método uranio-plomo, con errores de 30 a 50 millones de años para una muestra de 3 mil millones de años. |
|||
===Método de datación uranio-torio=== |
|||
{{AP|Datación uranio-torio}} |
|||
Una técnica de datación de un rango relativamente corto se basa en la descomposición del uranio-234 en torio-230, una sustancia con una vida media de aproximadamente {{unidad|80000|años}}. Se acompaña de un proceso hermano, en el cual el uranio-235 se desintegra en protactinio-231, que tiene una vida media de {{unidad|32760|años}}. |
|||
Mientras que el [[uranio]] es soluble en agua, el [[torio]] y el [[protactinio]] no lo son, por lo que se precipitan selectivamente en los sedimentos del fondo del océano, a partir de los cuales se miden sus proporciones. El esquema tiene un rango de varios cientos de miles de años. Un método relacionado es la [[datación ionio-torio]], que mide la proporción de [[ionio]] (torio-230) y torio-232 en sedimentos oceánicos. |
|||
===Método de datación por radiocarbono=== |
|||
{{AP|Datación por radiocarbono}} |
|||
[[Image:Ales stenar bred.jpg|upright=1.35|thumb|right|Las [[Piedras de Ale]] en Kåseberga, a unos diez kilómetros al sudeste de [[Ystad]], [[Suecia]] fueron fechadas en 56 CE utilizando el método de carbono 14 del material orgánico encontrado en el sitio<ref>{{Cite web |url=http://www.raa.se/cms/extern/en/places_to_visit/our_historical_sites/ales_stenar.html |title=Ales stenar |publisher=The Swedish National Heritage Board |date=11 October 2006 |accessdate=9 March 2009 |deadurl=yes |archiveurl=https://web.archive.org/web/20090331132307/http://www.raa.se/cms/extern/en/places_to_visit/our_historical_sites/ales_stenar.html |archivedate=31 March 2009 |df=dmy-all }}</ref>]] |
|||
La [[datación por radiocarbono]] también se denomina datación por carbono 14. El carbono 14 es un isótopo radioactivo del carbono, con una vida media de {{unidad|5730|años}},<ref>{{Cite journal|last=Clark |first=R. M. |year=1975 |title=A calibration curve for radiocarbon dates |journal=Antiquity |volume=49 |pages=251–266 |url=http://www.antiquity.ac.uk/ant/049/Ant0490251.htm}}</ref><ref>{{Cite journal|doi=10.5194/angeo-20-115-2002 |first=S. S. |last=Vasiliev |author2=V. A. Dergachev |year=2002 |title=The ~2400-year cycle in atmospheric radiocarbon concentration: Bispectrum of <sup>14</sup>''C'' data over the last 8000 years |journal=Annales Geophysicae |volume=20|issue=1 |pages=115–120 |url=http://www.ann-geophys.net/20/115/2002/angeo-20-115-2002.pdf|bibcode = 2002AnGeo..20..115V }}</ref> (que es muy corto en comparación con los isótopos anteriores) y se descompone en nitrógeno. <ref>{{Cite web|url=http://www.chem.uwec.edu/Chem115_F00/nelsolar/chem.htm|title=Carbon-14 Dating|website=www.chem.uwec.edu|access-date=2016-04-06}}</ref> En otros métodos de datación radiométrica, los pesados isótopos parentales se produjeron por [[nucleosíntesis]] en [[supernova]]s, lo que significa que cualquier isótopo parental con una vida media corta ya debería estar extinto. El carbono 14, sin embargo, se crea continuamente a través de las colisiones de los neutrones generados por los [[rayos cósmicos]] con el nitrógeno en la [[atmósfera superior]] y, por lo tanto, permanece en un nivel casi constante en la Tierra. El carbono 14 termina como un componente traza en el atmosférico [[dióxido de carbono]] (CO<sub>2</sub>). |
|||
Una forma de vida basada en el carbono adquiere carbono durante su vida. Las plantas lo adquieren mediante la [[fotosíntesis]], y los animales lo adquieren del consumo de plantas y de otros animales. Cuando un organismo muere, deja de absorber nuevo carbono 14 y el isótopo existente decae con una vida media característica ({{unidad|5730|años}}). La proporción de carbono 14 que queda cuando se examinan los restos del organismo proporciona una indicación del tiempo transcurrido desde su muerte. Esto hace que el carbono 14 sea un método de datación ideal para datar la edad de los huesos o los restos de un organismo. El límite de datación por carbono 14 se encuentra entre {{unidad|58000|años}} y {{unidad|62000|años}}.<ref>{{Cite journal|first=Wolfango |last=Plastino |author2=Lauri Kaihola |author3=Paolo Bartolomei |author4=Francesco Bella |year=2001 |title=Cosmic background reduction in the radiocarbon measurement by scintillation spectrometry at the underground laboratory of Gran Sasso |url=http://digitalcommons.library.arizona.edu/objectviewer?o=http%3A%2F%2Fradiocarbon.library.arizona.edu%2FVolume43%2FNumber2A%2Fazu_radiocarbon_v43_n2A_157_161_v.pdf |journal=Radiocarbon |volume=43 |issue=2A |pages=157–161}}</ref> |
|||
La tasa de creación de carbono 14 parece ser aproximadamente constante, ya que los controles cruzados de la datación por carbono 14 con otros métodos de datación muestran que da resultados consistentes. Sin embargo, las erupciones locales de volcanes u otros eventos que emiten grandes cantidades de dióxido de carbono pueden reducir las concentraciones locales de carbono 14 y dar fechas inexactas. Las emisiones de dióxido de carbono a la [[biosfera]] como consecuencia de la industrialización también han reducido la proporción de carbono 14 en un pequeño porcentaje; y a la inversa, la cantidad de carbono 14 se incrementó mediante las pruebas en superfice de [[bombas nucleares]] que se realizaron a principios de los años 1960. Además, un aumento del [[viento solar]] o del [[campo magnético]] de la Tierra por encima del valor actual deprimiría la cantidad de carbono 14 creado en la atmósfera. |
|||
===Método de datación por las trazas de fisión=== |
|||
{{AP|Datación por las trazas de fisión}} |
|||
[[Image:Apatite Canada.jpg|thumb|Los cristales de [[apatita]] son ampliamente utilizados en la datación por las trazas de fisión]] |
|||
Este método implica la inspección de un corte pulido de un material para determinar la densidad de las marcas de "traza" (''track'') dejadas en él por la [[fisión espontánea]] de impurezas de uranio 238. El contenido de uranio de la muestra debe ser conocido, pero eso puede determinarse colocando una película de plástico sobre la rebanada pulida del material y bombardeando con [[neutrones termales|neutrones lentos]]. Esto provoca una fisión inducida de <sup>235</sup>U, en oposición a la fisión espontánea de <sup>238</sup>U. Las trazas de fisión producidas por este proceso se registran en la película de plástico. El contenido de uranio del material se puede calcular a partir del número de trazas y del [[flujo de neutrones]]. |
|||
Este esquema tiene aplicación en una amplia gama de fechas geológicas. Para fechas de hasta unos pocos millones de años, se utilizan mejor las [[mica]]s, las [[tectita]]s (fragmentos de vidrio de erupciones volcánicas) y los meteoritos. Los materiales más antiguos se pueden fechar utilizando [[circonio]], [[apatita]], [[titanita]], [[epidota]] y [[granate]] que tienen una cantidad variable de contenido de uranio.<ref>{{Cite journal|doi=10.1016/S0899-5362(01)80066-X |title=A titanite fission track profile across the southeastern Archæan Kaapvaal Craton and the Mesoproterozoic Natal Metamorphic Province, South Africa: evidence for differential cryptic Meso- to Neoproterozoic tectonism |date=August 2001 |first=J. |last=Jacobs |author2=R. J. Thomas |journal=Journal of African Earth Sciences |volume=33 |issue=2 |pages=323–333|bibcode = 2001JAfES..33..323J }}</ref> Debido a que las huellas de fisión se curan con temperaturas de más de 200 °C, la técnica tiene tanto limitaciones como beneficios. La técnica tiene aplicaciones potenciales para detallar la historia térmica de un yacimiento. |
|||
=== Método de datación del cloro 36 === |
|||
Entre 1952 y 1958, se produjeron grandes cantidades del, por lo demás raro, [[Anexo:Isótopos de cloro|<sup>36</sup>Cl]] (semivida ~ 300 ka) durante la detonación atmosférica de las [[armas nucleares]]. El tiempo de residencia del <sup>36</sup>Cl en la atmósfera es de aproximadamente 1 semana. Por lo tanto, como un marcador de eventos de los años 1950 de de agua en el suelo y de agua subterránea, el <sup>36</sup>Cl también es útil para la datación de aguas de menos de 50 años antes del presente. El <sup>36</sup>Cl ha sido usado en otras áreas de las ciencias geológicas, como la datación de hielos y sedimentos. |
|||
=== Métodos de datación por luminiscencia === |
|||
{{AP|datación por luminiscencia}} |
|||
Los métodos de datación por luminiscencia no son métodos de datación radiométrica porque no dependen de la abundancia de isótopos para calcular la edad. En cambio, son una consecuencia de la [[radiación de fondo]] en ciertos minerales. Con el tiempo, la [[radiación ionizante]] es absorbida por los granos minerales en sedimentos y materiales arqueológicos como el [[cuarzo]] y el [[feldespato de potasio]]. La radiación hace que la carga permanezca dentro de los granos en «trampas de electrones» estructuralmente inestables. La exposición a la luz solar o al calor libera esas cargas, lo que «blanquea» la muestra y restablece el reloj a cero. La carga atrapada se acumula con el tiempo hasta una tasa determinada por la cantidad de radiación de fondo en el lugar donde se enterró la muestra. La estimulación de estos granos minerales mediante la luz ([[luminiscencia estimulada ópticamente]] o datación de luminiscencia estimulada con infrarrojos) o el calor ([[datación por termoluminiscencia]]) hace que se emita una señal de luminiscencia a medida que se libera la energía electrónica inestable almacenada, cuya intensidad varía dependiendo de la cantidad de radiación absorbida durante el entierro y de las propiedades específicas del mineral. |
|||
Estos métodos se pueden usar para fechar la edad de una capa de sedimento, ya que las capas depositadas en la parte superior evitarían que los granos se "blanqueasen" y se restableciesen con la luz solar. Los fragmentos de cerámica se pueden fechar hasta la última vez que experimentaron un calor significativo, generalmente cuando fueron horneados en un kiln. |
|||
===Otros métodos=== |
|||
Otros métodos son los siguientes: |
|||
* [[datación argón-argón]] (Ar–Ar) |
|||
* [[datación yodo-xenón]] (I–Xe) |
|||
* [[datación llantano-bario]] (La–Ba) |
|||
* [[datación plomo-plomo]] (Pb–Pb) |
|||
* [[datación lutecio-hafnio]] (Lu–Hf) |
|||
* [[datación potasio-calcio]] (K–Ca) |
|||
* [[datación renio-osmio]] (Re – Os) (Re–Os) |
|||
* [[datación uranio-plomo – helio]] (U–Pb–He) |
|||
* [[datación uranio-uranio]] (U–U) |
|||
* [[datación criptón-criptón]]] (Kr–Kr) |
|||
*[[Anexo:Isótopos de berilio|berilio]] (<sup>10</sup>Be–<sup>9</sup>Be)<ref>Application of the authigenic 10 Be/ 9 Be dating method to Late |
|||
Miocene–Pliocene sequences in the northern Danube Basin;Michal Šujan &a; Global and Planetary Change 137 (2016) 35–53; [https://www.researchgate.net/profile/Michal_Sujan/publication/287807148_Application_of_the_authigenic_10Be9Be_dating_method_to_Late_Miocene-Pliocene_sequences_in_the_northern_Danube_Basin_Pannonian_Basin_System_Confirmation_of_heterochronous_evolution_of_sedimentary_envir/links/5684144b08ae1e63f1f1c4c8/Application-of-the-authigenic-10Be-9Be-dating-method-to-Late-Miocene-Pliocene-sequences-in-the-northern-Danube-Basin-Pannonian-Basin-System-Confirmation-of-heterochronous-evolution-of-sedimentary-envi.pdf pdf]</ref> |
|||
== Datación con productos de decaimiento de radionucleidos extintos de corta duración == |
|||
La datación radiométrica absoluta requiere que una fracción mensurable del núcleo «padre» permanezca en la roca de muestra. Para las rocas que se remontan al principio del sistema solar, ello requiere isótopos «padre» de vida extremadamente larga, lo que hace que la medición de las edades exactas de tales rocas sea imprecisa. Para poder distinguir las edades relativas de las rocas de ese material antiguo y obtener una mejor resolución temporal que la disponible en los isótopos de larga vida, se pueden usar isótopos de corta duración que ya no esten presentes en la roca.<ref>Imke de Pater and Jack J. Lissauer: ''Planetary Sciences'', page 321. Cambridge University Press, 2001. {{ISBN|0-521-48219-4}}</ref> |
|||
Al comienzo del sistema solar, había varios radionucleidos de vida relativamente corta como <sup>26</sup>Al, <sup>60</sup>Fe, <sup>53</sup>Mn y <sup>129</sup>I presentes en la nebulosa solar. Esos radionucleidos, posiblemente producidos por la explosión de una supernova, se han extinguido hoy en día, pero sus productos de desintegración pueden detectarse en material muy antiguo, como el que constituye los [[meteorito]]s. Al medir los productos de descomposición de los radionucleidos extintos con un [[espectrómetro de masas]] y utilizar isocronplots, es posible determinar las edades relativas de diferentes eventos en la historia temprana del sistema solar. Los métodos de datación basados en radionucleidos extintos también se pueden calibrar con el método U-Pb para obtener edades absolutas. Por lo tanto, se puede obtener tanto la edad aproximada como una resolución de tiempo alta. En general, una vida media más corta conduce a una resolución de tiempo mayor a expensas de la escala de tiempo. |
|||
===El cronómetro <sup>129</sup>I – <sup>129</sup>Xe === |
|||
{{VT|Iodine-129#Meteorite age dating}} |
|||
<sup>129</sup>I beta-decays to <sup>129</sup>Xe with a half-life of 16 million years. The iodine-xenon chronometer<ref name=IXe>{{cite journal|last=Gilmour|first=J. D. |author2=O. V Pravdivtseva |author3=A. Busfield |author4=C. M. Hohenberg|title=The I-Xe Chronometer and the Early Solar System|journal=Meteoritics and Planetary Science|year=2006|volume=41|pages=19–31|doi=10.1111/j.1945-5100.2006.tb00190.x|url=http://articles.adsabs.harvard.edu/cgi-bin/nph-iarticle_query?bibcode=2006M%26PS...41...19G&db_key=AST&page_ind=0&data_type=GIF&type=SCREEN_VIEW&classic=YES|accessdate=2013-01-21|bibcode = 2006M&PS...41...19G }}</ref> is an isochron technique. Samples are exposed to neutrons in a nuclear reactor. This converts the only stable isotope of iodine (<sup>127</sup>I) into <sup>128</sup>Xe via neutron capture followed by beta decay (of <sup>128</sup>I). After irradiation, samples are heated in a series of steps and the xenon [[isotopic signature]] of the gas evolved in each step is analysed. When a consistent <sup>129</sup>Xe/<sup>128</sup>Xe ratio is observed across several consecutive temperature steps, it can be interpreted as corresponding to a time at which the sample stopped losing xenon. |
|||
Samples of a meteorite called Shallowater are usually included in the irradiation to monitor the conversion efficiency from <sup>127</sup>I to <sup>128</sup>Xe. The difference between the measured <sup>129</sup>Xe/<sup>128</sup>Xe ratios of the sample and Shallowater then corresponds to the different ratios of <sup>129</sup>I/<sup>127</sup>I when they each stopped losing xenon. This in turn corresponds to a difference in age of closure in the early solar system. |
|||
Ver también: Iodine-129 § Meteorite data de edad |
|||
129 I beta-decae a 129 Xe con una vida media de 16 millones de años. El cronómetro de yodo-xenón [32] es una técnica isócrona. Las muestras se exponen a neutrones en un reactor nuclear. Esto convierte el único isótopo estable de yodo (127 I) en 128 Xe a través de la captura de neutrones seguido de desintegración beta (de 128 I). Después de la irradiación, las muestras se calientan en una serie de pasos y se analiza la firma isotópica de xenón del gas evolucionado en cada paso. Cuando se observa una relación constante de 129 Xe / 128 Xe en varios pasos de temperatura consecutivos, se puede interpretar como correspondiente a un momento en el que la muestra dejó de perder el xenón. |
|||
Las muestras de un meteorito llamado Shallowater generalmente se incluyen en la irradiación para monitorear la eficiencia de conversión de 127 I a 128 Xe. La diferencia entre las relaciones medidas de 129 Xe / 128 Xe de la muestra y Shallowater corresponde a las diferentes relaciones de 129 I / 127 I cuando cada una de ellas dejó de perder el xenón. Esto, a su vez, corresponde a una diferencia en la edad de cierre en el sistema solar temprano. |
|||
===El cronómetro <sup>26</sup>Al – <sup>26</sup>Mg === |
|||
Otro ejemplo de la datación de radionucleidos extintos de corta duración es el cronómetro de [[Aluminio 26|<sup>26</sup>Al]] – <sup>26</sup>Mg, que se puede usar para estimar las edades relativas de los [[condrules]]. El <sup>26</sup>Al se desintegra en <sup>26</sup>Mg con una vida media de 720 000 años. La datación es simplemente una cuestión de encontrar la desviación de la [[abundancia natural]] del <sup>26</sup>Mg (el producto de la desintegración del <sup>26</sup>Al) en comparación con la relación de los isótopos estables <sup>27</sup>Al/<sup>24</sup>Mg. |
|||
El exceso de <sup>26</sup>Mg (a menudo designado <sup>26</sup>Mg*) se encuentra comparando la relación de <sup>26</sup>Mg/<sup>27</sup>Mg con la de otros materiales del sistema solar.<ref>Alexander N. Krot(2002) Dating the Earliest Solids in our Solar System, Hawai'i Institute of Geophysics and Planetology http://www.psrd.hawaii.edu/Sept02/isotopicAges.html.</ref> |
|||
El cronómetro de <sup>26</sup>Al – <sup>26</sup>Mg da una estimación del período de tiempo para la formación de meteoritos primitivos de solo unos pocos millones de años (1,4 millones de años para la formación del condrulo).<ref>Imke de Pater and Jack J. Lissauer: ''Planetary Sciences'', page 322. Cambridge University Press, 2001. {{ISBN|0-521-48219-4}}</ref> |
|||
== Véase también == |
== Véase también == |
||
* [[Métodos de datación en arqueología]] |
* [[Métodos de datación en arqueología]] |
||
| Línea 47: | Línea 185: | ||
* [[Datación samario-neodimio]] |
* [[Datación samario-neodimio]] |
||
* [[Edad de la Tierra]] |
* [[Edad de la Tierra]] |
||
* [[Historia de la geología]]* [[Circonio hadeano]] |
|||
* [[Geología]] |
|||
* [[Geoquímica de isótopos]] |
|||
* [[Registro paleopedológico]] |
|||
* [[Radioactividad]] |
|||
* [[Radiohalo]] |
|||
* [[SHRIMP|Microbomba de iones de alta resolución sensible (SHRIMP)]] |
|||
{{portal|Earth sciences|Geophysics|Physics}} |
|||
== Notas == |
|||
{{listaref|2}} |
|||
== Referencias == |
== Referencias == |
||
{{traducido ref|en|Radiometric dating}} |
|||
{{Listaref}} |
|||
== Bibliografía== |
|||
* {{cite journal|last1=Gunten|first1=Hans R. von|title=Radioactivity: A Tool to Explore the Past|journal=Radiochimica Acta|volume=70-71|issue=s1|year=1995|issn=2193-3405|doi=10.1524/ract.1995.7071.special-issue.305}} |
|||
* {{cite book|title=Radioactivity Radionuclides Radiation |chapter=Archaeology and Dating| first1=Joseph |last1=Magill |first2=Jean |last2=Galy |publisher=Springer Berlin Heidelberg |year=2005|pages=105–115|doi=10.1007/3-540-26881-2_6 |isbn=978-3-540-26881-9}} |
|||
* {{cite book|isbn=978-0521862288 |title=Isotope Geology|last1=Allègre|first1=Claude J|date=2008-12-04}} |
|||
* {{cite book|isbn=978-0-231-12440-9 |title=Geochemistry: Pathways and Processes |edition=2|last1=McSween |first1=Harry Y |last2=Richardson |first2=Steven Mcafee |last3=Uhle |first3=Maria E |last4=Uhle |first4=Professor Maria |year=2003 }} |
|||
* {{cite book|isbn=978-0-521-87862-3 |title= Cosmochemistry|last1= Harry y. Mcsween|first1= Jr|last2= Huss|first2= Gary R|date= 2010-04-29}} |
|||
{{Chronology}} |
|||
[[Category:Radiometric dating|*]] |
|||
[[Category:Conservation and restoration]] |
|||
[[Categoría:Instrumentos de medición]] |
[[Categoría:Instrumentos de medición]] |
||
Revisión del 17:11 9 may 2019
La datación radiométrica, datación radioactiva o datación por radioisótopos es una técnica utilizada para datar materiales como rocas, minerales y restos orgánicos (carbono), en los que se incorporaron de manera selectiva impurezas radiactivas cuando se formaron. El método se basa en la comparación de la abundancia de un radionucleido de ocurrencia natural dentro del material con la abundancia de sus productos de descomposición, que se forman a unatasa constante de desintegración conocida.[1] El uso de la datación radiométrica fue publicado por primera vez en 1907 por Bertram Boltwood[2] —avanzado por Ernest Rutherford en 1905— y ahora es la principal fuente de información sobre la edad absoluta de las rocas y otras características geológicas, incluida la edad de las formas de vida fosilizadas o la propia edad de la Tierra, y también se puede utilizar para datar una amplia gama de materiales naturales y artefactos.[3]
Junto con los principios estratigráficos, los métodos de datación radiométrica se utilizan en geocronología para establecer la escala de tiempo geológica.[4] Entre las técnicas más conocidas están la datación potasio-argón, la datación uranio-plomo y la datación por radiocarbono (basada en la desintegración del isótopo carbono 14), comúnmente utilizada para la datación de restos orgánicos relativamente recientes, de hasta 60 000 años.[5] (Otros dataciones posibles son K/Ar, U/Pb, Rb/Sr, Sm/Nd, etc.[6])
Al permitir el establecimiento de escalas de tiempo geológicas, proporciona una importante fuente de información sobre las edades de los fósiles y las tasas deducidas de cambio evolutivo. La datación radiométrica también se utiliza para datar materiales arqueológicos, incluidos artefactos antiguos. Los diferentes métodos de datación radiométrica varían según sea la escala de tiempo en la que son precisos y de los materiales a los que se pueden aplicar.
Fundamentos
Desintegración radioactiva
Toda la materia ordinaria se compone de combinaciones de elementos químicos, cada uno con su propio número atómico, que indica el número de protones en el núcleo atómico. Además, los elementos pueden existir en diferentes isótopos, con cada isótopo de un elemento difiriendo en el número de neutrones en el núcleo. Un isótopo particular de un elemento particular se llama nucleido. Algunos nucleidos son inherentemente inestables. Es decir, en algún momento en el tiempo, un átomo de tal nucleido sufrirá un decaimiento radioactivo y se transformará espontáneamente en un nucleido diferente. Esta transformación se puede lograr de varias maneras diferentes, incluida la desintegración alfa (emisión de partículas alfa) y la desintegración beta (emisión de electrones, emisión de positrones o captura de electrones). Otra posibilidad es la fisión espontánea en dos o más nucleidos.
Si bien el momento en el que un núcleo particular se desintegra es impredecible, una colección de átomos de un nucleido radiactivo decae exponencialmente a una tasa descrita por un parámetro conocido como vida media, generalmente dada en unidades de años cuando se estudian las técnicas de datación. Después de que haya transcurrido una vida media, la mitad de los átomos del nucleido en cuestión se habrán desintegrado en un nucleido «hijo» o producto de desintegración. En muchos casos, el nucleido «hijo» en sí mismo es radioactivo, lo que resulta en una nueva cadena de desintegración, que finalmente termina con la formación de un nucleido «hijo» estable (no radioactivo); cada paso en tal cadena se caracteriza por una vida media distinta. En estos casos, generalmente la vida media de interés en la datación radiométrica es la más larga de la cadena, que es el factor limitante de la velocidad en la transformación final del nucleido radioactivo en su «hijo» estable. Los sistemas isotópicos que han sido explotados para la datación radiométrica tienen vidas medias que van desde solo unos 10 años (por ejemplo, tritio) hasta los más de 100 mil millones de años (por ejemplo, el samario 147).[7]
Para la mayoría de los nucleidos radiactivos, la vida media depende únicamente de las propiedades nucleares y es esencialmente una constante. No se ve afectado por factores externos como la temperatura, la presión, el entorno químico o la presencia de un campo magnético o eléctrico.[8][9][10] Las únicas excepciones son los nucleidos que se descomponen por el proceso de captura de electrones, como el berilio 7, el estroncio 85 y el circonio 89, cuya tasa de decaimiento puede verse afectada por la densidad electrónica local. Para todos los demás nucleidos, la proporción del nucleido original en relación a sus productos de desintegración cambia de manera predecible a medida que el nucleido original decae con el tiempo. Esta previsibilidad permite que las abundancias relativas de los nucleidos relacionados se utilicen como un reloj para medir el tiempo desde la incorporación de los nucleidos originales en un material hasta el presente.
Precisión de la datación radiométrica

La ecuación básica de la datación radiométrica requiere que ni el nucleido «padre» ni el producto «hijo» puedan entrar o salir del material después de su formación. Los posibles efectos de confusión de la contaminación de los isótopos «padre» e «hijo» deben considerarse, al igual que los efectos de cualquier pérdida o ganancia de dichos isótopos desde que se creó la muestra. Por lo tanto, es esencial contar con la mayor cantidad de información posible sobre el material que se está datando y verificar posibles signos de alteración.[11] La precisión se mejora si las mediciones se toman en múltiples muestras de diferentes ubicaciones del cuerpo de roca. Alternativamente, si se pueden datar varios minerales diferentes de la misma muestra y se supone que fueron formados por el mismo evento y que estaban en equilibrio con el yacimiento cuando se formaron, deberían formar una isocrona. Esto puede reducir el problema de la contaminación. En la datación uranio-plomo, se utiliza el diagrama de concordia que también disminuye el problema de la pérdida de nucleidos. Finalmente, la correlación entre los diferentes métodos de datación isotópica puede ser necesaria para confirmar la edad de una muestra. Por ejemplo, se determinó que la edad de los gneises de Amitsoq, en el oeste de Groenlandia, era de 3,6 ± 0.05 millones de años (Ma) utilizando la datación plomo-uranio y de 3,56 ± 0.10 Ma utilizando la datación de plomo-plomo, resultados que coinciden entre sí.[12]: 142–143
Una datación radiométrica precisa generalmente requiere que el «padre» tenga una vida media lo suficientemente larga como para que esté presente en cantidades significativas en el momento de la medición (excepto, como se describe a continuación, en la «Datación con radionucleidos extintos de vida corta»), que la vida media del «padre» se conozca con precisión y que se produzca suficiente cantidad del producto «hijo» para medirlo y distinguirlo de la cantidad inicial del «hijo» presente en el material. Los procedimientos utilizados para aislar y analizar los nucleidos «padre» e «hijo» deben ser precisos y seguros. Esto normalmente implica el uso de espectrometría de masas de relación isotópica.[13]
La precisión de un método de datación depende en parte de la vida media del isótopo radioactivo involucrado. Por ejemplo, el carbono 14 tiene una vida media de 5730 años. Después de que un organismo haya estado muerto desde hace 60 000 años, queda tan poco carbono 14 que no se puede establecer una datación precisa. Por otro lado, la concentración de carbono-14 cae tan abruptamente que la edad de los restos relativamente jóvenes se puede determinar con una precisión de unas pocas décadas.[14]
Temperatura de cierre
Si un material que rechaza selectivamente el nucleido hijo se calienta, cualquier nucleido hijo que se haya acumulado a lo largo del tiempo se perderá por difusión, lo que pondrá a cero el reloj isotópico. La temperatura a la que sucede esto se conoce como temperatura de cierre o temperatura de bloqueo y es específica de cada material en particular y sistema isotópico. Estas temperaturas se determinan experimentalmente en el laboratorio mediante el restablecimiento artificial de los minerales de muestra utilizando un horno de alta temperatura. A medida que el mineral se enfría, comienza a formarse la estructura cristalina y la difusión de los isótopos es menos fácil. A cierta temperatura, la estructura cristalina se ha formado lo suficiente como para evitar la difusión de isótopos. Esa temperatura es lo que se conoce como temperatura de cierre y representa la temperatura por debajo de la cual el mineral es un sistema cerrado para los isótopos. Por lo tanto, una roca o masa fundida ígnea o metamórfica, que se está enfriando lentamente, no comienza a mostrar una disminución radiactiva mensurable hasta que se enfríe por debajo de la temperatura de cierre. La edad que se puede calcular por datación radiométrica es, por lo tanto, el momento en que la roca o el mineral se enfriaron hasta la temperatura de cierre.[15][16] La datación de diferentes minerales y/o sistemas de isótopos (con diferentes temperaturas de cierre) dentro de la misma roca puede, por lo tanto, permitir el seguimiento de la historia térmica de la roca en cuestión en el tiempo, y por lo tanto la historia de los eventos metamórficos puede ser conocida en detalle. Este campo se conoce como termocronología o termocronometría.
Ecuación de datación

La expresión matemática que relaciona la desintegración radioactiva con el tiempo geológico es:[15][18]
o
siendo:
- , la edad de la muestra,
- , el número de átomos del isótopo «hijo» en la muestra,
- , el número de átomos del isótopo «hijo» en la composición original (igual al n.º de átomos «padre» que han decaído radioactivamente),
- , el número de átomos del isótopo «padre» en la muestra en el momento t (el presente), dado por N(t) = Noe-λt, y
- , la constante de desintegración radiactiva del isótopo «padre», igual a la inversa de la vida media —duración promedio de un isótopo radiactivo previa a su desintegración— del isótopo «padre»[19] multiplicado por el logaritmo neperiano o natural () de 2. La vida media es igual a la inversa de la constante de desintegración radiactiva: . Al tiempo que transcurre hasta que la cantidad de nucleidos se reduce a la mitad de la cantidad inicial se le denomina periodo de semidesintegración, periodo, semiperiodo o semivida (no confundir con la vida media): . Al final de cada período de semidesintegración la radiactividad se reduce a la mitad (de la inicial). A cada radioisótopo le corresponde un período de semidesintegración característico, en general diferente de los respectivos de otros isótopos.
| Principales dataciones | |||
| Isótopo | Período | Emisión | |
|---|---|---|---|
| Radón 222 | 3,82 días | Alfa | |
| Cobalto 60 | 5271 años | Gamma | |
| Carbono 14 | 5730 años | Beta | |
| Uranio 238 | 4510 millones de años[20] | Alfa | |
La ecuación se expresa mejor en términos de la cantidad medida en lugar del valor inicial constante .
La ecuación anterior hace uso de la información sobre la composición de los isótopos «padre» e «hijo» en el momento en que el material que se está probando se enfrió por debajo de su temperatura de cierre. Esto está bien establecido para la mayoría de los sistemas isotópicos.[16][21] Sin embargo, la construcción de una isocrona no requiere información sobre las composiciones originales, utilizando simplemente las relaciones actuales de los isótopos «padre» e «hijo» de un isótopo estándar. El trazado de una isocrona se utiliza para resolver gráficamente la ecuación de edad y calcular la edad de la muestra y la composición original.
Esta ecuación es válida siempre que el modo de decaimiento del isótopo «padre» sea único y que el isótopo «hijo» sea estable. Para otros casos se pueden obtener ecuaciones más complejas, en las que se tienen en cuenta múltiples decaimientos posibles.
Métodos modernos de datación
La datación radiométrica se conoce desde 1905, cuando fue ideada por Ernest Rutherford como un método por el cual se podría determinar la edad de la Tierra. En el siglo transcurrido desde entonces, las técnicas se han mejorado y ampliado enormemente.[19] La datación se puede realizar ahora en muestras muy pequeñas, del orden de un nanogramo, usando un espectrómetro de masas. El espectrómetro de masas se inventó en la década de 1940 y comenzó a usarse en la datación radiométrica en la década de 1950. Opera generando un haz de átomos ionizados a partir de la muestra a prueba. Luego, los iones viajan a través de un campo magnético, que los desvía hacia diferentes sensores de muestreo, conocidos como «copas de Faraday», según sean su masa y nivel de ionización. Al impactar en las copas, los iones establecen una corriente muy débil que puede medirse para determinar la tasa de impactos y las concentraciones relativas de los diferentes átomos en los haces.
Método de datación uranio-plomo

La datación radiométrica de uranio-plomo implica el uso de uranio 235 o uranio 238 para datar la edad absoluta de una sustancia. Este esquema se ha refinado hasta el punto de que el margen de error en las fechas de las rocas puede llegar a ser de menos de dos millones de años en dos mil quinientos millones de años.[17][23] Se ha logrado un margen de error de 2–5% en las rocas mesozoicas más jóvenes.[24]
La datación de plomo y uranio a menudo se realiza en el zircón mineral (ZrSiO4), aunque se puede usar en otros materiales, como [baddeleyita]], así como monazita (ver: geocronología monazita).[25] El circonio y la baddeleyita incorporan átomos de uranio en su estructura cristalina como sustitutos del zirconio, pero rechazan el plomo. El circonio tiene una temperatura de cierre muy alta, es resistente a la intemperie mecánica y es muy inerte químicamente. El circonio también forma múltiples capas de cristal durante los eventos metamórficos, cada uno de los cuales puede registrar una edad isotópica del evento. El análisis de microhaz in situ se puede lograr mediante técnicas de láser ICP-MS o SIMS.[26]
Una de sus grandes ventajas es que cualquier muestra proporciona dos relojes, uno basado en la desintegración del uranio 235 a plomo 207 con una vida media de aproximadamente 700 millones de años, y otro basado en la desintegración del uranio 238 al plomo 206 con una semivida de alrededor de 4.500 millones de años, lo que proporciona una verificación cruzada incorporada que permite determinar con precisión la edad de la muestra, incluso si se ha perdido parte del plomo. Esto se puede ver en el diagrama de concordia, donde las muestras se trazan a lo largo de un crona de error (errorchron) (línea recta) que cruza la curva de concordia en la edad de la muestra.
Método de datación samario-neodimio
Este método implica la desintegración alfa de 147Sm a 143Nd con una vida media de 1.06 x 1011 años. Se pueden alcanzar niveles de precisión de veinte millones de años en edades de dos mil quinientos millones de años.[27]
Método de datación potasio-argón
Este método implica la captura de electrones o la descomposición de positrones de potasio-40 en argón-40. El potasio-40 tiene una vida media de 1.300 millones de años, por lo que este método es aplicable a las rocas más antiguas. El radiactivo potasio-40 es común en micas, feldespatos y hornblendas, aunque la temperatura de cierre es bastante baja en esos materiales, aproximadamente de 350 °C (mica) a 500 °C (hornblenda).
Método de datación rubidio-estroncio
Este método se basa en la desintegración beta del rubidio 87 a estroncio 87, con una vida media de 50 mil millones de años. Este esquema se usa para datar rocas ígneas y metamórficas antiguas, y también se ha usado para datar muestras lunares. Las temperaturas de cierre son tan altas que no son motivo de preocupación. La datación de rubidio-estroncio no es tan precisa como el método uranio-plomo, con errores de 30 a 50 millones de años para una muestra de 3 mil millones de años.
Método de datación uranio-torio
Una técnica de datación de un rango relativamente corto se basa en la descomposición del uranio-234 en torio-230, una sustancia con una vida media de aproximadamente 80 000 años. Se acompaña de un proceso hermano, en el cual el uranio-235 se desintegra en protactinio-231, que tiene una vida media de 32 760 años.
Mientras que el uranio es soluble en agua, el torio y el protactinio no lo son, por lo que se precipitan selectivamente en los sedimentos del fondo del océano, a partir de los cuales se miden sus proporciones. El esquema tiene un rango de varios cientos de miles de años. Un método relacionado es la datación ionio-torio, que mide la proporción de ionio (torio-230) y torio-232 en sedimentos oceánicos.
Método de datación por radiocarbono

La datación por radiocarbono también se denomina datación por carbono 14. El carbono 14 es un isótopo radioactivo del carbono, con una vida media de 5730 años,[29][30] (que es muy corto en comparación con los isótopos anteriores) y se descompone en nitrógeno. [31] En otros métodos de datación radiométrica, los pesados isótopos parentales se produjeron por nucleosíntesis en supernovas, lo que significa que cualquier isótopo parental con una vida media corta ya debería estar extinto. El carbono 14, sin embargo, se crea continuamente a través de las colisiones de los neutrones generados por los rayos cósmicos con el nitrógeno en la atmósfera superior y, por lo tanto, permanece en un nivel casi constante en la Tierra. El carbono 14 termina como un componente traza en el atmosférico dióxido de carbono (CO2).
Una forma de vida basada en el carbono adquiere carbono durante su vida. Las plantas lo adquieren mediante la fotosíntesis, y los animales lo adquieren del consumo de plantas y de otros animales. Cuando un organismo muere, deja de absorber nuevo carbono 14 y el isótopo existente decae con una vida media característica (5730 años). La proporción de carbono 14 que queda cuando se examinan los restos del organismo proporciona una indicación del tiempo transcurrido desde su muerte. Esto hace que el carbono 14 sea un método de datación ideal para datar la edad de los huesos o los restos de un organismo. El límite de datación por carbono 14 se encuentra entre 58 000 años y 62 000 años.[32]
La tasa de creación de carbono 14 parece ser aproximadamente constante, ya que los controles cruzados de la datación por carbono 14 con otros métodos de datación muestran que da resultados consistentes. Sin embargo, las erupciones locales de volcanes u otros eventos que emiten grandes cantidades de dióxido de carbono pueden reducir las concentraciones locales de carbono 14 y dar fechas inexactas. Las emisiones de dióxido de carbono a la biosfera como consecuencia de la industrialización también han reducido la proporción de carbono 14 en un pequeño porcentaje; y a la inversa, la cantidad de carbono 14 se incrementó mediante las pruebas en superfice de bombas nucleares que se realizaron a principios de los años 1960. Además, un aumento del viento solar o del campo magnético de la Tierra por encima del valor actual deprimiría la cantidad de carbono 14 creado en la atmósfera.
Método de datación por las trazas de fisión

Este método implica la inspección de un corte pulido de un material para determinar la densidad de las marcas de "traza" (track) dejadas en él por la fisión espontánea de impurezas de uranio 238. El contenido de uranio de la muestra debe ser conocido, pero eso puede determinarse colocando una película de plástico sobre la rebanada pulida del material y bombardeando con neutrones lentos. Esto provoca una fisión inducida de 235U, en oposición a la fisión espontánea de 238U. Las trazas de fisión producidas por este proceso se registran en la película de plástico. El contenido de uranio del material se puede calcular a partir del número de trazas y del flujo de neutrones.
Este esquema tiene aplicación en una amplia gama de fechas geológicas. Para fechas de hasta unos pocos millones de años, se utilizan mejor las micas, las tectitas (fragmentos de vidrio de erupciones volcánicas) y los meteoritos. Los materiales más antiguos se pueden fechar utilizando circonio, apatita, titanita, epidota y granate que tienen una cantidad variable de contenido de uranio.[33] Debido a que las huellas de fisión se curan con temperaturas de más de 200 °C, la técnica tiene tanto limitaciones como beneficios. La técnica tiene aplicaciones potenciales para detallar la historia térmica de un yacimiento.
Método de datación del cloro 36
Entre 1952 y 1958, se produjeron grandes cantidades del, por lo demás raro, 36Cl (semivida ~ 300 ka) durante la detonación atmosférica de las armas nucleares. El tiempo de residencia del 36Cl en la atmósfera es de aproximadamente 1 semana. Por lo tanto, como un marcador de eventos de los años 1950 de de agua en el suelo y de agua subterránea, el 36Cl también es útil para la datación de aguas de menos de 50 años antes del presente. El 36Cl ha sido usado en otras áreas de las ciencias geológicas, como la datación de hielos y sedimentos.
Métodos de datación por luminiscencia
Los métodos de datación por luminiscencia no son métodos de datación radiométrica porque no dependen de la abundancia de isótopos para calcular la edad. En cambio, son una consecuencia de la radiación de fondo en ciertos minerales. Con el tiempo, la radiación ionizante es absorbida por los granos minerales en sedimentos y materiales arqueológicos como el cuarzo y el feldespato de potasio. La radiación hace que la carga permanezca dentro de los granos en «trampas de electrones» estructuralmente inestables. La exposición a la luz solar o al calor libera esas cargas, lo que «blanquea» la muestra y restablece el reloj a cero. La carga atrapada se acumula con el tiempo hasta una tasa determinada por la cantidad de radiación de fondo en el lugar donde se enterró la muestra. La estimulación de estos granos minerales mediante la luz (luminiscencia estimulada ópticamente o datación de luminiscencia estimulada con infrarrojos) o el calor (datación por termoluminiscencia) hace que se emita una señal de luminiscencia a medida que se libera la energía electrónica inestable almacenada, cuya intensidad varía dependiendo de la cantidad de radiación absorbida durante el entierro y de las propiedades específicas del mineral.
Estos métodos se pueden usar para fechar la edad de una capa de sedimento, ya que las capas depositadas en la parte superior evitarían que los granos se "blanqueasen" y se restableciesen con la luz solar. Los fragmentos de cerámica se pueden fechar hasta la última vez que experimentaron un calor significativo, generalmente cuando fueron horneados en un kiln.
Otros métodos
Otros métodos son los siguientes:
- datación argón-argón (Ar–Ar)
- datación yodo-xenón (I–Xe)
- datación llantano-bario (La–Ba)
- datación plomo-plomo (Pb–Pb)
- datación lutecio-hafnio (Lu–Hf)
- datación potasio-calcio (K–Ca)
- datación renio-osmio (Re – Os) (Re–Os)
- datación uranio-plomo – helio (U–Pb–He)
- datación uranio-uranio (U–U)
- datación criptón-criptón] (Kr–Kr)
- berilio (10Be–9Be)[34]
Datación con productos de decaimiento de radionucleidos extintos de corta duración
La datación radiométrica absoluta requiere que una fracción mensurable del núcleo «padre» permanezca en la roca de muestra. Para las rocas que se remontan al principio del sistema solar, ello requiere isótopos «padre» de vida extremadamente larga, lo que hace que la medición de las edades exactas de tales rocas sea imprecisa. Para poder distinguir las edades relativas de las rocas de ese material antiguo y obtener una mejor resolución temporal que la disponible en los isótopos de larga vida, se pueden usar isótopos de corta duración que ya no esten presentes en la roca.[35]
Al comienzo del sistema solar, había varios radionucleidos de vida relativamente corta como 26Al, 60Fe, 53Mn y 129I presentes en la nebulosa solar. Esos radionucleidos, posiblemente producidos por la explosión de una supernova, se han extinguido hoy en día, pero sus productos de desintegración pueden detectarse en material muy antiguo, como el que constituye los meteoritos. Al medir los productos de descomposición de los radionucleidos extintos con un espectrómetro de masas y utilizar isocronplots, es posible determinar las edades relativas de diferentes eventos en la historia temprana del sistema solar. Los métodos de datación basados en radionucleidos extintos también se pueden calibrar con el método U-Pb para obtener edades absolutas. Por lo tanto, se puede obtener tanto la edad aproximada como una resolución de tiempo alta. En general, una vida media más corta conduce a una resolución de tiempo mayor a expensas de la escala de tiempo.
El cronómetro 129I – 129Xe
129I beta-decays to 129Xe with a half-life of 16 million years. The iodine-xenon chronometer[36] is an isochron technique. Samples are exposed to neutrons in a nuclear reactor. This converts the only stable isotope of iodine (127I) into 128Xe via neutron capture followed by beta decay (of 128I). After irradiation, samples are heated in a series of steps and the xenon isotopic signature of the gas evolved in each step is analysed. When a consistent 129Xe/128Xe ratio is observed across several consecutive temperature steps, it can be interpreted as corresponding to a time at which the sample stopped losing xenon.
Samples of a meteorite called Shallowater are usually included in the irradiation to monitor the conversion efficiency from 127I to 128Xe. The difference between the measured 129Xe/128Xe ratios of the sample and Shallowater then corresponds to the different ratios of 129I/127I when they each stopped losing xenon. This in turn corresponds to a difference in age of closure in the early solar system.
Ver también: Iodine-129 § Meteorite data de edad
129 I beta-decae a 129 Xe con una vida media de 16 millones de años. El cronómetro de yodo-xenón [32] es una técnica isócrona. Las muestras se exponen a neutrones en un reactor nuclear. Esto convierte el único isótopo estable de yodo (127 I) en 128 Xe a través de la captura de neutrones seguido de desintegración beta (de 128 I). Después de la irradiación, las muestras se calientan en una serie de pasos y se analiza la firma isotópica de xenón del gas evolucionado en cada paso. Cuando se observa una relación constante de 129 Xe / 128 Xe en varios pasos de temperatura consecutivos, se puede interpretar como correspondiente a un momento en el que la muestra dejó de perder el xenón.
Las muestras de un meteorito llamado Shallowater generalmente se incluyen en la irradiación para monitorear la eficiencia de conversión de 127 I a 128 Xe. La diferencia entre las relaciones medidas de 129 Xe / 128 Xe de la muestra y Shallowater corresponde a las diferentes relaciones de 129 I / 127 I cuando cada una de ellas dejó de perder el xenón. Esto, a su vez, corresponde a una diferencia en la edad de cierre en el sistema solar temprano.
El cronómetro 26Al – 26Mg
Otro ejemplo de la datación de radionucleidos extintos de corta duración es el cronómetro de 26Al – 26Mg, que se puede usar para estimar las edades relativas de los condrules. El 26Al se desintegra en 26Mg con una vida media de 720 000 años. La datación es simplemente una cuestión de encontrar la desviación de la abundancia natural del 26Mg (el producto de la desintegración del 26Al) en comparación con la relación de los isótopos estables 27Al/24Mg.
El exceso de 26Mg (a menudo designado 26Mg*) se encuentra comparando la relación de 26Mg/27Mg con la de otros materiales del sistema solar.[37]
El cronómetro de 26Al – 26Mg da una estimación del período de tiempo para la formación de meteoritos primitivos de solo unos pocos millones de años (1,4 millones de años para la formación del condrulo).[38]
Véase también
- Métodos de datación en arqueología
- Datación por radiocarbono
- Datación potasio-argón
- Datación uranio-torio
- Datación uranio-plomo
- Datación samario-neodimio
- Edad de la Tierra
- Historia de la geología* Circonio hadeano
- Geoquímica de isótopos
- Registro paleopedológico
- Radioactividad
- Radiohalo
- Microbomba de iones de alta resolución sensible (SHRIMP)
 Portal:Earth sciences. Contenido relacionado con Geophysics.
Portal:Earth sciences. Contenido relacionado con Geophysics.
Notas
- ↑ Unión Internacional de Química Pura y Aplicada. «radioactive dating». Compendium of Chemical Terminology. Versión en línea (en inglés).
- ↑ Boltwood, Bertram (1907). «The Ultimate Disintegration Products of the Radio-active Elements. Part II. The disintegration products of uranium». American Journal of Science. 4 23 (134): 77-88. doi:10.2475/ajs.s4-23.134.78.
- ↑ [1] Geologic Time: Radiometric Time Scale". United States Geological Survey.
- ↑ McRae, A. 1998. Radiometric Dating and the Geological Time Scale: Circular Reasoning or Reliable Tools? Radiometric Dating and the Geological Time Scale TalkOrigins Archive
- ↑ EQUIPO (2000). Diccionario de ciencias de la tierra. Editorial Complutense. ISBN 9788489784772. Consultado el 19 de febrero de 2018.
- ↑ Los isótopos radiactivos y nuestro pasado
- ↑ Bernard-Griffiths, J.; Groan, G. (1989). «The samarium–neodymium method». En Roth, Etienne; Poty, Bernard, eds. Nuclear Methods of Dating. Springer Netherlands. pp. 53 - 72. ISBN 978-0-7923-0188-2.
- ↑ Emery, G T (1972). «Perturbation of Nuclear Decay Rates». Annual Review of Nuclear Science 22 (1): 165-202. Bibcode:1972ARNPS..22..165E. doi:10.1146/annurev.ns.22.120172.001121.
- ↑ Shlyakhter, A. I. (1976). «Direct test of the constancy of fundamental nuclear constants». Nature 264 (5584): 340. Bibcode:1976Natur.264..340S. doi:10.1038/264340a0.
- ↑ Johnson, B. 1993. How to Change Nuclear Decay Rates Usenet Physics FAQ
- ↑ Stewart, K,, Turner, S, Kelley, S, Hawkesworh, C Kristein, L and Manotvani, M (1996). «3-D, 40Ar---39Ar geochronology in the Paraná continental flood basalt province». Earth and Planetary Science Letters 143 (1–4): 95-109. Bibcode:1996E&PSL.143...95S. doi:10.1016/0012-821X(96)00132-X.
- ↑ Dalrymple, G. Brent (1994). The age of the earth. Stanford, Calif.: Stanford Univ. Press. ISBN 9780804723312.
- ↑ Dickin, Alan P. (2008). Radiogenic isotope geology (2nd edición). Cambridge: Cambridge Univ. Press. pp. 15–49. ISBN 9780521530170.
- ↑ «INTCAL04 Terrestrial Radiocarbon Age Calibration, 0–26 Cal Kyr BP». Radiocarbon 46 (3): 1029-1058. 2004. Parámetro desconocido
|vauthors=ignorado (ayuda) - ↑ a b Faure, Gunter (1998). Principles and applications of geochemistry: a comprehensive textbook for geology students (2nd edición). Englewood Cliffs, New Jersey: Prentice Hall. ISBN 978-0-02-336450-1. OCLC 37783103.[página requerida]
- ↑ a b c Rollinson, Hugh R. (1993). Using geochemical data: evaluation, presentation, interpretation. Harlow: Longman. ISBN 978-0-582-06701-1. OCLC 27937350.[página requerida]
- ↑ a b Oberthür, T, Davis, DW, Blenkinsop, TG, Hoehndorf, A (2002). «Precise U–Pb mineral ages, Rb–Sr and Sm–Nd systematics for the Great Dyke, Zimbabwe—constraints on late Archean events in the Zimbabwe craton and Limpopo belt». Precambrian Research 113 (3–4): 293-306. Bibcode:2002PreR..113..293O. doi:10.1016/S0301-9268(01)00215-7.
- ↑ White, W. M. (2003). «Basics of Radioactive Isotope Geochemistry». Cornell University.
- ↑ a b «Geologic Time: Radiometric Time Scale». United States Geological Survey. 16 June 2001.
- ↑ Salazar, Salvador Mosqueira Pérez (2000). Introducción a la Química y el ambiente. Grupo Editorial Patria. ISBN 9786077440659. Consultado el 19 de febrero de 2018.
- ↑ Stacey, J. S.; J. D. Kramers (June 1975). «Approximation of terrestrial lead isotope evolution by a two-stage model». Earth and Planetary Science Letters 26 (2): 207-221. Bibcode:1975E&PSL..26..207S. doi:10.1016/0012-821X(75)90088-6.
- ↑ Vinyu, M. L.; R. E. Hanson; M. W. Martin; S. A. Bowring; H. A. Jelsma; P. H. G. M. Dirks (2001). «U-Pb zircon ages from a craton-margin archaean orogenic belt in northern Zimbabwe». Journal of African Earth Sciences 32 (1): 103-114. Bibcode:2001JAfES..32..103V. doi:10.1016/S0899-5362(01)90021-1.
- ↑ Manyeruke, Tawanda D.; Thomas G. Blenkinsop; Peter Buchholz; David Love; Thomas Oberthür; Ulrich K. Vetter; Donald W. Davis (2004). «The age and petrology of the Chimbadzi Hill Intrusion, NW Zimbabwe: first evidence for early Paleoproterozoic magmatism in Zimbabwe». Journal of African Earth Sciences 40 (5): 281-292. Bibcode:2004JAfES..40..281M. doi:10.1016/j.jafrearsci.2004.12.003.
- ↑ Li, Xian-hua; Liang, Xi-rong; Sun, Min; Guan, Hong; Malpas, J. G. (2001). «Precise 206Pb/238U age determination on zircons by laser ablation microprobe-inductively coupled plasma-mass spectrometry using continuous linear ablation». Chemical Geology 175 (3–4): 209-219. Bibcode:2001ChGeo.175..209L. doi:10.1016/S0009-2541(00)00394-6.
- ↑ Wingate, M.T.D. (2001). «SHRIMP baddeleyite and zircon ages for an Umkondo dolerite sill, Nyanga Mountains, Eastern Zimbabwe». South African Journal of Geology 104 (1): 13-22. doi:10.2113/104.1.13.
- ↑ Ireland, Trevor (December 1999). «Isotope Geochemistry: New Tools for Isotopic Analysis». Science 286 (5448): 2289-2290. doi:10.1126/science.286.5448.2289.
- ↑ Mukasa, S. B.; A. H. Wilson; R. W. Carlson (December 1998). «A multielement geochronologic study of the Great Dyke, Zimbabwe: significance of the robust and reset ages». Earth and Planetary Science Letters 164 (1–2): 353-369. Bibcode:1998E&PSL.164..353M. doi:10.1016/S0012-821X(98)00228-3.
- ↑ «Ales stenar». The Swedish National Heritage Board. 11 October 2006. Archivado desde el original el 31 March 2009. Consultado el 9 March 2009. Parámetro desconocido
|df=ignorado (ayuda) - ↑ Clark, R. M. (1975). «A calibration curve for radiocarbon dates». Antiquity 49: 251-266.
- ↑ Vasiliev, S. S.; V. A. Dergachev (2002). «The ~2400-year cycle in atmospheric radiocarbon concentration: Bispectrum of 14C data over the last 8000 years». Annales Geophysicae 20 (1): 115-120. Bibcode:2002AnGeo..20..115V. doi:10.5194/angeo-20-115-2002.
- ↑ «Carbon-14 Dating». www.chem.uwec.edu. Consultado el 6 de abril de 2016.
- ↑ Plastino, Wolfango; Lauri Kaihola; Paolo Bartolomei; Francesco Bella (2001). «Cosmic background reduction in the radiocarbon measurement by scintillation spectrometry at the underground laboratory of Gran Sasso». Radiocarbon 43 (2A): 157-161.
- ↑ Jacobs, J.; R. J. Thomas (August 2001). «A titanite fission track profile across the southeastern Archæan Kaapvaal Craton and the Mesoproterozoic Natal Metamorphic Province, South Africa: evidence for differential cryptic Meso- to Neoproterozoic tectonism». Journal of African Earth Sciences 33 (2): 323-333. Bibcode:2001JAfES..33..323J. doi:10.1016/S0899-5362(01)80066-X.
- ↑ Application of the authigenic 10 Be/ 9 Be dating method to Late Miocene–Pliocene sequences in the northern Danube Basin;Michal Šujan &a; Global and Planetary Change 137 (2016) 35–53; pdf
- ↑ Imke de Pater and Jack J. Lissauer: Planetary Sciences, page 321. Cambridge University Press, 2001. ISBN 0-521-48219-4
- ↑ Gilmour, J. D.; O. V Pravdivtseva; A. Busfield; C. M. Hohenberg (2006). «The I-Xe Chronometer and the Early Solar System». Meteoritics and Planetary Science 41: 19-31. Bibcode:2006M&PS...41...19G. doi:10.1111/j.1945-5100.2006.tb00190.x. Consultado el 21 de enero de 2013.
- ↑ Alexander N. Krot(2002) Dating the Earliest Solids in our Solar System, Hawai'i Institute of Geophysics and Planetology http://www.psrd.hawaii.edu/Sept02/isotopicAges.html.
- ↑ Imke de Pater and Jack J. Lissauer: Planetary Sciences, page 322. Cambridge University Press, 2001. ISBN 0-521-48219-4
Referencias
- Esta obra contiene una traducción derivada de «Radiometric dating» de Wikipedia en inglés, publicada por sus editores bajo la Licencia de documentación libre de GNU y la Licencia Creative Commons Atribución-CompartirIgual 4.0 Internacional.
Bibliografía
- Gunten, Hans R. von (1995). «Radioactivity: A Tool to Explore the Past». Radiochimica Acta. 70-71 (s1). ISSN 2193-3405. doi:10.1524/ract.1995.7071.special-issue.305.
- Magill, Joseph; Galy, Jean (2005). «Archaeology and Dating». Radioactivity Radionuclides Radiation. Springer Berlin Heidelberg. pp. 105-115. ISBN 978-3-540-26881-9. doi:10.1007/3-540-26881-2_6.
- Allègre, Claude J (4 de diciembre de 2008). Isotope Geology. ISBN 978-0521862288.
- McSween, Harry Y; Richardson, Steven Mcafee; Uhle, Maria E; Uhle, Professor Maria (2003). Geochemistry: Pathways and Processes (2 edición). ISBN 978-0-231-12440-9.
- Harry y. Mcsween, Jr; Huss, Gary R (29 de abril de 2010). Cosmochemistry. ISBN 978-0-521-87862-3.











