Leyes de Fick
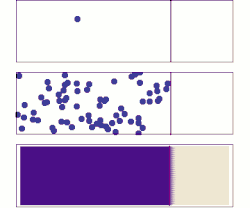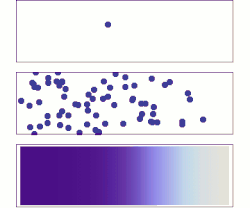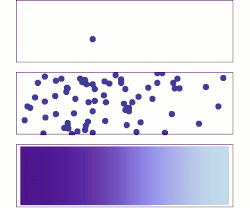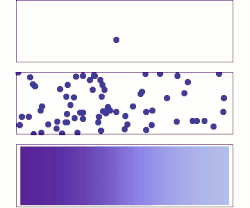
Las leyes de Fick sobre la difusión son leyes cuantitativas, escritas en forma de ecuación diferencial que describen matemáticamente al proceso de difusión (física) de materia o energía en un medio en el que inicialmente no existe equilibrio químico o térmico. Estas leyes pueden ser utilizadas para resolver el coeficiente de difusión, D. Se puede utilizar la primera ley de Fick para derivar la segunda ley, la cual resulta idéntica a la ecuación de difusión.
En situaciones en las que existen gradientes de concentración de una sustancia, o de temperatura, se produce un flujo de partículas o de calor que tiende a homogeneizar la disolución y uniformar la concentración o la temperatura. El flujo homogeneizador es una consecuencia estadística del movimiento aleatorio de las partículas que da lugar al segundo principio de la termodinámica, conocido también como movimiento térmico aleatorio de las partículas. Así los procesos físicos de difusión pueden ser vistos como procesos físicos o termodinámicos irreversibles.
Etimología[editar]
Reciben su nombre del médico y fisiólogo alemán Adolf Fick (1829-1901), que las derivó en 1855.
Historia[editar]
En el año 1855, el fisiólogo Adolf Fick reporta por primera vez sus ahora muy bien conocidas leyes que gobiernan el transporte de masas por un medio difusivo.[1][2] El trabajo de Fick fue inspirado por anteriores experimentos de Thomas Graham, los cuales estuvieron muy cerca de proponer las leyes fundamentales por las cuales Fick se hizo famoso. Las leyes de Fick son análogas a las relaciones descubiertas aproximadamente en la misma época por otros eminentes científicos: ley de Darcy (flujo hidráulico), ley de Ohm (transporte de carga), y ley de Fourier (transporte de calor).
Los experimentos de Fick (modelados por Graham) lidian con la medición de concentraciones y flujos de sal, difundiendo entre dos reservorios a través de tubos de agua. Es notable que el trabajo de Fick se ocupa primariamente de la difusión de fluidos, porque en ese tiempo, la difusión en sólidos, en general, no se consideraba posible.[3] Al día de hoy las leyes de Fick forman el núcleo de nuestro entendimiento de la difusión en sólidos, líquidos y gases (en ausencia de movimientos masivos de fluido en los últimos casos). Cuando el proceso de difusión no sigue las leyes de Fick (lo que suele suceder),[4][5] se denomina no Fickiano, en estos hay excepciones que "demuestran" la importancia de las reglas generales que delineó Fick en 1855.
Simbología[editar]
| Símbolo | Nombre | Unidad |
|---|---|---|
| Flujo difusivo | mol / (m2 s) | |
| Vector de flujo difusivo | ||
| Concentración (para mezclas ideales) | mol / m3 | |
| Constantes | ||
| Concentración | mol / m3 | |
| Coeficiente de difusión (Difusividad) | m2 / s | |
| Constante universal de los gases | J / (mol K) | |
| Temperatura absoluta | K | |
| Potencial químico | J / mol | |
| Densidad del fluido | kg / m3 | |
| Variables | ||
| Tiempo | s | |
| Posición | m | |
| Dependen de | ||
| i-ésima especie | ||
| Concentración | mol / m3 | |
| Flujo difusivo | mol / (m2 s) | |
| Masa molar | kg / mol | |
| Fracción de masa | kg / kg | |
| Potencial químico | J / mol |
Primera ley de Fick[editar]
La primera ley de Fick relaciona al flujo difusivo con la concentración bajo la asunción de un estado estacionario. Esta ley postula que el flujo va desde una región de alta concentración a las regiones de baja concentración, con una magnitud que es proporcional al gradiente de concentración (derivada espacial), o en términos más simples el concepto de que el soluto se moverá desde una región de alta concentración a una de baja concentración atravesando un gradiente de concentración. En una única dimensión (espacial), la ley toma la forma:
() es proporcional a la velocidad de difusión al cuadrado de las partículas que están difundiendo, la cual depende de la temperatura, viscosidad del fluido y del tamaño de las partículas de acuerdo a la relación de Einstein-Stokes. En soluciones acuosas diluidas los coeficientes de difusión de diferentes iones son similares y tienen valores a temperatura ambiente que van desde los (0,6 x 10−9) a los (2 x 10−9) m2 / s. Para moléculas biológicas los coeficientes de difusión normalmente van entre los (10−11) y los (10−10) m2 / s.
Para dos o más dimensiones espaciales, podemos hacer uso del operador (), (nabla o gradiente), lo cual generaliza la primera derivada, obteniéndose:
La fuerza impulsora para la difusión unidimensional es la cantidad
que para mezclas ideales es el gradiente de concentración. En sistemas químicos diferentes a soluciones ideales, la fuerza impulsora para la difusión de cada especie es el gradiente de potencial químico de estas especies. En estos casos la primera ley de Fick (para una dimensión) puede ser reescrita como:
| Potencial químico | Haciendo | 1° Ley de Fick | |
|---|---|---|---|
| Ecuaciones | |||
| Derivando | |||
| Simplificando | |||
| Sustituyendo | |||
| Despejando | |||
| Sustituyendo | |||
Si la variable primaria es la fracción de masa (), dada, por ejemplo, en (kg / kg), entonces la ecuación toma la forma:
| 1° Ley de Fick | 2 | Potencial químico | |
|---|---|---|---|
| Ecuaciones | |||
| Despejando | |||
| Derivando | |||
| Simplificando | |||
| Sustituyendo | |||
| Simplificando | |||
Nótese que la densidad se encuentra fuera del operador gradiente.
Segunda ley de Fick[editar]
La segunda ley de Fick predice la forma en que la difusión causa que la concentración cambie con el tiempo. Se trata de una ecuación diferencial parcial que en una dimensión se escribe:
En dos o más dimensiones debemos usar el Laplaciano (), que generaliza la segunda derivada, obteniéndose la ecuación
Solución de ejemplo en una dimensión: longitud de difusión[editar]
Un caso simple de difusión a tiempo () en una dimensión (tomada como el eje ()) a partir de una frontera localizada en la posición (), donde la concentración se mantiene a un valor () es
| Símbolo | Nombre |
|---|---|
| Función error complementario |
Este es el caso que se presenta cuando los gases corrosivos difunden atravesando la capa oxidativa hacia la superficie del metal (esto si asumimos que la concentración de los gases en ese medio es constante y el espacio de difusión —p. ej. la capa de producto de corrosión— es semiinfinita, comenzando en 0 en la superficie y expandiéndose infinitamente en profundidad en el material). Si, a su vez, el espacio de difusión es infinito (permaneciendo a través de la capa con () y a través de aquella con (), entonces la solución se corrige sólo con un coeficiente ½ por delante de () (esto podría parecer obvio, ya que la difusión ahora ocurre en dos direcciones). Este caso es válido cuando algunas soluciones con concentración () son puestas en contacto con una capa de solvente puro (Bokstein, 2005). La longitud () se denomina longitud de difusión y provee una medida de cuan lejos la concentración se propaga en la dirección () por difusión a un tiempo () (Bird, 1976).
Como una aproximación rápida a la función error, se pueden utilizar los dos primeros términos de la serie de Taylor:
si es dependiente del tiempo, la longitud de difusión se transforma en . Esta idea es útil para estimar la longitud de difusión sobre un ciclo de calentamiento-enfriamiento, donde () varía con la temperatura.
Generalizaciones[editar]
1. En los medios no homogéneos, el coeficiente de difusión varía en espacio, (). Esta dependencia no afecta a la primera ley de Fick, pero la segunda ley cambia:
2. En los medios anisotrópicos, el coeficiente de difusión depende de la dirección. Es un tensor simétrico (). La primera ley de Fick cambia a
Para la ecuación de difusión esta fórmula da
La matriz simétrica de los coeficientes de difusión () debería ser positiva y definida. Es necesario hacer que el operador situado a mano derecha sea elíptico.
3. Para los medios anisotrópicos no homogéneos se pueden combinar estas dos formas de la ecuación de difusión para obtener:
4. El enfoque basado en la fórmula de la movilidad de Einstein y Teorell lleva a la siguiente generalización de la ecuación de Fick para la difusión multicomponente de componentes perfectos:
donde () son las concentraciones de los componentes, y () es la matriz de coeficientes. Aquí, los índices () se encuentran relacionados con cada uno de los diversos componentes, y no a las coordenadas espaciales.
Las fórmulas de Chapman-Enskog para la difusión en gases, incluyen exactamente los mismos términos. Cabe destacar que estos modelos físicos de difusión son diferentes de los "modelos de juguete" () que son válidos para desviaciones muy pequeñas del equilibrio uniforme. Estos términos fueron incluidos tempranamente en la ecuación de difusión de Maxwell-Stefan.
Para coeficientes de difusión anisotrópicos multicomponentes hace falta un tensor de rango cuatro, por ejemplo (), donde () se refieren a los componentes y () corresponden a las coordenadas espaciales.
Aplicaciones[editar]
Se han utilizado con frecuencia ecuaciones derivadas de las leyes de Fick para modelar procesos de transporte pasivo en alimentos, neuronas, biopolímeros, productos farmacéuticos, poros, suelos, dinámica de poblaciones, materiales nucleares, procesos de dopado de semiconductores, etc. La teoría de todos los métodos voltametricos se encuentra basada en las soluciones a las ecuaciones de Fick. Una gran cantidad de investigación experimental en ciencia de polímeros y alimentos ha mostrado que se requiere un enfoque más general para describir el transporte de componentes en materiales que experimentan una transición vítrea. En las proximidades de una transición vítrea el comportamiento del flujo se convierte en no Fickeano. Se puede demostrar que las leyes de Fick pueden obtenerse de las ecuaciones de Maxwell-Stefan[6] para transferencia de masa multicomponente. La ley de Fick es un caso límite de las ecuaciones de Maxwell-Stefan, donde la mezcla se encuentra extremadamente diulida y cada especie química se encuentra actuando únicamente con el total de la mezcla y no con otras especies. Para tomar cuenta de la presencia de múltiples especies en mezclas no diluidas se haceuso de variaciones de las ecuaciones de Maxwell-Stefan. Puede verse también procesos de transporte acoplado no diagonales (relaciones de Onsanger).
Perspectiva biológica[editar]
La primera ley conduce a la siguiente fórmula:[7]
| Símbolo | Nombre |
|---|---|
| Permeabilidad, una conductancia de membrana determinada experimentalmente para un determinado gas a una determinada temperatura | |
| Diferencia en la concentración del gas a través de una membrana artificial para la dirección de flujo (desde a ) |
La primera ley de Fick también es importante para las ecuaciones de transferencia de radiación. Sin embargo, en este contexto se vuelve inexacta cuando la constante de difusión es baja y la radiación se encuentra limitada por la velocidad de la luz, antes que por la resistencia del material a través del cual la radiación se está propagando. En esta situación, se puede hacer uso de un limitador de flujo.
La tasa de intercambio de un gas a través de una membrana de fluido puede determinarese utilizando esta ley en conjunción con la ley de Graham.
Flujo de Fick en líquidos[editar]
Cuando dos líquidos miscibles se ponen en contacto, y ocurre la difusión, la concentración macroscópica o promedio evoluciona siguiendo la ley de Fick. A escala mesoscópica, esto es, entre la escala macroscópica descrita por la ley de Fick y la escala molecular, donde toma lugar el paseo aleatorio de las moléculas, las fluctuaciones no pueden ser menospreciadas. Tales situaciones pueden ser exitosamente modeladas por medio de las fluctuaciones hidrodinámicas de Landau-Lifshitz. En este marco teórico, la difusión es debida a fluctuaciones cuyas dimensiones van desde la escala molecular a la macroscópica.[8]
En particular, las ecuaciones de hidrodinámica fluctuante incluyen el término de flujo de Fick, con un coeficiente de difusión, junto con ecuaciones hidrodinámicas y términos estocásticos que describen las fluctuaciones.
Al calcular las fluctuaciones con un enfoque perturbativo, la aproximación de orden cero es la ley de Fick. El primer orden añade las variaciones, y salen de como las fluctuaciones contribuyen a la difusión.
Esto representa en cierta forma una tautología, ya que el fenómeno descrito por una aproximación de bajo orden es el resultado de una aproximación mayor: este problema se resuelve únicamente renormalizando las ecuaciones de hidrodinámica fluctuante.
Aplicaciones en la fabricación de semiconductores[editar]
Las tecnologías de fabricación de circuitos integrados, procesos de modelados tales como el CVD, oxidación térmica, dopado, etc. hacen uso de las ecuaciones de difusión obtenidas de las leyes de Fick.
En ciertos casos, las soluciones se obtienen para las condiciones de contorno tales como una fuente de difusión de concentración, una fuente limitada de concentración, o difusión de contorno móvil (donde la profundidad de unión se mantiene en movimiento dentro del sustrato).
Derivación de las leyes de Fick[editar]
Primera ley de Fick[editar]
Para una dimensión, la siguiente derivación se encuentra basada en un argumento similar desarrollado en Berg 1977 (ver las referencias).
Considérese una colección de partículas desarrollando un paseo aleatorio en una dimensión con escala de longitud () y escala de tiempo (). Sea () el número de partículas en la posición () a tiempo ().
A un tiempo dado, la mitad de las partículas podrían moverse a la derecha y la mitad podrían hacerlo hacia la izquierda. Ya que la mitad de las partículas en el punto () se mueven hacia la derecha y la mitad de las partículas en el punto () lo hacen hacia la izquierda, el siguiente movimiento hacia la derecha está dado por:
El flujo (), es el movimiento de las partículas a través de determinado elemento de área, o área (), normal al paseo aleatorio durante el intervalo de tiempo (). De esta forma podríamos escribir:
| 1 | 2 | General | |
|---|---|---|---|
| Ecuaciones | |||
| Multiplicando | |||
| Ordenando | |||
| Sustituyendo | |||
| Aplicando límite | |||
| Definición de derivada | |||
Segunda ley de Fick[editar]
La segunda ley de Fick puede ser derivada de la primera ley de Fick y de la ley de conservación de masa (véase Ecuación de continuidad) en ausencia de cualquier reacción química:
| Conservación | 1° Fick | |
|---|---|---|
| Ecuaciones | ||
| Sustituyendo | ||
| Despejando | ||
| Ordenando | ||
| Simplificando | ||
y, entonces, recibir la forma de las ecuaciones de Fick como se desarrolló anteriormente.
Para el caso de difusión en dos o más dimensiones, la segunda ley de Fick se transforma en
la cual es análoga a la ecuación del calor.
Si el coeficiente de difusión no es constante, sino que depende de las coordenadas y/o de la concentración, la segunda ley de Fick conduce a
Un importante ejemplo es el caso donde es el estado estacionario, p. ej. la concentración no cambia en el tiempo, de forma tal que el miembro izquierdo de la ecuación de más arriba es idéntica a cero. En una dimensión con constante, la solución para la concentración puede ser una variación lineal de concentración sobre . En dos o más dimensiones obtenemos
La cual es la ecuación de Laplace, de la cual sus soluciones suelen ser referidas por los matemáticos como funciones armónicas.
Véase también[editar]
- Difusión
- Ósmosis
- Flujo de masa
- Difusión de Maxwell-Stefan
- Ecuación de Churchill-Bernstein
- Ecuación de Nernst-Planck
- Intercambio gaseoso
- Falsa difusión
- Ecuación de Mansen-Dumbre
Referencias[editar]
- ↑ A. Fick, Ann. der. Physik (1855), 94, 59, doi 10.1002/andp.18551700105 (in German).
- ↑ A. Fick, Phil. Mag. (1855), 10, 30. (in English)
- ↑ Jean Philibert, One and a Half Century of Diffusion: Fick, Einstein, before and beyond, Diffusion Fundamentals 2, 2005 1.1–1.10 Archivado el 5 de febrero de 2009 en Wayback Machine.
- ↑ J. L. Vázquez (2006), The Porous Medium Equation. Mathematical Theory, Oxford Univ. Press.
- ↑ A.N. Gorban, H.P. Sargsyan and H.A. Wahab (2011), Quasichemical Models of Multicomponent Nonlinear Diffusion, Mathematical Modelling of Natural Phenomena, Volume 6 / Issue 05, 184−262.
- ↑ Taylor, Ross; R Krishna (1993). Multicomponent mass transfer. Wiley.
- ↑ Physiology: 3/3ch9/s3ch9_2 - Essentials of Human Physiology
- ↑ D. Brogioli and A. Vailati, Diffusive mass transfer by nonequilibrium fluctuations: Fick's law revisited, Phys. Rev. E 63, 012105/1-4 (2001) [1]
Bibliografía[editar]
- W.F. Smith, Foundations of Materials Science and Engineering 3rd ed., McGraw-Hill (2004)
- H.C. Berg, Random Walks in Biology, Princeton (1977)
- R.B. Bird, W.E. Stewart, E.N. Lightfoot, Transport Phenomena, John Wiley & sons, (1976)
- J. Crank, The Mathematics of Diffusion, Oxford University Press (1980)
- Thermodynamics and Kinetics in Materials Science: A Short Course. Bokshtein, B. S. Mendelev, M. I. Srolovitz, D. J. Eds. Oxford University Press: Oxford (2005) – pp. 167–171.
- A. Fick, On liquid diffusion, Poggendorffs Annalen. 94, 59 (1855) - reprinted in Journal of Membrane Science, vol. 100 pp. 33–38 (1995)



















































![{\displaystyle n(x,t)=n_{0}\left[1-2\left({\frac {x}{2{\sqrt {\pi \ D\ t}}}}\right)\right]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/8eb91a037ad7deaa2f03091ca1b3097d0bf9e687)
























![{\displaystyle -{\frac {1}{2}}\left[N(x+\Delta x,t)-N(x,t)\right]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/113fa477425cea34b18a53514dcf2bcda78de508)

![{\displaystyle J=-{\frac {1}{2}}\left[{\frac {N(x+\Delta x,t)}{a\ \Delta t}}-{\frac {N(x,t)}{a\ \Delta t}}\right]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/a88f3ad447685b792c39079814c86cf99f8e847e)



![{\displaystyle J=-{\frac {1}{2}}\left[{\frac {N(x+\Delta x,t)}{a\ \Delta t}}-{\frac {N(x,t)}{a\ \Delta t}}\right]{\Bigl (}{\frac {\Delta x}{\Delta x}}{\Bigr )}^{2}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/f6c42d92c42958da1dfa0bf34e5a437b10909547)
![{\displaystyle J=-{\frac {(\Delta x)^{2}}{2\ \Delta t}}\left[{\frac {N(x+\Delta x,t)}{a\ \Delta x\ \Delta x}}-{\frac {N(x,t)}{a\ \Delta x\ \Delta x}}\right]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/90d909edfb95ee6d5e6249f45cef820ee7415cb7)
![{\displaystyle J=-D\left[{\frac {\phi (x+\Delta x,t)}{\Delta x}}-{\frac {\phi (x,t)}{\Delta x}}\right]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/a5741b84940c245fcbe923e5849675001c46d17d)

![{\displaystyle J=-D\lim _{\Delta x\to 0}\left[{\frac {\phi (x+\Delta x,t)-\phi (x,t)}{\Delta x}}\right]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/9ec8b9cfa2a149c5501da159d8c3e8e60e0ab67a)









