Ciclooctatetraeno
| Ciclooctatetraeno | ||
|---|---|---|
 | ||
 | ||
| Nombre IUPAC | ||
| Cicloocta-1,3,5,7-tetraeno | ||
| General | ||
| Otros nombres |
1,3,5,7-ciclooctatetraeno [8]-anuleno | |
| Símbolo químico | COT | |
| Fórmula estructural |
 | |
| Fórmula molecular | C8H8 | |
| Identificadores | ||
| Número CAS | 629-20-9[1] | |
| ChemSpider | 553448 | |
| Propiedades físicas | ||
| Apariencia | incoloro-amarillo pálido | |
| Densidad | 925 kg/m³; 0,925 g/cm³ | |
| Masa molar | 10 415 g/mol | |
| Punto de fusión | 269 K (−4 °C) | |
| Punto de ebullición | 416 K (143 °C) | |
| Índice de refracción (nD) | 1,537 | |
| Compuestos relacionados | ||
| Ciclooctadieno | 1,5-ciclooctadieno (COD) | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
El ciclooctatetraeno o COT es un derivado insaturado del ciclooctano, con la fórmula molecular C8H8. También se conoce como [8]-anuleno. Este hidrocarburo poliinsaturado es un líquido incoloro tirando a amarillo claro inflamable a temperatura ambiente. Debido a que la relación entre los átomos de carbono e hidrógeno (1:1) es la del benceno, el COT ha sido objeto de mucha investigación y una cierta controversia.
A diferencia del benceno, C6H6, el ciclooctatetraeno, C8H8, no es aromático, aunque su dianión, C8H82- (ciclooctatetradienuro) sí lo es, puesto que con 10 electrones, cumple con la regla de Hückel. Su reactividad es la característica de un polieno ordinario, es decir, sobre todo se somete a reacciones de adición.
Historia[editar]
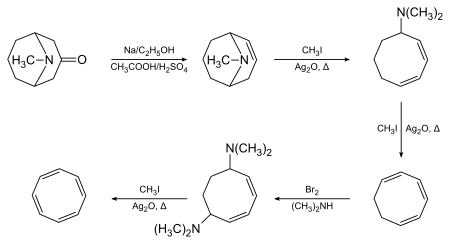
El 1,3,5,7-ciclooctatetraeno fue sintetizado inicialmente por Richard Willstätter en Múnich en 1905:[2][3]
Willstätter se dio cuenta de que el compuesto no exhibía la aromaticidad esperada. Entre 1939 y 1943 , los químicos a lo largo de los EE. UU. , sin éxito, intentaron sintetizar COT . Pensaron que su falta de éxito era en realidad porque Willstätter no había sintetizado el COT, sino que su isómero , el estireno. Willstätter respondió a estas críticas en su autobiografía, en la que señaló que los químicos estadounidenses estaban reduciendo "sin problemas" el ciclooctatetraeno a ciclooctano (una reacción imposible para el estireno). Durante la Segunda Guerra Mundial, Walter Reppe en BASF desarrolló de manera sencilla, con la síntesis en una sola etapa del ciclooctatetraeno a partir de acetileno, el suministro de material idéntico al preparado por Willstätter:[4]
Cualquier duda que quedara sobre la exactitud de síntesis original de Willstätter se resolvió cuando Arthur C. Cope (y compañeros de trabajo en el MIT) informó, en 1947, una repetición completa de la síntesis de Willstätter, paso a paso, utilizando las técnicas reportadas originalmente. Obtuvieron el mismo ciclooctatetraeno,[5] y además llevaron a cabo la caracterización de muchos de los productos intermedios por métodos espectroscópicos, volviendo a confirmar la exactitud de la obra original de Willstätter.[6]
Otra síntesis comienza a partir del cubano. Con la presencia de catalizadores de rodio, se forma primero el triciclooctadieno SYN, que se puede convertir térmicamente a ciclooctatetraeno a una temperatura entre 50-60 °C:

Estructura y enlace[editar]

Los primeros estudios demostraron que el COT no es un compuesto aromático.[7] Entonces, los primeros experimentos de difracción de electrones llegaron a la conclusión de que las distancias de enlace C-C eran idénticas.[8] Sin embargo, los datos de difracción de rayos X de SA Kaufman demostraron que el ciclooctatetraeno podía adoptar varias conformaciones y eso justificaba obtener dos distancias de enlace C-C distintas.[9] Este resultado indicó que el COT es un anuleno con enlaces C-C simples y dobles alternados.
En su estado normal, el ciclooctatetraeno no es plano y adopta una conformación de tipo bañera con ángulos C=C-C=126,1° y C=C-H=117,6°.[10]
Síntesis[editar]
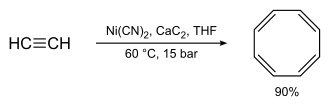
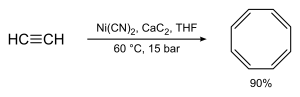
La síntesis de Reppe del ciclooctatetraeno implica el tratamiento de acetileno a alta presión con una mezcla caliente de cianuro de níquel y carburo de calcio, con rendimientos químicos cerca del 90% es mucho mejor que la síntesis de Willstätter comentada anteriormente:[4]
El COT también se pueden preparar por fotólisis del barrileno, uno de sus isómeros estructurales. Esta reacción de proceder a través de otro isómero aislable, el semibullvaleno.[11] También puede sintetizarse derivados de COT por medio de intermedios semibullvaleno. En la secuencia ilustrada debajo, el octaetilciclooctatetraeno (C8Et8) se forma por isomerización térmica del octaetilsemibullvaleno, que ha sido formado previamente por ciclodimerización del 1,2,3,4-tetraetil-1,4-dilitio-1,3-butadieno mediada por bromuro de cobre (I).[12]
Debido a que el COT es inestable y fácilmente forma peróxidos orgánicos explosivos, una pequeña cantidad de hidroquinona se añade generalmente al reactivo disponible comercialmente. Se recomienda por precaución hacer un test de peróxidos antes de usar una botella abierta anteriormente. Puede haber cristales de color blanco alrededor del cuello de la botella compuestos por peróxidos, que pueden explotar por perturbación mecánica.
Anión ciclooctatetraenuro[editar]


El COT reacciona fácilmente con el potasio metálico para formar la sal K2COT, que contiene el dianión C8H82−.[13] El dianión es plano y octogonal, con un recuento de electrones de 10, por lo que al cumplir con la regla de Hückel es además aromático.
Tanto el COT como el COD son ligandos típicos en química organometálica. El primero es un ligando de 10 electrones como ya hemos comentado y el segundo un ligando de 4 electrones. El recuento de electrones en importante, puesto que los compuestos organometálicos suelen cumplir la regla de los 18 electrones. Los compuestos sándwich como el U(COT)2 (mal llamado uranoceno) y el Fe(COT)2 son bastante conocidos.
Referencias[editar]
- ↑ Número CAS
- ↑ Mason, S. "The Science and Humanism of Linus Pauling (1901-1994)", Chemical Society Reviews 26, 1 (February 1997).
- ↑ Richard Willstätter, Ernst Waser (1911). «Über Cyclo-octatetraen». Berichte der deutschen chemischen Gesellschaft 44 (3): 3423-3445. doi:10.1002/cber.191104403216.
- ↑ a b Walter Reppe, Otto Schlichting, Karl Klager, Tim Toepel (1948). «Cyclisierende Polymerisation von Acetylen I Über Cyclooctatetraen». Justus Liebigs Annalen der Chemie 560 (1): 1-92. doi:10.1002/jlac.19485600102.
- ↑ Arthur C. Cope, C. G. Overberger (1947). «The synthesis of cycloöctatetraene from pseudopelletierine». Journal of the American Chemical Society 69 (4): 976. doi:10.1021/ja01196a513.
- ↑ Arthur C. Cope, C. G. Overberger (1947). «Cyclic Polyolefins. I. Synthesis of Cycloöctatetraene from Pseudopelletierine». Journal of the American Chemical Society 70 (4): 1433-1437. doi:10.1021/ja01184a041.
- ↑ Johnson, A.W., Sci. Progress; 506; 1947; 35.
- ↑ Bastiensen, O.; Hassel, O.; Langseth, A. (1947). «The ‘Octa-Benzene’, Cyclo-octatetraene (C8H8)». Nature 160 (4056): 128. Bibcode:1947Natur.160..128B. doi:10.1038/160128a0.
- ↑ Kaufman, H. S.; Fankuchen, I.; Mark, H. (1948). «Structure of Cyclo-octatetraene». Nature 161 (4083): 165. Bibcode:1948Natur.161..165K. doi:10.1038/161165a0.
- ↑ Thomas, P. M.; Weber, A. (1978). «High resolution Raman spectroscopy of gases with laser sources. XIII - the pure rotational spectra of 1,3,5,7-cyclooctatetraene and 1,5-cyclooctadiene». Journal of Raman Spectroscopy 7 (6): 353-357. Bibcode:1978JRSp....7..353T. doi:10.1002/jrs.1250070614.
- ↑ Zimmerman, H. E.; Grunewald, G. L. (1966). «The Chemistry of Barrelene. III. A Unique Photoisomerization to Semibullvalene». J. Am. Chem. Soc. 88 (1): 183-184. doi:10.1021/ja00953a045.
- ↑ Wang, C.; Yuan, J.; Li, G.; Wang, Z.; Zhang, S.; Xi, Z. (2006). «Metal-Mediated Efficient Synthesis, Structural Characterization, and Skeletal Rearrangement of Octasubstituted Semibullvalenes». J. Am. Chem. Soc. 128 (14): 4564-4565. PMID 16594680. doi:10.1021/ja0579208.
- ↑ The cyclooctatetraenyl dianion Thomas J. Katz J. Am. Chem. Soc.; 1960; 82(14); 3784-3785. doi 10.1021/ja01499a077