Diferencia entre revisiones de «Bismuto»
Sin resumen de edición |
|||
| Línea 244: | Línea 244: | ||
[[zh:铋]] |
[[zh:铋]] |
||
[[zh-yue:鉍]] |
[[zh-yue:鉍]] |
||
{{{gayys}}} |
|||
Revisión del 18:00 21 sep 2010
| |||||||||||||||||||||||||
| General | |||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
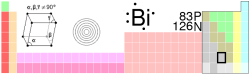
| Nombre, símbolo, número | Bismuto, Bi, 83 | ||||||||||||||||||||||||
| Serie química | Metales del bloque p | ||||||||||||||||||||||||
| Grupo, periodo, bloque | 15, 6, p | ||||||||||||||||||||||||
| Densidad, dureza Mohs | 9780 kg/m3, 2,25 | ||||||||||||||||||||||||
| Apariencia | Rojo, blanco brillante
| ||||||||||||||||||||||||
| Propiedades atómicas | |||||||||||||||||||||||||
| Masa atómica | 208,98038 u | ||||||||||||||||||||||||
| Radio medio† | 160 pm | ||||||||||||||||||||||||
| Radio atómico calculado | 143 pm | ||||||||||||||||||||||||
| Radio covalente | 146 pm | ||||||||||||||||||||||||
| Radio de Van der Waals | sin datos | ||||||||||||||||||||||||
| Configuración electrónica | [Xe]4f14 5d10 6s2 6p3 | ||||||||||||||||||||||||
| Estados de oxidación (óxido) | 3, 5 (levemente ácido) | ||||||||||||||||||||||||
| Estructura cristalina | Romboédrica | ||||||||||||||||||||||||
| Propiedades físicas | |||||||||||||||||||||||||
| Estado de la materia | Sólido | ||||||||||||||||||||||||
| Punto de fusión | 544,4 K (271,4°C) | ||||||||||||||||||||||||
| Punto de ebullición | 1837 K (1564°C) | ||||||||||||||||||||||||
| Entalpía de vaporización | 104,8 kJ/mol | ||||||||||||||||||||||||
| Entalpía de fusión | 11,3 kJ/mol | ||||||||||||||||||||||||
| Presión de vapor | 0,000627 Pa a 544 K | ||||||||||||||||||||||||
| Velocidad del sonido | 1790 m/s a 293,15 K | ||||||||||||||||||||||||
| Información diversa | |||||||||||||||||||||||||
| Electronegatividad | 2,02 (Pauling) | ||||||||||||||||||||||||
| Calor específico | 122 J/(kg·K) | ||||||||||||||||||||||||
| Conductividad eléctrica | 0,867 106 m-1·Ω-1 | ||||||||||||||||||||||||
| Conductividad térmica | 7,87 W/(m·K) | ||||||||||||||||||||||||
| 1er potencial de ionización | 703 kJ/mol | ||||||||||||||||||||||||
| 2° potencial de ionización | 1610 kJ/mol | ||||||||||||||||||||||||
| 3er potencial de ionización | 2466 kJ/mol | ||||||||||||||||||||||||
| 4° potencial de ionización | 4370 kJ/mol | ||||||||||||||||||||||||
| 5° potencial de ionización | 5400 kJ/mol | ||||||||||||||||||||||||
| 6° potencial de ionización | 8520 kJ/mol | ||||||||||||||||||||||||
| Isótopos más estables | |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| Plantilla:Cnpt | |||||||||||||||||||||||||
El bismuto es un elemento químico de la tabla periódica cuyo símbolo es Bi y su número atómico es 83.
Este metal del bloque p, pesado, quebradizo y blanco cristalino, se parece químicamente a los elementos que le preceden en el grupo, antimonio y arsénico (aunque estos se suelen considerar como semimetales). Se obtiene como subproducto del refinado de cobre (Cu), plomo (Pb) y estaño (Sn). Es el metal con mayor diamagnetismo y, después del mercurio, es el metal con menor conductividad térmica.
Se emplea en algunas aleaciones y algunos de sus compuestos se emplean como cosméticos y en aplicaciones farmacéuticas. Debido a la alta toxicidad del plomo, el uso de aleaciones con bismuto como reemplazo del plomo ha hecho que este elemento tenga una creciente importancia comercial.
Características del bismuto

Cuando es sólido flota sobre su estado líquido, por tener menor densidad en el estado sólido. Esta característica es compartida con el agua, el galio, el ácido acético, el antimonio y el silicio.
Enlaces externos
 Wikimedia Commons alberga una categoría multimedia sobre bismuto.
Wikimedia Commons alberga una categoría multimedia sobre bismuto.- WebElements.com - Bismuth
- EnvironmentalChemistry.com - Bismuth
- Bismuth breaks half-life record for alpha decay
{{{gayys}}}