Teoría ácido-base de Lewis
| Ácidos y Bases | |
|---|---|

| |
| Ácidos y Bases | |
| |
| Tipos de ácidos | |
| Tipos de bases | |

Un ácido de Lewis es una especie química que contiene un orbital vacío que es capaz de aceptar un par de electrones de una base de Lewis para formar un aducto de Lewis. Una base de Lewis, entonces, es cualquier especie que tiene un orbital lleno que contiene un par de electrones que no está involucrado en un enlace, pero que puede formar un enlace dativo con un ácido de Lewis para formar un aducto de Lewis. Por ejemplo, el NH3 es una base de Lewis, porque puede donar su único par de electrones libres. El trimetilborano (Me3B) es un ácido de Lewis, ya que es capaz de aceptar un par solitario. En un aducto de Lewis, el ácido y la base de Lewis comparten un par de electrones proporcionado por la base de Lewis, formando un enlace dativo.[1] En el contexto de una reacción química específica entre NH3 y Me3B, el par solitario de NH3 formará un enlace dativo con el orbital vacío de Me 3 B para formar un aducto NH3 • BMe3. La terminología se refiere a las contribuciones de Gilbert N. Lewis.[2]
Los términos nucleófilo y electrófilo son más o menos intercambiables con base de Lewis y ácido de Lewis, respectivamente. Sin embargo, estos términos, especialmente sus formas sustantivas abstractas, nucleofilia y electrofilia, enfatizan el aspecto cinético de la reactividad, mientras que la basicidad de Lewis y la acidez de Lewis enfatizan el aspecto termodinámico de la formación de aductos de Lewis.[3]
Representando aductos[editar]
En muchos casos, la interacción entre la base de Lewis y el ácido de Lewis en un complejo se indica con una flecha que indica la base de Lewis que dona electrones hacia el ácido de Lewis utilizando la notación de un enlace dativo, por ejemplo, Me3B ← NH3. Algunas fuentes indican la base de Lewis con un par de puntos (los electrones explícitos que se donan), lo que permite una representación coherente de la transición de la propia base al complejo con el ácido:
- Me3B + :NH3 → Me3B:NH3
También se puede usar un punto central para representar un aducto de Lewis, como Me3B • NH3. Otro ejemplo es el dietil eterato de trifluoruro de boro, BF3 • Et2O. (En un uso ligeramente diferente, el punto central también se usa para representar la coordinación de hidratos en varios cristales, como en MgSO4 • 7H2O para sulfato de magnesio hidratado, independientemente de si el agua forma un enlace dativo con el metal.)
Aunque ha habido intentos de utilizar criterios energéticos computacionales y experimentales para distinguir el enlace dativo de los enlaces covalentes no dativos,[4] en su mayor parte, la distinción simplemente toma nota de la fuente del par de electrones y los enlaces dativos, una vez formados, se comportan simplemente como lo hacen otros enlaces covalentes, aunque normalmente tienen un carácter polar considerable. Además, en algunos casos (por ejemplo, sulfóxidos y óxidos de amina como R2S → O y R3N → O), el uso de la flecha de enlace dativo es solo una conveniencia de notación para evitar el dibujo de cargas formales. En general, sin embargo, el enlace donante-aceptor se considera simplemente en algún lugar de un continuo entre el enlace covalente idealizado y el enlace iónico.[5]
Ácidos de Lewis[editar]
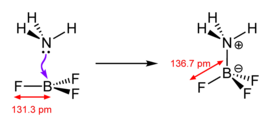
Clásicamente, el término "ácido de Lewis" se restringe a especies planas trigonales con un orbital p vacío, como BR3, donde R puede ser un sustituyente orgánico o un haluro. Para los propósitos de la discusión, incluso los compuestos complejos como Et3Al2Cl3 y AlCl3 se tratan como ácidos de Lewis planos trigonales. Los iones metálicos como Na+, Mg2+ y Ce3+, que invariablemente forman complejos con ligandos adicionales, son a menudo fuentes de derivados coordinativamente insaturados que forman aductos de Lewis tras la reacción con una base de Lewis. Otras reacciones podrían simplemente denominarse reacciones "catalizadas por ácido". Algunos compuestos, como el H2O, son tanto ácidos de Lewis como bases de Lewis, porque pueden aceptar un par de electrones o donar un par de electrones, dependiendo de la reacción.
Los ácidos de Lewis son diversos. Los más sencillos son los que reaccionan directamente con la base de Lewis. Pero más comunes son aquellos que experimentan una reacción antes de formar el aducto. Ejemplos de ácidos de Lewis basados en la definición general de aceptor de pares de electrones incluyen:
- el protón (H+) y los iones de onio compuestos ácidos, como NH4+ y H3O+
- cationes de metales de transición de alto estado de oxidación, por ejemplo, Fe3+;
- otros cationes metálicos, como Li+ y Mg2+, a menudo como sus complejos aquo o éter,
- especies planas trigonales, como BF3 y carbocationes H3C+
- pentahaluros de fósforo, arsénico y antimonio
- π pobres en electrones, tales como enonas y tetracianoetilenos.
Una vez más, la descripción de un ácido de Lewis a menudo se usa de manera flexible. Por ejemplo, en solución, los protones desnudos no existen.
Ácidos de Lewis simples[editar]
Algunos de los ejemplos más estudiados de tales ácidos de Lewis son los trihaluros de boro y los organoboranos, pero otros compuestos exhiben este comportamiento:
- BF3 + F- → BF4-
En este aducto, los cuatro centros de fluoruro (o más exactamente, ligandos) son equivalentes.
- BF3 + OMe2 → BF3OMe2
Tanto BF4- como BF3OMe2 son aductos de base de Lewis de trifluoruro de boro.
En muchos casos, los aductos violan la regla del octeto, como el anión triyoduro:
- I2 + I− → I3−
La variabilidad de los colores de las soluciones de yodo refleja las capacidades variables del solvente para formar aductos con el ácido de Lewis I2.
En algunos casos, el ácido de Lewis es capaz de unir dos bases de Lewis, siendo un ejemplo famoso la formación de hexafluorosilicato:
- SiF4 + 2 F− → SiF62−
Ácidos de Lewis complejos[editar]
La mayoría de los compuestos considerados ácidos de Lewis requieren un paso de activación antes de la formación del aducto con la base de Lewis. Casos bien conocidos son los trihaluros de aluminio, que en general se consideran ácidos de Lewis. Los trihaluros de aluminio, a diferencia de los trihaluros de boro, no existen en la forma AlX3, sino como agregados y polímeros que deben ser degradados por la base de Lewis.[6] Un caso más simple es la formación de aductos de borano. El BH3 monomérico no existe de manera apreciable, por lo que los aductos de borano se generan por degradación del diborano:
- B2H6 + 2 H− → 2 BH4−
En este caso, se puede aislar un intermedio B2H7-.
Muchos complejos metálicos sirven como ácidos de Lewis, pero generalmente solo después de disociar una base de Lewis unida más débilmente, a menudo agua.
- [Mg(H2O)6]2+ + 6 NH3 → [Mg(NH3)6]2+ + 6 H2O
H+ como ácido de Lewis[editar]
El protón (H+)[7] es uno de los más fuertes, pero también uno de los ácidos de Lewis más complicados. Es una convención ignorar el hecho de que un protón está fuertemente solvatado (unido al solvente). Con esta simplificación en mente, las reacciones ácido-base pueden verse como la formación de aductos:
- H+ + NH3 → NH4+
- H+ + OH− → H2O
Aplicaciones de los ácidos de Lewis[editar]
Un ejemplo típico de un ácido de Lewis en acción es la reacción de alquilación de Friedel-Crafts.[5] El paso clave es la aceptación por AlCl3 de un par solitario de iones cloruro, formando AlCl4- y la creación de la que es, fuertemente ácida, electrófilo, ion carbonio.
- RCl +AlCl3 → R+ + AlCl4−
Bases de Lewis[editar]
Una base de Lewis es una especie atómica o molecular donde el orbital molecular ocupado más alto (HOMO) está altamente localizado. Las bases de Lewis típicas son aminas convencionales tales como amoniaco y alquilaminas. Otras bases de Lewis comunes incluyen piridina y sus derivados. Algunas de las principales clases de bases de Lewis son
- aminas de fórmula NH3−xRx donde R = alquilo o arilo. Relacionados con estos están la piridina y sus derivados.
- fosfinas de fórmula PR3−xAx, donde R = alquilo, A = arilo.
- compuestos de O, S, Se y Te en estado de oxidación -2, incluyendo agua, éteres, cetonas
Las bases de Lewis más comunes son los aniones. La fuerza de correlatos basicidad de Lewis con el pKa del ácido de origen: ácidos con alto pKa dan buenas bases de Lewis. Como es habitual, un ácido más débil tiene una base conjugada más fuerte.
- Ejemplos de bases de Lewis basadas en la definición general de donante de pares de electrones incluyen:
Se ha evaluado la fuerza de las bases de Lewis para varios ácidos de Lewis, como I2, SbCl 5 y BF3.[8]
| Base de Lewis | Átomo donante | Entalpía de complejación (kJ/mol) |
|---|---|---|
| Et3N | N | 135 |
| Quinuclidina | N | 150 |
| Piridina | N | 128 |
| Acetonitrilo | N | 60 |
| Et2O | O | 78,8 |
| THF | O | 90,4 |
| Acetona | O | 76,0 |
| EtOAc | O | 75,5 |
| DMA | O | 112 |
| DMSO | O | 105 |
| Tetrahidrotiofeno | S | 51,6 |
| Trimetilfosfina | P | 97,3 |
Aplicaciones de las bases de Lewis[editar]
Casi todos los donantes de pares de electrones que forman compuestos al unirse a elementos de transición pueden verse como colecciones de bases de Lewis, o ligandos . Por tanto, una gran aplicación de las bases de Lewis es modificar la actividad y selectividad de los catalizadores metálicos. Por tanto, las bases de Lewis quirales confieren quiralidad a un catalizador, lo que permite la catálisis asimétrica, que es útil para la producción de productos farmacéuticos.
Muchas bases de Lewis son "multidentadas", es decir, pueden formar varios enlaces con el ácido de Lewis. Estas bases de Lewis multidentadas se denominan agentes quelantes.
Clasificación duro y blando[editar]
Los ácidos y bases de Lewis se clasifican comúnmente según su dureza o suavidad. En este contexto, fuerte implica pequeños y no polarizables y débil indica átomos más grandes que son más polarizables.
- Ácidos duros típicos: H+, cationes de metales alcalinos/alcalinotérreos, boranos, Zn2+
- Ácidos blandos típicos: Ag+, Mo(0), Ni(0), Pt2+
- Bases duras típicas: amoniaco y aminas, agua, carboxilatos, fluoruro y cloruro
- Bases blandas típicas: organofosfinas, tioéteres, monóxido de carbono, yoduro
Por ejemplo, una amina desplazará la fosfina del aducto con el ácido BF3. De la misma forma se podrían clasificar las bases. Por ejemplo, las bases que donan un par solitario de un átomo de oxígeno son más duras que las que se donan a través de un átomo de nitrógeno. Aunque la clasificación nunca se cuantificó, demostró ser muy útil para predecir la fuerza de la formación de aductos, utilizando los conceptos clave de que las interacciones entre ácido duro—base dura y ácido blando—base blanda son más fuertes que las interacciones ácido duro—base blanda o el ácido blando—base dura. La investigación posterior de la termodinámica de la interacción sugirió que las interacciones duro—duro son favorecidas por la entalpía, mientras que las interacciones blando—blando son favorecidas por la entropía.
Cuantificando la acidez de Lewis[editar]
Se han ideado muchos métodos para evaluar y predecir la acidez de Lewis. Muchos se basan en firmas espectroscópicas, como cambios de señales de RMN o bandas de infrarrojos, por ejemplo, el método de Gutmann-Beckett y el método de Childs.[9]
El modelo ECW es un modelo cuantitativo que describe y predice la fuerza de las interacciones ácido-base de Lewis, −ΔH. El modelo asignó parámetros E y C a muchos ácidos y bases de Lewis. Cada ácido se caracteriza por un EA y un CA. Cada base se caracteriza igualmente por su propia EB y CB. Los parámetros E y C se refieren, respectivamente, a las contribuciones electrostáticas y covalentes a la fuerza de los enlaces que formarán el ácido y la base. La ecuación es
- −ΔH = E A E B + C A C B + W
El término W representa una contribución de energía constante para la reacción ácido-base, como la escisión de un ácido dimérico o una base. La ecuación predice la reversión de las concentraciones de ácidos y bases. Las presentaciones gráficas de la ecuación muestran que no hay un solo orden de concentraciones de bases de Lewis o de concentraciones de ácidos de Lewis.[10][11] y que las escalas de propiedades individuales están limitadas a un rango más pequeño de ácidos o bases.
Historia[editar]
El concepto se originó con Gilbert N. Lewis, quien estudió los enlaces químicos. En 1923, Lewis escribió Una sustancia ácida es aquella que puede emplear un par de electrones solitarios de otra molécula para completar el grupo estable de uno de sus propios átomos.[2][12] La teoría ácido-base de Brønsted-Lowry se publicó en el mismo año. Las dos teorías son distintas pero complementarias. Una base de Lewis también es una base de Brønsted-Lowry, pero un ácido de Lewis no necesita ser un ácido de Brønsted-Lowry. La clasificación en ácidos y bases duros y blandos (teoría HSAB) siguió en 1963. La fuerza de las interacciones ácido-base de Lewis, medida por la entalpía estándar de formación de un aducto, puede predecirse mediante la ecuación de dos parámetros de Drago-Wayland.
Reformulación de la teoría de Lewis[editar]
Lewis había sugerido en 1916 que dos átomos se mantienen juntos en un enlace químico al compartir un par de electrones.[13] Cuando cada átomo contribuía con un electrón al enlace, se llamaba enlace covalente. Cuando ambos electrones provienen de uno de los átomos, se denomina enlace covalente dativo o enlace coordinado. La distinción no está muy clara. Por ejemplo, en la formación de un ion amonio a partir de amoníaco e hidrógeno, la molécula de amoníaco dona un par de electrones al protón; la identidad de los electrones se pierde en el ion amonio que se forma. No obstante, Lewis sugirió que un donante de pares de electrones se clasifique como base y un aceptor de pares de electrones se clasifique como ácido.
Una definición más moderna de un ácido de Lewis es una especie atómica o molecular con un orbital atómico o molecular vacío localizado de baja energía. Este orbital molecular de menor energía (LUMO) puede acomodar un par de electrones.
Comparación con la teoría de Brønsted-Lowry[editar]
Una base de Lewis es a menudo una base de Brønsted-Lowry, ya que puede donar un par de electrones a H+;[7] el protón es un ácido de Lewis, ya que puede aceptar un par de electrones. La base conjugada de un ácido de Brønsted-Lowry también es una base de Lewis, ya que la pérdida de H+ del ácido deja los electrones que se usaron para el enlace A-H como un par solitario en la base conjugada. Sin embargo, una base de Lewis puede ser muy difícil de protonar y aun así reaccionar con un ácido de Lewis. Por ejemplo, el monóxido de carbono es una base de Brønsted-Lowry muy débil, pero forma un fuerte aducto con BF3.
En otra comparación de la acidez de Lewis y Brønsted-Lowry realizada por Brown y Kanner,[14] 2,6-di-t-butilpiridina reacciona para formar la sal clorhidrato con HCl pero no con BF3. Este ejemplo demuestra que los factores estéricos, además de los factores de configuración electrónica, juegan un papel en la determinación de la fuerza de la interacción entre la di-t-butilpiridina voluminosa y el protón diminuto.
Véase también[editar]
- Ácido
- Base (química)
- Reacción ácido-base
- Teoría ácido-base de Brønsted-Lowry
- Ácido quiral de Lewis
- Par de Lewis frustrado
- Método de Gutmann-Beckett
- Modelo ECW
Referencias[editar]
- ↑ IUPAC Gold Book − Lewis acid
- ↑ a b Lewis, Gilbert Newton (1923). Valence and the Structure of Atoms and Molecules. New York, New York, U.S.A.: Chemical Catalog Company. p. 142. From p. 142: "We are inclined to think of substances as possessing acid or basic properties, without having a particular solvent in mind. It seems to me that with complete generality we may say that a basic substance is one which has a lone pair of electrons which may be used to complete the stable group of another atom, and that an acid substance is one which can employ a lone pair from another molecule in completing the stable group of one of its own atoms. In other words, the basic substance furnishes a pair of electrons for a chemical bond, the acid substance accepts such a pair."
- ↑ 1960-, Anslyn, Eric V. (2006). Modern physical organic chemistry. Dougherty, Dennis A., 1952-. Sausalito, CA: University Science. ISBN 1891389319. OCLC 55600610.
- ↑ Lepetit, Christine; Maraval, Valérie; Canac, Yves; Chauvin, Remi (2016). «On the nature of the dative bond: Coordination to metals and beyond. The carbon case». Coordination Chemistry Reviews 308: 59-75. doi:10.1016/j.ccr.2015.07.018.
- ↑ a b March, J. “Advanced Organic Chemistry” 4th Ed. J. Wiley and Sons, 1992: New York. ISBN 0-471-60180-2.
- ↑ Greenwood, N. N.; & Earnshaw, A. (1997). Chemistry of the Elements (2nd Edn.), Oxford:Butterworth-Heinemann. ISBN 0-7506-3365-4.
- ↑ a b Traditionally, but not precisely, H+ ions are referred as "protons". See Unión Internacional de Química Pura y Aplicada. «hydron». Compendium of Chemical Terminology. Versión en línea (en inglés).
- ↑ Christian Laurence and Jean-François Gal "Lewis Basicity and Affinity Scales : Data and Measurement" Wiley, 2009. ISBN 978-0-470-74957-9.
- ↑ Childs, R.F; Mulholland, D.L; Nixon, A. (1982). «Lewis acid adducts of α,β-unsaturated carbonyl and nitrile compounds. A nuclear magnetic resonance study». Can. J. Chem. 60 (6): 801-808. doi:10.1139/v82-117.
- ↑ Vogel G. C.;Drago, R. S. (1996). «The ECW Model». Journal of Chemical Education 73: 701-707. Bibcode:1996JChEd..73..701V. doi:10.1021/ed073p701.
- ↑ . Cramer, R. E., and Bopp, T. T. (1977) The Great E & C Plot. A graphical display of the enthalpies of adduct formation for Lewis acids and bases.. Journal of Chemical Education 54 612–613.
- ↑ Miessler, L. M., Tar, D. A., (1991) p. 166 – Table of discoveries attributes the date of publication/release for the Lewis theory as 1923.
- ↑ Lewis, Gilbert N. (April 1916). «The atom and the molecule». Journal of the American Chemical Society 38 (4): 762-785. doi:10.1021/ja02261a002.
- ↑ Brown HC and Kanner B. "Preparation and Reactions of 2,6-Di-t-butylpyridine and Related hindered Bases. A case of Steric Hindrance toward the Proton." J. Am. Chem. Soc. 88, 986 (1966).
Otras lecturas[editar]
- Jensen, W.B. (1980). The Lewis acid-base concepts : an overview. New York: Wiley. ISBN 0-471-03902-0.
- Yamamoto, Hisashi (1999). Lewis acid reagents : a practical approach. New York: Oxford University Press. ISBN 0-19-850099-8.
