Síndrome de Dravet
| Síndrome de Dravet | ||
|---|---|---|
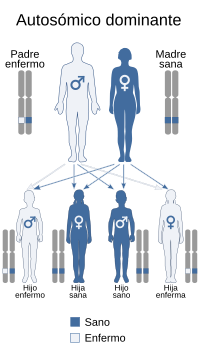 El Síndrome de Dravet se transmite con un patrón autosómico dominante | ||
| Especialidad | neurología | |
| Sinónimos | ||
| ||
El síndrome de Dravet, también conocido como epilepsia mioclónica grave de la infancia o epilepsia polimorfa, es una encefalopatía particular de la niñez. Fue identificado por Charlotte Dravet en 1978[1] y reconocido como un síndrome epiléptico por la Liga Internacional Contra la Epilepsia (ILAE) en 1985.
Es un síndrome epiléptico refractario al tratamiento farmacológico en la mayoría de los casos. Su incidencia es de 1/20 000 a 1/40 000 nacidos vivos y cuya prevalencia es del 7 % de las epilepsias en menores de 3 años. Afecta a varones y mujeres por igual y se da en todo el mundo.[2]
Aproximadamente un 25 % de los niños con síndrome de Dravet tienen historia familiar de epilepsia o de crisis convulsivas febriles.
El gen SCN1A que codifica para la subunidad alfa 1 del canal de sodio neuronal se encuentra con mutaciones hasta en un 80 % de los pacientes con epilepsia mioclónica grave de la infancia y un 5 % de niñas tienen una mutación en el GEN PCDH19. Se ha establecido como el más importante de los genes de la epilepsia que se conocen en la actualidad. Se han caracterizado más de 170 mutaciones patogénicas. La mayoría (95 %) de estas mutaciones son de novo. Hasta un 50 % de las mutaciones son mutaciones de truncado: el resto comprenden mutaciones por deleción, sitio de división, y sin sentido.
Los niños con síndrome de Dravet con frecuencia tienen un pobre desarrollo del lenguaje y las habilidades motoras, hiperactividad y dificultad para interactuar con otros niños.
Causas[editar]
En 2001, Claes y otros demostraron que el síndrome de Dravet es una enfermedad con un gran componente monogenético. En ese estudio inicial sobre siete pacientes, se encontraron mutaciones de novo en el gen SCN1A en el 100 % de los pacientes.[3]
Estudios posteriores confirmaron dichos hallazgos, aproximadamente el 70 al 80 % de los pacientes Dravet muestran mutaciones en el SCN1A, gen que codifica la subunidad alfa 1 del canal de sodio.[4]
Estas mutaciones heterocigotas son de novo en más de un 9 a 95 % de las ocasiones, las mutaciones familiares del 5 al 10 % son casi siempre mutaciones sin sentido.[3][5][6][7]
En las dos bases de datos más importantes se pueden hallar descritas más de 500 mutaciones del SCN1A.[8][9][10][11]
El 40 % de las mutaciones son missense (sin sentido); otro 40 %, trucantes (trucating); y el resto, splice-site.[12] En 2009 Depienne y otros al encontraron mutaciones en el gen PCDH19 (protocadherin 19) en pacientes femeninos diagnosticados con Dravet. Se estima que dicha mutación, que solo afecta a mujeres, se encuentra en un 5 % de todos los Dravet, y en un 25 % de las mujeres Dravet SCN1A negativos. Otros genes afectados de forma más infrecuente son el GABRG2, SCN1B (mutación homicigota). Un efecto potenciador se ha descrito en la coexistencia de la afectación del SCN9A con el SCN1A. También se ha descrito la existencia de un mosaicismo germinal y somático. Depenne (2010) cifra ese mosaicismo en un 7 %.[13] Se estima que el resto de Dravet con estudio genético negativo, el 15 al 25 % del total, puedan deberse a reordenamientos (rearrangements) o deleciones exonicas en los genes anteriores no medidas por las técnicas habituales de diagnóstico o a la existencia de otros genes no documentados hasta ahora.
La Fundación de Síndrome de Dravet, en colaboración con el Instituto de Genética Médica y Molecular (INGEMM) Hospital de La Paz Madrid, ha establecido un test genético que analiza todos los genes implicados en el Dravet de una manera gratuita.
Bases biológicas[editar]
En 15 a 25 % de los casos existe una historia familiar de crisis convulsivas febriles o de epilepsia, lo que sugiere una base genética para la enfermedad. Fujiwara reportó en 1990 un caso de gemelos monocigóticos con Síndrome de Dravet. Se desconoce el factor genético y el mecanismo de herencia. La deleción del exon 21 afecta el asa DlllS5-S6 de la proteína SCN1A. La deleción del exon 21-26 trunca la proteína en la misma posición. Las últimas investigaciones indican que un 5 % de las niñas diagnosticadas clínicamente con el Síndrome de Dravet dan positivo en un análisis de la proteína PCDH19
Diagnóstico[editar]
Diagnóstico Clínico[editar]
Algunos factores se han asociado con la mayor posibilidad de que el paciente tenga síndrome de Dravet:
- Inicio de crisis convulsivas febriles antes de los seis meses de vida
- Más de cinco episodios de crisis convulsivas
- Crisis convulsivas prolongadas (que duran más de 10 minutos).
Otros factores altamente asociados con esta posibilidad son:
- a). Convulsiones focalizadas a un hemicuerpo.
- b). Convulsiones parciales.
- c). Convulsiones mioclónicas.
- d). Convulsiones inducidas por agua caliente.
Si la suma del riesgo clínico es mayor de seis puntos, la sospecha de síndrome de Dravet es alta y se debe realizar un análisis para la búsqueda de la mutación SCN1A hay niñas con sospechas de Síndrome Dravet que dan negativo en este gen y tienen una mutación genética PCDH19.
Electroencefalografía[editar]
Un interesante patrón electroencefalográfico que combina espigas dobles o triples en la región frontal seguido o no por ondas lentas al estar despierto y activado por el sueño con descargas de 5-10 por segundo de espigas de 8-9 Hz se ha observado en un grupo de adolescentes con síndrome de Dravet.
Pronóstico y complicaciones[editar]
La evolución de esta epilepsia es muy variable. Los niños afectados, persistentemente presentaran crisis epilépticas. Las crisis convulsivas se presentan predominantemente al final de la noche a partir de la adolescencia. La fiebre continúa siendo un factor desencadenante y puede incluso ocasionar status epiléptico. La frecuencia de mortalidad es de hasta un 18 %, aunque estos datos están cambiando con la irrupción de nuevas terapias. Estudios recientes muestran que el diagnóstico se hace cada vez de manera más precoz, evitándose así el uso de medicaciones contraindicadas. Sin embargo, la necesidad de estimulación precoz y diferentes tipos de terapias motoras o del lenguaje, entre otras, supone una carga social y económica para las familias, como se ha mostrado una publicación reciente realizada en España.[14] Estudios recientes han mostrado que la pandemia COVID-19 ha afectado de manera negativa a familias afectadas, especialmente por los efectos indirectos (barreras en el sistema sanitario, efectos económicos, pérdida de terapias habituales etc.).[15]
Tratamiento[editar]
Los fármacos que en ocasiones funcionan son el Topiramato y el Valproato. La carbamazepina y la lamotrigina con frecuencia agravan las crisis. Además existe, la dieta cetogénica, que en varios casos funciona muy bien. Aunque el uso de tinturas de Cannabis Sativa es utilizado para reducir los episodios de crisis en algunos casos. Las investigaciones más recientes buscan utilizar substancias específicas dentro de la planta del cannabis, como el cannabidiol para el tratamiento de este síndrome y otras epilepsias farmacorresistentes.[16]
Referencias[editar]
- ↑ Dravet, Charlotte (2011). «Dravet syndrome history». Developmental Medicine & Child Neurology (en inglés) 53 (s2): 1-6. ISSN 1469-8749. doi:10.1111/j.1469-8749.2011.03964.x. Consultado el 24 de septiembre de 2021.
- ↑ Mingarro Castillo, M. ª Mercedes; Carmona de la Morena, Javier; Latre Martínez, Paz; Aras Portilla, Luis Miguel (2014-06). «Síndrome de Dravet». Revista Clínica de Medicina de Familia 7 (2): 134-136. ISSN 1699-695X. doi:10.4321/S1699-695X2014000200008. Consultado el 24 de septiembre de 2021.
- ↑ a b Claes L, Del-Favero J, Culemas B, lagae L Van Broeckhoven C, De Jonghe P. (2001). «De novo mutations in the sodium-channel gene SCN1A cause severe myoclonic epilepsy of infancy.». Am J Hum Genet 68: 1327-32.
- ↑ Marini C, Mei D, Temudo T et al. «Idiophatic epilepsies with seizures precitated by fever and SCN1A abnormalities.». Epilepsia 2007 48: 1678-96.
- ↑ Nabbout R, Gennaro E,. «Dalla Bernardina B et al Spectrum of SCN1A mutations in severe myoclonic epilepsy of infancy.». Neurology 2003 60: 1961-67.
- ↑ Wallace Rh, Hodgson BL, Grinton BE et al. «Sodium channel alpha1-subunit mutations in severe myoclonic epilepsy of infancy and infantile spasms.». Neurology 2003 61: 765-769.
- ↑ Fujiwara T, Sugawara T, Mazaki-Miyazaki E et al. «Mutations of sodium cannel alpha subunit type 1 (SCN1A) in intractable chilhood epilepsies with frequent generalized tonic-clonic seizures.». Brain 2003. 126 (pt3): 531-546.
- ↑ Claes LR, Deprez L, Suls A et al. «The SCN1A variant database:a novel research and diagnostic tool.». Hum Mutat 2009 30: E904-20.
- ↑ Lossin C. «a catalog of SCN1A variants.». Brain Dev 2009 31: 114-30.
- ↑ «Copia archivada». Archivado desde el original el 22 de julio de 2019. Consultado el 17 de diciembre de 2011.
- ↑ https://web.archive.org/web/20111009104545/http://www.scn1a.info/Home
- ↑ Marini C, Sheffe I, Nabbout R, Suls A, De Jonghe P, Zara F y Guerrini R. «The genetics of Dravet Syndrome.». Epilepsia 2001. 52(suppl 2): 24-29.
- ↑ Depienne C, Trouillard O, Gourfinkel-An I et al. «Mechanisms for variable expressivity of inherited SCN1A mutations causing Dravet Syndrome.». J Med Genet 2010 47: 404-10.
- ↑ S.L.U, 2020 Viguera Editores. «Análisis del impacto familiar y necesidades del síndrome de Dravet en España : Neurología.com». www.neurologia.com. Consultado el 14 de junio de 2020.
- ↑ Aledo‐Serrano, Ángel; Mingorance, Ana; Jiménez‐Huete, Adolfo; Toledano, Rafael; García‐Morales, Irene; Anciones, Carla; Gil‐Nagel, Antonio. «Genetic epilepsies and COVID-19 pandemic: Lessons from the caregiver perspective». Epilepsia (en inglés). n/a (n/a). ISSN 1528-1167. PMC 7276740. PMID 32420620. doi:10.1111/epi.16537. Consultado el 14 de junio de 2020.
- ↑ Luis Miguel Aras Portilla. «SÍNDROME DE DRAVET Y CANNABIDIOL». https://www.dravetfoundation.eu. Dravet Foundation. Archivado desde el original el 7 de noviembre de 2017. Consultado el 1 de noviembre de 2017.
Enlaces externos[editar]
- http://www.dravetfoundation.eu
- https://web.archive.org/web/20100922150015/http://www.sindromedewest.org/new/index.php?option=com_content&task=view&id=96&Itemid=86&lang=
- https://web.archive.org/web/20081225212135/http://doencasgeneticas.bloguepessoal.com/36668/Sindrome-de-Dravet/
- https://web.archive.org/web/20091212060615/http://secugen.es/pdf/Analisis%20Dravet.pdf
- http://www.todosobreepilepsia.com
- http://www.ilae.org/ctf/dravet.html
- https://web.archive.org/web/20081120213124/http://www.ninds.nih.gov/disorders/dravet_syndrome/dravet_syndrome.htm
- https://web.archive.org/web/20081109015542/http://www.dravet.com/dravet1uk.htm
- http://www.upsocl.com/inspiracion/crees-que-la-marihuana-es-solo-para-volarse-conoce-a-esta-nina-de-6-que-puede-estar-en-desacuerdo-contigo-en-eso/ Archivado el 6 de junio de 2014 en Wayback Machine.
