Pirazina
| Pirazina | |
|---|---|

| |
| Nombre IUPAC | Pirazina. |
| Otros nombres | 1,4-Diazina. 1,4-Diazobenceno |
| Fórmula empírica | C4H4N2 |
| Masa molecular | 80.09 g/mol |
| Estado físico/Color | Sólido/Incoloro |
| Número CAS | 290-37-9 |
| Propiedades | |
| Densidad | 1.031 g/cm³ a 20 °C |
| Punto de fusión | 52 °C (325 K) |
| Punto de ebullición | 115 °C (388 K) |
| Solubilidad en agua | Soluble |
| pKA | pKa=0.37[1] (Pirazina protonada) |
La pirazina es un compuesto orgánico aromático heterocíclico. Su molécula presenta una simetría con grupo puntual D2h. Es un sólido de apariencia cerosa o cristalina. Presenta un fuerte olor similar al de la piridina. Es volátil con vapor de agua.
Síntesis[editar]
Se han reportado diversos métodos para la síntesis de la pirazina y sus derivados:
Síntesis de Staedel-Rugheimer[editar]
Reportada por primera vez en 1876. El método consiste en la reacción de 2-cloroacetofenona con amoniaco para obtener la 2- aminocetona, la cual se condensa para formar la dihidropirazidina, y se forma la aromaticidad por oxidación posterior.[2]

Síntesis de Gutknecht[editar]
Reportada por primera vez en 1879. Este método consiste en la ciclización de α-aminocetonas, producidas por reducción de isonitroso cetonas, para obtenerse las dihidropirazinas. Estas son posteriormente deshidrogenadas con óxido de mercurio (I) o sulfato de cobre (II), e inclusive con oxígeno atmosférico:[3][4]

Síntesis de Gastaldi[editar]
Reportada por primera vez en 1921. Se requiere de (4-N-sulfonilamino)cianometil cetonas:[5][6]

Tratamiento térmico de aminoácidos[editar]
La formación de pirazinas por tratamiento térmico de L-serina y L-treonina ha sido estudiada por Chi-Kuen Shu. La L-serina y L-treonina, ya sea solos o combinados, se sometieron a calentamiento a 120 °C durante 4 horas y a 300 °C durante 7 min. A partir de serina se formaron la pirazina, la metilpirazina, la etilpirazina, la 2-etil-6-metilpirazina y la 2,6 dietilpirazina. A partir de la treonina se formaron la 2,5-dimetilpirazina, la 2,6-dimetilpirazina, la trimetilpirazina, la 2-etil-3,6 dimetilpirazina y la 2-etil-3,5-dimetilpirazina. La degradación térmica de serina o treonina se compone de varias reacciones complejas. Entre estas reacciones, se encuentra la descarbonilación con deshidratación para generar intermediarios α-aminocarbonílicos. La desaminación de estos intermediarios generan más intermediarios reactivos, tales como los α-hidroxicarbonilos. Por otra parte, la condensación aldólica de estos intermediarios reactivos producen α-dicarbonilos, los cuales se condensan con los aminoácidos.[7]
Reacciones[editar]
Ácido base[editar]
La pirazina es menos básica que la piridina, la piridazina y la pirimidina. Esta disminución de basicidad es provocada (como en las demás diazinas) por la desestabilización de los cationes monoprotonados debidos al efecto inductivo del segundo átomo de nitrógeno. Además, en el caso diferente de las otras diazinas, la pirazina presenta desestabilización por el efecto mesomérico entre el nitrógeno protonado y el nitrógeno neutro.[8]
Alquilaciones[editar]
La reacción de la pirazina con agentes alquilantes habituales (Yoduro de metilo, tetrafluoroborato de trietiloxonio), produce las N-alquilpirazinas correspondientes.[8]
Se ha reportado la alquilación de anillos de pirazina utilizando aldehídos y cetonas en presencia de un metal alcalino o metal alcalinotérreo en amoniaco líquido. Esta reacción se ha aplicado en pirazina, alquil-, dialquil-, amino- y metoxipirazinas con rendimientos moderados.[9]
Se puede alquilar el anillo de pirazina utilizando como sustrato cloropirazina y un carbanión, mediante una reacción tipo sustitución nucleófila aromática (SNA)[8]

Los grupos vinilo y fenilo pueden ser unidos a un anillo de pirazina por reacciones de acoplamiento con paladio como catalizador, tales como la reacción de Heck y el acoplamiento de Suzuki.[8]

Oxidación[editar]
Las pirazinas forman el N-óxido correspondiente al hacer reaccionar la pirazina con peróxido de hidrógeno en medio ácido.[8]

Halogenación[editar]
La cloración de la 2-metilpirazina ocurre en condiciones moderadas de acuerdo al mecanismo de SEA:[8]

Formilación[editar]
La pirazina se puede formilar por medio de una litiación en la posición 2, y utilizando formiato de etilo como agente formilante:[8]

Carboxilación[editar]
La carboxilación de pirazinas se puede llevar a cabo via radicales libres, donde se utiliza un promotor de radicales libres y el monoéster etílico del ácido oxálico:[8]

Abundancia biológica[editar]
La metilpirazinas se encuentran de manera natural en el jarabe de arce. El sabor se debe además a una combinación de metil, dimetil y trimetil pirazinas. De hecho, la trimetilpirazina se utiliza en la fabricación de jarabes con sabores artificiales que sustituyen al jarabe de arce.[10]
La ligustrazina (o tetrametilpirazina) es un principio activo presente en la planta chuanxiong (Ligusticum wallichii), popular en la medicina china tradicional.[11][12]

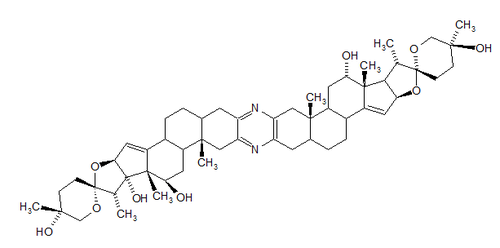
Las riterazinas son esteroides diméricos, altamente citotóxicos, aislados de tunicados del género Ritterella.[13]
El ácido aspergílico es un antibiótico que fue aislado por primera vez a partir de cultivos de algunas cepas de Aspergillus flavus.[14]

Importancia en la industria alimentaria[editar]
Las pirazinas se producen en los quesos durante el tratamiento térmico, siendo la trimetilpirazina el componente principal.La dimetilpirazina es utilizada por los chinos en la preparación de alimentos, ya que presenta un sabor característico que recuerda al maní frito, chocolate, mantequilla o patata frita. La metilpirazina también se utiliza como aditivo alimentario, debido a su aroma y el olor que recuerda al de la corteza de pan, nueces o palomitas de maíz. Las pirazinas más comunes como aditivos alimentarios se muestran a continuación:
| Tabla resumen. Algunas pirazinas responsables de aromas en alimentos.[10] | |||||||
|---|---|---|---|---|---|---|---|
| Nombre | Estructura | Aroma | Umbral de detección (μg/L; agua) | ||||
| Trimetilpirazina |  |
Papa cocida, cacahuete | 90 | ||||
| 2-Etil-3,5-dimetilpirazina |  |
Cacao tostado | 0.04 | ||||
| 2-Vinil-3,5-dimetilpirazina |  |
Pan tostado | 0.1 | ||||
| 2-Etil-3,6-dimetilpirazina |  |
Cacao tostado | 9 | ||||
| 2,3-Dietil-5-metilpirazina |  |
Pan tostado | 0.09 | ||||
| 2-Vinil-3-etil-5-metilpirazina |  |
Pan tostado | 0.1 | ||||
| Acetilpirazina |  |
Maíz asado | 62 | ||||
| 2-Isopropil-3-metoxipirazina |  |
Papas fritas | 0.002 | ||||
| 2-sec-butil-3-metoxipirazina |  |
Tierra | 0.001 | ||||
| 2-Isobutil-3-metoxipirazina |  |
Chile asado | 0.002 | ||||
Véase también[editar]
Enlaces externos[editar]
Referencias[editar]
- ↑ Brown, H.C., et al., in Baude, E.A. and Nachod, F.C., Determination of Organic Structures by Physical Methods, Academic Press, New York, 1955.
- ↑ Ueber die Einwirkung von Ammoniak auf Chloracetylbenzol (p 563-564) W. Staedel, L. Rügheimer doi 10.1002/cber.187600901174 Berichte der deutschen chemischen Gesellschaft Volume 9, Issue 1 , Pages 563 - 564 1876
- ↑ Mittheilungen Ueber Nitrosoäthylmethylketon H. Gutknecht Berichte der deutschen chemischen Gesellschaft Volume 12, Issue 2 , Pages 2290 - 2292 1879 doi 10.1002/cber.187901202284
- ↑ Heterocyclic chemistry T.L. Gilchrist ISBN 0-582-01421-2
- ↑ G. Gastaldi, Gazz. Chim. Ital. 51, (1921) 233
- ↑ Amines: Synthesis, Properties and Applications Stephen A. Lawrence 2004 Cambridge University Press ISBN 0-521-78284-8
- ↑ Chi-Kuen Shu (1999). «Pyrazine Formation from Serine and Threonine». J. Agric. Food Chem. 47 (10): 4332-4335. doi:10.1021/jf9813687.
- ↑ a b c d e f g h John A. Joule, Keith Mills (2010). Heterocyclic Chemistry. John Wiley and Sons, 5a ed. ISBN 9781405193658.
- ↑ A. F. Bramwell, L. S. Payne, G. Riezebos, P. Ward and R. D. Wells (1971). «The nuclear alkylation of pyrazines by ketones and aldehydes». J. Chem. Soc. C: 1627-1632. doi:10.1039/J39710001627.
- ↑ a b Hans-Dieter Belitz, Werner Grosch, Peter Schieberle (2009). Food Chemistry. Springer, 4a ed. ISBN 9783540699330.
- ↑ http://www.itmonline.org/arts/ligustrazine.htm
- ↑ Wei Xu, Qingping Xu, Jinghua Chen, Zhenming Lu, Rong Xia, Guoquan Li, Zhenghong Xu, Yanhe Ma (2011). «Ligustrazine formation in Zhenjiang aromatic vinegar: changes during fermentation and storing process». J Sci Agric 91 (8). doi:10.1002/jsfa.4356.
- ↑ Seketsu Fukuzawa, Shigeki Matsunaga, Nobuhiro Fusetani (1994). «Ritterazine A, a highly cytotoxic dimeric steroidal alkaloid, from the tunicate Ritterella tokioka». J. Org. Chem. 59 (21): 6164-6166. doi:10.1021/jo00100a014.
- ↑ James C. Macdonald (1961). «Biosynthesis of Aspergillic Acid». Journal Of Biological Chemistry 236 (2): 512-514.
