Diferencia entre revisiones de «Nitrato de celulosa»
Sin resumen de edición |
m Revertidos los cambios de 189.194.249.75 a la última edición de Muro Bot |
||
| Línea 1: | Línea 1: | ||
{{fusionar desde|Piroxilo}} |
|||
{{Referencias}} |
{{Referencias}} |
||
| Línea 72: | Línea 72: | ||
[[uk:Нітроцелюлоза]] |
[[uk:Нітроцелюлоза]] |
||
[[zh:硝化纤维]] |
[[zh:硝化纤维]] |
||
--[[Especial:Contributions/189.194.249.75|189.194.249.75]] ([[Usuario Discusión:189.194.249.75|discusión]]) 00:51 11 jul 2009 (UTC) |
|||
Revisión del 00:51 11 jul 2009
| Nitrato de celulosa | ||
|---|---|---|
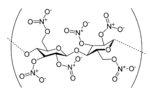 | ||
| Nombre IUPAC | ||
| Nitrato de celulosa | ||
| General | ||
| Otros nombres | Nitrocelulosa | |
| Fórmula molecular | ? | |
El nitrato de celulosa, nitrocelulosa, fulmicotón o algodón pólvora fue sintetizado por primera vez en el año 1845 por Schönbein. Es un sólido parecido al algodón, o un líquido gelatinoso ligeramente amarillo o incoloro con olor a éter. Se emplea en la elaboración de explosivos, propulsores para cohetes, celuloide (base transparente para las emulsiones de las películas fotográficas) y como materia prima en la elaboración de pinturas, lacas, barnices, tintas, selladores y otros productos similares. Es famoso su uso tradicional, como laca nitrocelulósica aplicada como acabado sobre la madera en guitarras eléctricas de calidad.[cita requerida]
Fabricación
Se sintetiza a base de algodón, nítrico y sulfúrico, los mismos utilizados en la nitroglicerina. De esta manera, forma principalmente nitrato de celulosa.
Para obtenerlo se hace una mezcla de 1 volumen de ácido nítrico (HNO3) y tres volúmenes de ácido sulfúrico (H2SO4), pues la reacción de la celulosa con el ácido nítrico, además de formar la nitrocelulosa, produce agua, la cual diluye rápidamente al ácido nítrico. Al ser el ácido sulfúrico higroscópico, éste toma el exceso de agua en la reacción sin diluir al ácido nítrico.
Cuando la mezcla de ambos ácidos está fría, se introduce el algodón y deja durante unos 15 minutos estabilizando la temperatura (enfriando, ya que la reacción es muy exotérmica), después de lo cual se lava en acetona y se seca. Opcional al lavado con acetona es un lavado rápido con agua y bicarbonato de sodio (NaHCO3), que eliminará posibles residuos de ácido; aunque hará que la nitrocelulosa obtenida se seque más lentamente, ya que el agua es menos volátil que la acetona.
Una vez fabricada conserva el aspecto de algodón ordinario, aunque la nitrocelulosa es más áspera al tacto.

La obtención descrita anteriormente genera una nitrocelulosa altamente explosiva y peligrosa, con un grado altisímo de pureza; por lo que se recomienda variar las proporciones con respecto al ácido sulfúrico si se desea hacer demostraciones sencillas. Cuanto menos ácido sulfúrico sea usado (Con respecto a la propoción 1HNO3:3H2SO4), menor grado de pureza tendrá la nitrocelulosa.
Una vez seco, es soluble en el dietiléter, acetona y el éter acético. Se enciende a 120 ºC. Al arder produce dióxido de carbono, monóxido de carbono, agua y nitrogeno.
La nitrocelulosa se obtiene, a nivel industrial, por nitración de alfa-celulosa de algodón o pulpa de madera.
Propiedades
Es uno de los explosivos plásticos más baratos. Es rígido y resistente al impacto. Admite técnicas finales de corte y mecanizado (evitando sobrecalentamiento). No es un buen aislante eléctrico. El celuloide se disuelve en acetona y acetato de amilo. Es atacado por los ácidos y bases (poca resistencia química). Se endurece al envejecer y es atacado por la radiación solar. Es inflamable, con deflagración. Los productos emitidos en la degradación térmica son tóxicos.
Es muy estable en comparación de la nitroglicerina, incluso es más estable que la pólvora. Los magos e ilusionistas lo utilizan para crear ilusiones con fuego.
Anecdotario
Como curiosidad, indicar que este explosivo es el que se usa en el libro de Julio Verne "De la Tierra a la Luna" (1865) para impulsar la bala que transporta a los protagonistas en su periplo.
