Batería recargable

Una pila (una celda) o batería (varias celdas) recargable (también llamada acumulador recargable) es un grupo de una o más celdas electroquímicas secundarias.
Nombre[editar]
Tanto pila como batería son términos provenientes de los primeros tiempos del estudio de la electricidad, cuando se juntaban varios elementos o celdas —en el primer caso uno encima de otro, "apilados", y en el segundo adosados lateralmente, "en batería"— como se sigue haciendo actualmente, para así aumentar la magnitud de los fenómenos eléctricos y poder estudiarlos sistemáticamente.
En castellano ha sido costumbre llamar batería a los dispositivos recargables, mientras que a los no recargable se ha venido llamando pila, aunque hoy día no se hace tal distinción; más bien se utilizan uno u otro término en función de su forma y tamaño. No obstante, se entiende que las baterías poseen dos o más celdas de energías y las pilas son de una sola celda de energía.
Funcionamiento[editar]
Las baterías recargables usan reacciones electroquímicas que son eléctricamente reversibles,[1] es decir:
- Cuando la reacción transcurre en un sentido, se agotan los materiales de la pila mientras se genera una corriente eléctrica.
- Para que la reacción transcurra en sentido inverso, es necesaria una corriente eléctrica para regenerar los materiales consumidos.
Las baterías recargables vienen en diferentes tamaños y emplean diferentes combinaciones de productos químicos. Las celdas secundarias ("batería recargable") utilizadas con más frecuencia son las de plomo-ácido, la de níquel-cadmio (NiCd), la de níquel-metal hidruro (NiMH), la de iones de litio (Li-ion), y la de polímero de iones de litio (polímero de Li-ion).
Las baterías recargables pueden ofrecer beneficios económicos y ambientales en comparación con las pilas desechables. Algunos tipos de baterías recargables están disponibles en los mismos tamaños que los tipos desechables. Aunque las pilas recargables tienen un mayor costo inicial, pueden ser recargadas muchas veces. La selección adecuada de una batería recargable puede reducir los materiales tóxicos desechados en los vertederos, frente a una serie equivalente de pilas de un solo uso. Por ejemplo, los fabricantes de baterías o pilas recargables de NiMH proclaman una vida de servicio de 100-1000 ciclos de carga/descarga para sus baterías.
Usos y aplicaciones[editar]

Actualmente se utilizan pilas o baterías recargables para aplicaciones tales como motores de arranque de automóviles, dispositivos portátiles de consumo, vehículos ligeros (como sillas de ruedas motorizadas, carros de golf, bicicletas eléctricas y carretillas elevadoras eléctricas), herramientas y sistemas de alimentación ininterrumpida. También en nuevas aplicaciones como para vehículos eléctricos híbridos y vehículos eléctricos están impulsando la tecnología para reducir costos, reducir el peso y aumentar de la vida útil.[2]
A diferencia de las pilas no recargables (celdas primarias), las baterías recargables tienen que ser cargadas antes de su primer uso, aunque algunas vienen recargadas de fábrica. La necesidad de cargar las pilas recargables antes de su uso disuade a los posibles compradores que quieran usar las pilas inmediatamente. Sin embargo, las nuevas baterías de baja autodescarga permiten a los usuarios comprar una batería recargable que ya tienen cerca del 70 % de su capacidad nominal, permitiendo a los consumidores utilizar las baterías inmediatamente y regenerarlas (recargarlas) más tarde hasta el 100 % de su capacidad.
Hay aplicaciones de almacenamiento de energía en red que emplean baterías recargables industriales para nivelación de carga, almacenando la energía eléctrica durante períodos de carga máxima para su posterior uso, y para aprovechamiento de energías renovables, tales como el almacenamiento de energía generada a partir de paneles fotovoltaicos durante el día para ser utilizada durante la noche. Al cargar las baterías durante los períodos de baja demanda y devolver la energía a la red durante los períodos de alta demanda eléctrica, la nivelación de carga ayuda a eliminar la necesidad de costosas plantas de energía en horas punta y ayuda a amortizar el costo de los generadores durante las horas de más funcionamiento.
La Asociación Nacional de Fabricantes Eléctricos de Estados Unidos ha estimado que la demanda de pilas recargables en EE. UU. está creciendo dos veces más deprisa que la demanda de las no-recargables (desechables).[3]
Baterías externas[editar]
Las baterías externas para tabletas, smartphones y portátiles,[4] reduce significativamente la dependencia de una fuente de electricidad externa (como un cargador de corriente alterna), porque la reemplaza, al menos temporalmente. De esta manera, el dispositivo móvil funciona como si estuviera conectado. La salida suele ser mini o micro-USB y USB TIPO C.
Para los teléfonos móviles actuales se utiliza una batería externa de al menos 3000 mAh, ya que una batería externa no proporciona el 100 % de su capacidad, debido a que se pierde parte de su energía en la transferencia y la conversión de voltaje.[5]
Algunas baterías externas cuentan con paneles solares para uso al aire libre y con la posibilidad de que se le inserten usar pilas.
Carga y descarga[editar]
Información adicional: Cargador de batería
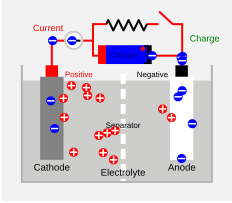
Durante la carga, el material activo del electrodo positivo se oxida, liberando electrones, y el material del electrodo negativo es reducido, captando dichos electrones. Estos electrones constituyen el flujo de corriente eléctrica que atraviesa el circuito externo. El electrolito puede servir como un simple medio de transporte para el flujo de iones entre los electrodos, como en el caso de la batería de iones de litio y la batería de níquel-cadmio, o puede ser un participante activo en la reacción electroquímica, como en la batería de plomo-ácido.


La energía utilizada para cargar las baterías recargables en su mayoría proviene de corriente alterna de la red eléctrica, utilizando un rectificador (cargador). La mayoría de los cargadores de baterías pueden tardar varias horas para cargar una batería. La mayoría de las baterías pueden ser cargadas en mucho menos tiempo de lo que emplean los cargadores de baterías más comunes y simples. Duracell y Rayovac ahora venden cargadores que pueden regenerar o recargar baterías de NiMH tamaño AA y AAA en sólo 15 minutos; Energizer vende cargadores que pueden recargar baterías de tamaño C/D y baterías de NiMH de 9 V. Sin embargo, las altas tasas de carga (por ejemplo, el empleo de cargadores de 15 minutos o cargadores de 1 hora) causarán daño a largo plazo en las baterías recargables de NiMH y en la mayoría de las otras.
Las baterías recargables son susceptibles a daños debido a recarga inversa (inversión de los polos) si están completamente descargadas. Existen cargadores de baterías totalmente integrados que optimizan la corriente de carga.
Además, el intento de recargar las pilas o baterías no recargables conlleva una pequeña posibilidad de causar una explosión de la pila.
Las baterías de flujo, que no son utilizados habitualmente por los consumidores, se recargan mediante la sustitución del líquido electrolito.
En las especificaciones técnicas de los fabricantes de la batería a menudo se refieren al parámetro VPC. VPC significa voltios por celda, y se refiere al voltaje de las celdas individuales que conforman la batería o celda secundaria. Por ejemplo, para cargar una batería de 12 V (con 6 celdas de 2 V cada una) a 2,3 VPC se necesita una tensión de 6 x 2,3 V = 13,8 V a través de los terminales externos de la batería.
La mayoría de pilas de NiMH tipo AA o AAA disponen de celdas de 1,2 V. No obstante, esto no es un problema en la mayoría de los dispositivos porque las pilas alcalinas sufren una caída de tensión cuando se agota la energía. La mayoría de los dispositivos están diseñados para seguir funcionando con un voltaje reducido de entre 0,9 y 1,1 V.
Recarga inversa (polaridad invertida)[editar]
La recarga inversa daña las pilas, y se produce cuando una batería recargable se recarga con la polaridad invertida. La recarga inversa se puede producir en una serie de circunstancias, siendo las tres más comunes las siguientes:
- Cuando la batería está incorrectamente insertada en el cargador, con los polos al revés.
- Cuando un cargador de baterías de tipo automoción está conectado a la inversa a los terminales de la batería. Esto suele ocurrir cuando se está cargando una batería completamente descargada, de lo contrario se producirán chispas.
- Cuando las celdas están conectadas en serie y muy descargadas.
Cuando una celda se descarga completamente y no las demás, las celdas no descargadas aplicarán una corriente inversa a la celda descargada. Esto es comúnmente llamado "inversión de la celda". La inversión de celda acorta significativamente la vida de la célula afectada, por lo que acorta la vida en general de la batería. En algunos casos extremos, la célula revertida puede comenzar a emitir humo o incendiarse. Algunas células de tipo Ni-Cd presentan un efecto memoria. Algunas células de tipo Ni-Cd, que no se cargan y descargan completamente cada cierto tiempo pueden perder su capacidad de mantener una carga completa, es decir, presentan disminución de la capacidad. Reciclar una batería multicelda en descarga profunda para superar este efecto memoria puede causar reversión de células y hacer más daño que bien. En aplicaciones críticas que utilizan baterías de Ni-Cd, como en los aviones, cada célula se descarga individualmente mediante la conexión de un clip de carga en los terminales de cada célula, evitando así la inversión de célula para, a continuación, cargar las pilas en serie.
Profundidad de descarga[editar]
La profundidad de descarga se establece normalmente como un porcentaje de la capacidad nominal en amperios-hora; un 0 % de profundidad de descarga significa que no hay descarga. Puesto que la capacidad utilizable de una batería depende de la velocidad de descarga y de la tensión admisible al final de la descarga, la profundidad de la descarga debe estar calificada para mostrar de qué forma se va a medir. Debido a las variaciones en la fabricación y el envejecimiento de la batería, la profundidad de descarga para la descarga completa puede cambiar con el tiempo y los ciclos de descarga. En general, un sistema de baterías recargable va a tolerar más ciclos de carga y descarga si la profundidad de descarga es más baja en cada ciclo.[6]
Componentes activos[editar]
Los componentes activos de una celda secundaria son los productos químicos que componen los materiales activos de los electrodos positivo y negativo, y el electrolito. Los electrodos positivo y negativo contienen diferentes materiales: en el positivo se presentan materiales con un potencial de reducción alto o positivos; en el negativo tendremos materiales con potencial de oxidación bajo o negativos. La diferencia de estos potenciales es el potencial estándar de celda o fuerza electromotriz (ε) o tensión de la pila.
En las células primarias los electrodos positivo y negativo son conocidos como cátodo y ánodo, respectivamente. Aunque este convenio se traslada a veces a los sistemas recargables —especialmente las pilas de iones litio, a causa de su origen en las celdas de litio— esta práctica puede llevar a confusión. En las pilas recargables el electrodo positivo es el cátodo en la descarga y el ánodo en la carga, y viceversa para el electrodo negativo.
Tabla de tecnologías usadas en las baterías y pilas recargables[editar]
| Tipo | Voltajea | Densidad de energíab | Potenciac | Eficienciad | E/$e | Descargaf | Ciclosg | Vida mediah | ||
|---|---|---|---|---|---|---|---|---|---|---|
| (V) | (MJ/kg) | (Wh/kg) | (Wh/L) | (W/kg) | (%) | (Wh/$) | (%/mes) | (#) | (años) | |
| Plomo y ácido | 2.1 | 0.11-0.14 | 30-40 | 60-75 | 180 | 70-92 % | 5-8 | 3-4 % | 500-800 | 5-8 (batería de coche), 20 (estacionaria) |
| VRLAi | 2.105 | |||||||||
| Alcalina | 1.5 | 0.31 | 85 | 250 | 50 | 99.9 % | 7.7 | <0.3 | 100-1000 | <5 |
| Ni-Hierro | 1.2 | 0.18 | 50 | 100 | 65 % | 5-7.3[7] | 20-40 % | 50+ | ||
| Ni-Cadmio | 1.2 | 0.14-0.22 | 40-60 | 50-150 | 150 | 70-90 % | 20 % | 1500 | ||
| Ni-H2 | 1.5 | 75 | 20 000 | 15+ | ||||||
| NiMH | 1.2 | 0.11-0.29 | 30-80 | 140-300 | 250-1000 | 66 % | 1.37 | 20 % | 1000 | |
| Ni-zinc | 1.7 | 0.22 | 60 | 170 | 900 | 2-3.3 | 100-500 | |||
| ion Li | 3.6 | 0.58 | 160 | 270 | 1800 | 99.9 % | 2.8-5[8] | 5-10 % | 1200 | 2-3 |
| polímeros Li | 3.7 | 0.47-0.72 | 130-200 | 300 | 3000+ | 99.8 % | 2.8-5.0 | 500~1000 | 2-3 | |
| LiFePO4 | 3.25 | 80-120 | 170[9] | 1400 | 0.7-3.0 | 2000+[10] | ||||
| Li azufre[11] | 2.0 | 0.94-1.44[12] | 400[13] | 350 | ~100 | |||||
| Li titanato | 2.3 | 90 | 4000+ | 87-95 %r | 0.5-1.0[14] | 9000+ | 20+ | |||
| Li película delgada | ? | 350 | 959 | ? | ?p[15] | 40000 | ||||
| ZnBr | 75-85 | |||||||||
| V redox | 1.15-1.55 | 25-35[16] | 80 %[17] | 20 %[17] | 14 000[18] | 10(estacionario)[17] | ||||
| NaS | 150 | 89-92 % | ||||||||
| Sal fundida | 70-110[19] | 150-220 | 4.54[20] | 3000+ | 8+ | |||||
| Plata-zinc (Ag-Zn) | 1.86 | 130 | 240 | |||||||
- Notas
Para mayor brevedad, las entradas en la tabla tuvieron que ser abreviadas. Para una descripción completa, consulte el artículo individual sobre cada tipo de pila o batería. Los tipos de baterías para los que no hay ningún artículo todavía se enumeran a continuación.
- a Tensión nominal de la pila en V.

- b Densidad de energía = energía/peso o energía/tamaño, dada en tres diferentes unidades.
- c Potencia específica = potencia/peso en W/kg.
- d % eficiencia carga/descarga.
- e Cociente Energía/precio al consumidor en W·h/dólares EE .UU. (aproximadamente).
- j Profundidad de descarga de seguridad para mantener los ciclos de vida.
- f Velocidad de autodescarga en %/mes.
- g Durabilidad de ciclos, en número de ciclos.
- h Tiempo de duración en años.
- i Baterías selladas VRLA o recombinantes (incluye baterías con electrolito fijado en gel y absorbido en fieltro).
- p Producción piloto.
- r Depende de la tasa de carga.
Baterías recargables más comunes[editar]
- Batería de níquel-cadmio (NiCd)
Creada por Waldemar Jungner de Suecia en 1899, basada en la primera batería alcalina de Thomas Edison. Usa hidróxido de níquel e hidróxido de cadmio como electrodos.[21] El cadmio es un elemento tóxico, y fue prohibido para la mayoría de los usos por la Unión Europea en 2004. Las baterías de níquel-cadmio han sido casi completamente sustituidas por baterías de níquel-hidruro metálico.
Se desarrolló por primera vez alrededor de 1980. La batería tiene una aleación capaz de absorber hidrógeno como electrodo negativo, en lugar de cadmio.
La tecnología de la batería de iones litio aún no ha alcanzado la madurez. Sin embargo, estas baterías son la elección preferente en electrónica de consumo y muchas tienen una de las mejores relaciones energía/masa y una pérdida muy lenta de carga cuando no está en uso. La popularidad de las baterías de litio-ion se ha extendido mientras la tecnología continúa mejorando.
Es una de las baterías recargables que más prometen. Tienen una alta densidad energética, pero operan en un rango de temperaturas que va de 270 °C a 350 °C, lo que requiere un aislamiento. Son apropiadas en autobuses eléctricos. En Stabio, en el sur del cantón del Tesino (Suiza), se está construyendo una fábrica para producir estas baterías en serie. Entre sus inconvenientes, además de la temperatura de trabajo, están las pérdidas térmicas cuando no se usa la batería. El automóvil eléctrico Think City va equipado con baterías Zebra Na-NiCl de 17,5 kW
Tipos menos comunes[editar]
- Batería de litio-azufre
Un nuevo modelo de batería desarrollado por Sion Power desde 1994.[23] Afirma poseer un cociente energía/peso superior que las tecnologías actuales de baterías de litio en el mercado. También su menor coste material puede ayudar a que este producto llegue al mercado de masas.[24] No debe confundirse con las baterías de dióxido de azufre y litio (Li-SO2) que pueden explotar cuando se recargan.
- Batería de película delgada
Una mejora emergente de la tecnología de iones de litio ha sido llevada a cabo por Excellatron.[25] Los desarrolladores proclaman haber conseguido un aumento muy grande en los ciclos de recarga, alrededor de 40 000 ciclos. Con mayores tasas de carga y descarga. Al menos 5 C de tasa de carga. Descargas mantenidas de 60 C, y picos de tasa de descarga de 1000 C. Y también un aumento significativo de la energía específica, y la densidad de energía.[26] También Infinite Power Solutions fabrica baterías de película delgada (TFB) para aplicacione de microelectrónica, que son pilas de litio de estado sólido, flexibles y recargables.[27]
- Batería inteligente
Una batería inteligente tiene el circuito de control de la tensión construido en el interior. Véase también: Sistema de batería inteligente
- Batería de plomo y ácido, con carbono en espuma.
Firefly Energy ha desarrollado una batería de plomo y ácido, con carbono en espuma, con una densidad de energía reportada de un 30-40 % más que su valor original 38 W.h/kg,[28] con una duración larga y alta densidad de potencia.
Baterías plegables[editar]
Una importante novedad han supuesto la invención de las baterías flexibles, que se pueden hacer en papel fino.[29][30]
Nokia ha patentado una batería plegable para los miniatura, compuesta por una gran serie de células flexibles. Se trataría, según los expertos, de una tecnología que permitiría fabricar teléfonos mucho más pequeños y delgados. Las baterías flexibles de Nokia podrían integrarse en los denominados teléfonos con pantalla curva. Una batería más flexible —o flexible por completo— permitiría a los fabricantes trabajar con teléfonos mucho más curvados o enrollables.[31]
Investigaciones recientes[editar]
En 2007, el profesor asistente Yi Cui y sus colegas del Departamento de Ciencia e Ingeniería de los Materiales, de la Universidad de Stanford, descubrieron que, usando nanocables de silicio como ánodo, se aumenta la densidad de carga volumétrica del ánodo hasta 10 veces. Véase también Batería de nanohilos.[32][33]
Ceramatec, una filial de investigación y desarrollo de CoorsTek, está probando una batería que contiene un trozo de metal de sodio sólido asociado a un compuesto de azufre por un extraordinaria membrana de cerámica fina como el papel. La membrana conduce a los iones de un lado a otro para generar una corriente. La compañía afirma que puede meter alrededor de 40 kilovatios-hora de energía en un paquete del tamaño de un refrigerador, y operar por debajo de 90 grados centígrados. La empresa también afirma que su batería permitirá 3650 ciclos de recarga (o aproximadamente 1 vez por día durante una década.)[34]
Alternativas[editar]
Para usos como radios portátiles y linternas, las baterías recargables pueden ser sustituidas por mecanismos de relojería o dínamos que se mueven con una manivela por el usuario para proporcionar la energía. Para el transporte, sistemas de suministro ininterrumpido de energía y laboratorios, los sistemas de almacenamiento de energía mediante volante almacenan energía en un rotor que gira para reconversión en energía eléctrica cuando sea necesario; esos sistemas se pueden utilizar para proporcionar grandes pulsos de energía que de otro modo sería objetable en una red eléctrica común.
Un desarrollo es el empleo de ultracondensadores para el sector del transporte y de telefonía móvil, que permite cargar el móvil en 20 segundos,[35] utilizando un gran condensador para almacenar la energía en lugar de los bancos de baterías recargables usados en vehículo eléctrico. Un inconveniente de los condensadores en comparación con las baterías es que la tensión en bornes disminuye rápidamente, un condensador al que le queda el 25 % de su energía inicial, tendrá la mitad de la tensión inicial. Los sistemas de baterías tienden a tener una tensión en los terminales que no disminuye rápidamente hasta casi estar agotados. Esta característica dificulta el diseño de electrónica de potencia para el uso con ultracapacitadores. Sin embargo, hay beneficios potenciales en la eficiencia del ciclo, la duración, y el peso en comparación con los sistemas recargables.
Véase también[editar]
- Batería
- Batería de automóvil
- Batería externa para móvil.
- Batería de níquel-litio
- Carga de mantenimiento
- Nanobatería
- Pila
- Reciclaje de pilas
- Supercondensador
- Tarjeta inteligente
- Vida útil
- WiTricity
- Reacción reversible
Referencias[editar]
- ↑ INIECO, Equipo (2011-08). Montaje eléctrico y electrónico en instalaciones solares fotovoltaicas. Editorial Vértice. ISBN 9788499313504. Consultado el 27 de marzo de 2018.
- ↑ David Linden, Thomas B. Reddy (ed). Handbook Of Batteries 3rd Edition. McGraw-Hill, New York, 2002 ISBN 0-07-135978-8 chapter 22
- ↑ «U.S. EPA - Product Stewardship - Batteries». 27 de septiembre de 2006. Archivado desde el original el 27 de septiembre de 2006. Consultado el 13 de septiembre de 2017.
- ↑ http://batterywiki.batteries-company.co.uk/universal-external-battery-makes-recharging-convenient-and-easy/ (enlace roto disponible en Internet Archive; véase el historial, la primera versión y la última).
- ↑ «Capacidad real de una batería externa».
- ↑ Reddy, Handbook of Batteries page 22-20
- ↑ «mpoweruk.com: Accumulator and battery comparisons (pdf)».
- ↑ http://www.werbos.com/E/WhoKilledElecPJW.htm (que enlaza a «Copia archivada». Archivado desde el original el 29 de septiembre de 2007. Consultado el 5 de noviembre de 2007.)
- ↑ «Electric bike hub motors, LiFepo4batteries, regen controllers, electric scooters». www.falconev.com.
- ↑ Zero Emission Vehicles Australia
- ↑ Lithium_Sulfur
- ↑ «Solar plane makes record flight». 24 de agosto de 2008 – via news.bbc.co.uk.
- ↑ «Wayback Machine». 18 de julio de 2009. Archivado desde el original el 18 de julio de 2009. Consultado el 13 de septiembre de 2017.
- ↑ Power & Energy Systems FAQ
- ↑ «Excellatron - the Company». www.excellatron.com. Archivado desde el original el 8 de agosto de 2012. Consultado el 7 de marzo de 2010.
- ↑ «Vanadium Redox Battery». Archivado desde el original el 26 de abril de 2012. Consultado el 7 de marzo de 2010.
- ↑ a b c «Copia archivada». Archivado desde el original el 17 de mayo de 2016. Consultado el 17 de mayo de 2016.
- ↑ «The Vanadium Advantage: Flow Batteries Put Wind Energy in the Bank». 20 de enero de 2009. Archivado desde el original el 20 de enero de 2009. Consultado el 13 de septiembre de 2017.
- ↑ «Wayback Machine». 28 de septiembre de 2007. Archivado desde el original el 28 de septiembre de 2007. Consultado el 13 de septiembre de 2017.
- ↑ «Fuel Cell Disruptor - Part 2 : EVWORLD.COM». www.evworld.com. Archivado desde el original el 25 de mayo de 2012. Consultado el 7 de marzo de 2010.
- ↑ Gutiérrez, Felipe Gato; Gutiérrez, Ángel Mario Gato (1 de noviembre de 2011). Sistemas de Aeronaves de Turbina: Tomo III. NoBooks Editorial. ISBN 9788415378433. Consultado el 20 de marzo de 2018.
- ↑ «Quiénes somos - REVE – Revista Eólica y del Vehículo Eléctrico». www.evwind.com.
- ↑ «Sion Power® Licerion® ultra-high energy density lithium rechargeable battery». Sion Power.
- ↑ «Sion Power Corporation - Advanced Energy Storage : Technology Overview». Archivado desde el original el 10 de noviembre de 2012. Consultado el 14 de agosto de 2012.
- ↑ «Excellatron». www.excellatron.com.
- ↑ «Excellatron - the Company». www.excellatron.com. Archivado desde el original el 12 de septiembre de 2012. Consultado el 9 de marzo de 2010.
- ↑ «Infinite Power Solutions - Global Energy & Technology Leader». www.infinitepowersolutions.com.
- ↑ «Firefly Energy Eyeing the Hybrid Market; Lead-Acid Foam Batteries for Mild-Hybrid Applications Heading to DOE for Testing and Validation». Green Car Congress.
- ↑ «Self rechargeable battery (flexible organic battery)». Archivado desde el original el 14 de julio de 2009. Consultado el 9 de marzo de 2010.
- ↑ «Power Paper thin and flexible batteries». Archivado desde el original el 26 de junio de 2009. Consultado el 9 de marzo de 2010.
- ↑ «Nokia patenta una batería plegable para los futuros Lumia - tuexperto.com». 9 de noviembre de 2013.
- ↑ Serpo, Alex (15 de enero de 2008). «A tenfold improvement in battery life?». News.com. CNET. Consultado el 12 de abril de 2008.
- ↑ «High-performance lithium battery anodes using silicon nanowires». Nanotechnology 3, 31 - 35 (2008). Nature. 16 de diciembre de 2007. doi:10.1038/nnano.2007.411. Archivado desde el original el 21 de marzo de 2008. Consultado el 12 de abril de 2008.
- ↑ Herald, Randy Wright - Daily. «New battery could change world, one house at a time». Archivado desde el original el 17 de octubre de 2015. Consultado el 9 de marzo de 2010.
- ↑ Cómo cargar el móvil en 20 segundos Archivado el 8 de junio de 2013 en Wayback Machine..
Enlaces externos[editar]
 Wikimedia Commons alberga una categoría multimedia sobre Batería recargable.
Wikimedia Commons alberga una categoría multimedia sobre Batería recargable.

