Ácido tetrahidrofólico
| Ácido tetrahidrofólico | ||
|---|---|---|
 | ||
| Nombre IUPAC | ||
| Ácido (2S)-2-{[4-({[(6R)-2-amino-4-oxo-1,4,5,6,7,8-hexahidropteridin-6-il]metil}amino)fenil]formamido}pentanedioico | ||
| General | ||
| Fórmula molecular |
C 19H 23N 7O 6 | |
| Identificadores | ||
| Número CAS | 29347-89-5[1] | |
| ChEBI | 20506 | |
| ChemSpider | 82572 | |
| DrugBank | DB00116 | |
| PubChem | 91443 | |
| KEGG | C00101 | |
|
O=C(O)[C@@H](NC(=O)c1ccc(cc1)NCC3N/C2=C(/N/C(=N\C2=O)N)NC3)CCC(=O)O
| ||
| Propiedades físicas | ||
| Masa molar | 445.43 g/mol g/mol | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
El ácido tetrahidrofólico, o su anión tetrahidrofolato, es un derivado del ácido fólico.
Metabolismo[editar]
Síntesis en humanos[editar]
En los seres humanos es producido a partir del ácido dihidrofólico por la enzima dihidrofolato reductasa. Esta reacción es inhibida por el metotrexato.
En un paso posterior se convierte en 5,10-metilentetrahidrofolato por la enzima serina hidroximetiltransferasa.
Síntesis bacteriana[editar]
Muchas bacterias utilizan la dihidropteroato sintetasa para producir dihidropteroato, una molécula que no tiene ninguna función en humanos. Esto la convierte en una diana terapéutica muy interesante, los antibióticos tipo sulfonamida compiten con el precursor de esta vía, el PABA.
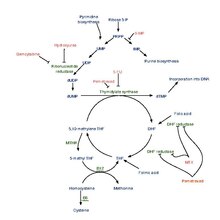
Funciones[editar]
Es cofactor en muchas reacciones biológicas, especialmente en el metabolismo de los aminoácidos y ácidos nucleicos. Actúa como donante de grupos con un solo átomo de carbono. Obtiene este átomo de carbono secuestrando el formaldehído que se produce en otros procesos metabólicos. La falta de tetrahidrofolato puede provocar anemia megaloblástica.
El metotrexato actúa sobre la dihidrofolato reductasa, al igual que la pirimetamina o el trimetoprim; como un inhibidor que reduce la cantidad de tetrahidrofolato que se produce. Esto puede provocar anemia megaloblástica.
El ácido tetrahidrofólico se encuentra involucrado en la conversión del ácido formiminoglutámico en ácido glutámico; esto puede provocar que la cantidad de histidina disponible para descarboxilación y síntesis de proteínas disminuya, y por lo tanto hacer que los niveles de histamina y ácido formiminoglutámico en orina disminuyan.[2]
Referencias[editar]
- ↑ Número CAS
- ↑ Dawson W, Maudsley DV, West GB (diciembre de 1965). «Histamine formation in guinea-pigs». J. Physiol. (Lond.) 181 (4): 801-9. PMC 1357684. PMID 5881255.
Enlaces externos[editar]

