Saxitoxina


La saxitoxina es la neurotoxina ficotoxina paralizante más conocida dentro de las producidas por varias especies de microalgas dinoflageladas de los géneros Alexandrium, Gymnodinium y Pyrodinium, y también por cianobacterias. Las algas dinoflageladas son organismos unicelulares de vida acuática que en condiciones favorables son capaces de multiplicarse rápidamente, alcanzando concentraciones de millones de células por litro de agua. En estas circunstancias, la saxitoxina que producen las algas se acumula en otros organismos marinos, principalmente moluscos bivalvos, pero también cangrejos e incluso gasterópodos y peces comedores de plancton. Los moluscos no son afectados por la saxitoxina, pero si un humano los ingiere (generalmente a través de mariscos contaminados por la proliferación de algas tóxicas) puede sufrir una intoxicación denominada intoxicación por ingestión de marisco (en inglés PSP) que puede ser muy grave.[1]
El término saxitoxina viene del nombre latino del animal del que se aisló por primera vez (Saxidomus giganteus). Este término también puede hacer referencia a todo el conjunto de neurotoxinas (conocidos colectivamente como "saxitoxinas"), en las que se incluyen: Saxitoxina pura (STX), Neosaxitoxina (NSTX), Gonyautoxinas (GTX) y Decarbamoilsaxitoxina (dcSTX).
En los últimos 20 años se ha registrado un aumento aparente de las intoxicaciones causadas por PSP. Sin embargo, aún no se sabe a ciencia cierta si el aumento es real, si puede ser la consecuencia de los progresos en la identificación, detección y de registros médicos, o si se debe a una expansión del cultivo y del consumo de mariscos. Una veintena de países cuentan con reglamentación referente a las toxinas PSP, en la mayoría de los casos referida a las toxinas PSP como un grupo.[2]
Fuentes en la naturaleza y presencia en los frutos de mar[editar]
STX es una neurotoxina producida de manera natural por ciertas especies de dinoflagelados marinos (Alexandrium sp., Gymnodinium sp., Pyrodinium sp.) y cianobacterias (Anabaena sp., algunos Aphanizomenon spp., Cylindrospermopsis sp., Lyngbya sp., Planktothrix sp.)[3][4]
Los dinoflagelados y sus quistes se han encontrado principalmente en aguas próximas a América del Norte, Europa y Japón, aunque aumentan los informes de su presencia en Asia. En el noreste de Canadá, las PSP se hallaron hace ya más de 100 años.[2]
Si bien la mayoría de las especies de mariscos que se alimentan por filtración son relativamente poco sensibles a las toxinas STX, el mecanismo y la respuesta de cada una de ellas difiere. En condiciones similares parece que, en general, los mejillones, por ejemplo, acumulan más cantidad de toxinas PSP que las ostras. En zonas templadas, los mariscos asociados a casos de PSP son mejillones, almejas y en menor proporción ostras, vieiras y berberechos.[2]
Mecanismo de acción[editar]
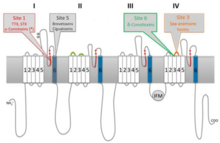
La saxitoxina es una de las toxinas naturales más potentes conocidas por el hombre. Actúa sobre los canales de sodio dependientes de voltaje de las neuronas, lo que impide la función celular normal y conduce a la parálisis.[5]
El canal de sodio dependiente de voltaje es esencial para el funcionamiento neuronal normal. Estos canales existen como proteínas integrales de membrana intercaladas a lo largo del axón de las neuronas y poseen cuatro dominios que atraviesan la membrana celular. La apertura del canal se produce cuando hay un cambio en el voltaje o algún ligando se une de forma correcta. Sin esta capacidad, la célula nerviosa se vuelve incapaz de transmitir señales y la región del cuerpo que inerva está aislada del sistema nervioso. Esto puede conducir a la parálisis de la región afectada, como en el caso de saxitoxina.
La saxitoxina se une al canal de sodio directamente en el poro de la proteína del canal de manera reversible, tapando la abertura, y evita el flujo de iones de sodio a través de la membrana.
Biosíntesis[editar]
Aunque la biosíntesis de STX parece compleja, los organismos de dos reinos diferentes (especies de dinoflagelados marinos y cianobacterias de agua dulce) son capaces de producir estas toxinas. Mientras que la teoría predominante de la producción en dinoflagelados es a través de mutualismo simbiótico con cianobacterias, la evidencia sugiere que los dinoflagelados, por sí mismos, también poseen los genes necesarios para su síntesis.[6]
La síntesis de saxitoxina constituye la primera vía de alcaloides no terpénicos descritos para bacterias, aunque el mecanismo exacto de la biosíntesis aún es un modelo teórico. El mecanismo de cómo se unen a sustratos de enzimas es todavía desconocido, y algunos de los genes implicados se han identificado recientemente mientras que otros son todavía desconocidos.[6][7]
En el pasado han sido propuestas dos biosíntesis, siendo diferentes a una propuesta más reciente de Kellmann, et.al.,[7] basada tanto en consideraciones biosintéticas como en evidencias genéticas no disponibles en el momento de las primeras propuestas.
El modelo más reciente describe un cluster de genes (SXT) utilizado para obtener una reacción más favorable. La secuencia de reacción más reciente de la saxitoxina en cianobacterias[7] es el siguiente. Consulte el diagrama de la biosíntesis detallada y estructuras intermedias.

- Se inicia con la carga de la proteína portadora de acilo (ACP) con el acetato a partir de acetil-CoA, obteniéndose el compuesto intermedio 1.
- A continuación, se sigue por una metilación catalizada por SxtA de acetil-ACP, que se convierte a continuación en propionil-ACP, obteniéndose el compuesto intermedio 2.
- Más tarde, otro SxtA realiza una reacción de condensación de Claisen entre propionil-ACP y arginina producir intermedio 4 y el intermedio 3.
- SxtG transfiere un grupo amidino de una arginina al grupo α-amino del compuesto intermedio 4 producir intermedio 5.
- El Intermedio 5 se somete a una condensación retroaldólica por medio de SxtBC, produciendo intermedio el 6.
- SxtD añade un doble enlace entre C-1 y C-5 del compuesto intermedio 6, que da lugar al cambio de 1,2-H entre C-5 y C-6 en el compuesto intermedio 7.
- SxtS realiza una epoxidación del doble enlace obteniéndose el compuesto intermedio 8, con posterior apertura del epóxido a un aldehído, formando intermedio 9.
- SxtU reduce el grupo aldehído terminal de la STX intermedia 9, formando así el intermedio 10.
- SxtIJK cataliza la transferencia de un grupo carbamoílo con el grupo hidroxilo libre en intermedia 10, formando intermedio 11.
- SxtH y SxtT, en conjunción con SxtV y la agrupación de genes SXTW, realizan una función similar que es la hidroxilación consecutivo de C-12, produciendo así la saxitoxina y terminar la ruta biosintética STX.
Toxicidad[editar]
Las dosis letales de saxitoxina en ratones han sido descritas para diferentes vías de administración: intraperitoneal (DL50 = 10 µg / kg), intravenosa (DL50 = 3,4 µg / kg) o vía oral (DL50 = 263 µg / kg). En el caso de los conejillos de indias la DL50 es similar.[8]
En humanos, la concentración causante de las intoxicaciones varía considerablemente. Se debe principalmente a diferencias de sensibilidad individuales y a oscilaciones del método de determinación. Se observaron síntomas leves con una ingesta oral entre 144 y 1 660 µg eq de STX/persona e intoxicaciones fatales por ingerir entre 456 y 12 400 µg eq de STX/persona, calculado a partir de los restos de mejillones tóxicos y considerando que estos valores pueden presentar grandes variaciones.[9] En algunos casos, la ingesta oral de 300 µg de toxinas PSP por persona causó la muerte, mientras que en otros casos se observó la ausencia de síntomas tóxicos luego de una dosis oral de 320 µg de toxinas por persona.[10]
Enfermedad en humanos[editar]
La enfermedad asociada con la ingestión de niveles dañinos de saxitoxina se conoce como intoxicación paralítica por ingestión de marisco.[11]
Los síntomas varían según la gravedad de la intoxicación. Esta está determinada por la toxicidad específica de la toxina PSP ingerida, la cantidad de alimento ingerido y la velocidad de eliminación de la o las toxinas PSP del cuerpo. Según la cantidad de alimento tóxico ingerida, los primeros síntomas pueden ocurrir en un par de minutos[9]
En casos leves, los síntomas clínicos de intoxicación con PSP incluyen una sensación de hormigueo en los labios que generalmente aparece dentro de los primeros 30 minutos. Posteriormente el hormigueo o entumecimiento se extiende progresivamente por el rostro y el cuello. Con frecuencia, el paciente experimenta una sensación de picazón en las puntas de los dedos de las manos y de los pies, cefaleas, mareos, náuseas, vómitos y diarrea. La mayoría de los síntomas aparecen rápidamente (en cuestión de horas) y pueden durar varios días.[10]
En intoxicaciones graves, la parestesia se extiende a los brazos y las piernas, que presentan también debilidad motriz. El paciente padece también vahídos y problemas para articular palabras. Con frecuencia se observa ataxia, falta de coordinación motora y dismetría. Las primeras dificultades respiratorias se manifiestan con una sensación de ahogo alrededor de la garganta. En algunos casos, entre 2 y 24 horas luego de la ingestión el paciente presenta dificultades respiratorias graves y muere por parálisis respiratoria.
Los médicos clínicos observaron que si el paciente sobrevive a las PSP durante 24 horas, ya sea con o sin respiración artificial, cuenta con excelentes probabilidades de una recuperación rápida y completa. Esto indica que la o las toxinas que causan la intoxicación por PSP o se excretan rápidamente o se metabolizan, o ambas.
Si bien la mayoría de las toxinas PSP tienen carga positiva, se absorben rápidamente a través de la mucosa gastrointestinal.
Hay algunos informes sobre la reversión de los efectos letales de la saxitoxina utilizando 4-aminopiridina,,[12][13][14] pero no hay estudios en seres humanos.
Casos en España[editar]
Desde 1976, la región de las rías de Galicia, se ha visto seriamente afectada por incidentes de PSP. Los mejillones españoles contaminados causaron intoxicación alimentaria, tanto en España, como en los países que los importaron.[15]
En 1989 se observó un aumento de las concentraciones de PSP en las escupiñas. Las autoridades sanitarias regionales decidieron establecer una veda para la recolección y venta de mariscos en razón de las concentraciones superiores a 80 µg eq de STX/100 g de carne detectadas en otras especies de moluscos (Venus verrucosa, Venerupis rhomboides, Callista chione, Acanthocardia tuberculatum) provenientes de las áreas afectadas. El incidente afectó la costa mediterránea de España entre Málaga y Algeciras, una extensión de 150 kilómetros aproximadamente.[16]
En 1993 ocurrió otro episodio en las Rías Bajas con eventos tóxicos que se extendieron durante períodos inusualmente largos con síntomas poco habituales.[17]
En 1995 y 1997 se registraron episodios esporádicos de dos o tres semanas de duración en Galicia.[18]
En 2000 ocurrieron eventos tóxicos a que resultaron en la prohibición de cosechar bivalvos en ciertas zonas de cultivo gallegas.[19]
En los meses de abril y mayo de 1995, una floración de Alexandrium minutum tiñó las aguas del puerto de Palma de Mallorca (Islas Baleares) de un color marrón rojizo poco habitual. Las muestras de poblaciones no cultivadas de moluscos bivalvos analizadas por bioensayo en ratón dieron resultados positivos. En abril de 1996 y en febrero de 1997 se observaron en esa misma área del puerto mareas rojas.[20]
En 2002, A. minutum y A. catenella provocaron eventos tóxicos de corta duración. En Andalucía, la presencia de G. catenatum determinó el cierre de ciertas zonas de cultivo, especialmente de Acanthocardia tuberculata y de vieiras.
Referencias[editar]
- ↑ Martha L. Hernández-Orozco, Ismael Gárate-Lizárraga: Síndrome de envenenamiento paralizante por consumo de moluscos. Archivado el 22 de diciembre de 2014 en Wayback Machine. Rev Biomed 2006; 17:45-60
- ↑ a b c Biotoxinas marinas - Estudio FAO:Alimentación y nutrición 80. 2004, Fao.org, (2015). [online] disponible en: http://www.fao.org/docrep/008/y5486s/y5486s00.htm [Aceso 11 Nov. 2015].
- ↑ Clark R. F., Williams S. R., Nordt S. P., Manoguerra A. S. (1999). "A review of selected seafood poisonings". Undersea Hyperb Med 26 (3): 175–84. PMID 10485519. Retrieved 2008-08-12.
- ↑ Landsberg, Jan H. (2002). "The Effects of Harmful Algal Blooms on Aquatic Organisms".Reviews in Fisheries Science 10 (2): 113–390. doi:10.1080/20026491051695.
- ↑ Huot, R. I.; Armstrong, D. L.; Chanh, T. C. (June 1989). "Protection against nerve toxicity by monoclonal antibodies to the sodium channel blocker tetrodotoxin". Journal of Clinical Investigation 83 (6): 1821–1826. doi:10.1172/JCI114087. PMC 303901.PMID 2542373.
- ↑ a b Stüken, Anke; Orr, Russell; Kellmann, Ralf; Murray, Shauna; Neilan, Brett; Jakobsen, Kjetill (18 May 2011). "Discovery of Nuclear-Encoded Genes for the Neurotoxin Saxitoxin in Dinoflagellates". PLoS One 6 (5): e20096. doi:10.1371/journal.pone.0020096. Retrieved 1 May 2015.
- ↑ a b c Kellmann, R.; Mihali, T. K.; Jeon, Y. J.; Pickford, R.; Pomati, F.; Neilan, B. A. (2008)."Biosynthetic Intermediate Analysis and Functional Homology Reveal a Saxitoxin Gene Cluster in Cyanobacteria". Applied and Environmental Microbiology 74 (13): 4044–4053.doi:10.1128/AEM.00353-08. PMC 2446512. PMID 18487408.
- ↑ Patocka J; Stredav L (April 23, 2002). Price, Richard, ed. "Brief Review of Natural Nonprotein Neurotoxins". ASA Newsletter (Applied Science and Analysis inc.) 02–2 (89): 16–23. ISSN 1057-9419. Retrieved 26 May 2012.
- ↑ a b Mons M.N., van Egmond H.P., Speijers G.J.A. Paralytic shellfish poisoning: a review. National Institute of Public Health and the Environment, 1998.
Volumen 388802005 de RIVM report - ↑ a b Biotoxinas marinas - Estudio FAO:Alimentación y nutrición 80. 2004, Fao.org, (2015). [online] disponible en: http://www.fao.org/docrep/008/y5486s/y5486s00.htm [Aceso 11 Nov. 2015].
- ↑ Clark R. F., Williams S. R., Nordt S. P., Manoguerra A. S. (1999). "A review of selected seafood poisonings". Undersea Hyperb Med 26 (3): 175–84. PMID 10485519. Retrieved 2008-08-12.
- ↑ Benton, B. J.; Keller, S. A.; Spriggs, D. L.; Capacio, B. R.; Chang, F. C. (1998). "Recovery from the lethal effects of saxitoxin: A therapeutic window for 4-aminopyridine (4-AP)". Toxicon : official journal of the International Society on Toxinology 36 (4): 571–588.doi:10.1016/s0041-0101(97)00158-x. PMID 9643470.
- ↑ Chang, F. C.; Spriggs, D. L.; Benton, B. J.; Keller, S. A.; Capacio, B. R. (1997). "4-Aminopyridine reverses saxitoxin (STX)- and tetrodotoxin (TTX)-induced cardiorespiratory depression in chronically instrumented guinea pigs". Fundamental and applied toxicology: official journal of the Society of Toxicology 38 (1): 75–88. doi:10.1006/faat.1997.2328.PMID 9268607.
- ↑ Chen, H.; Lin, C.; Wang, T. (1996). "Effects of 4-Aminopyridine on Saxitoxin Intoxication". Toxicology and Applied Pharmacology 141 (1): 44–48.doi:10.1006/taap.1996.0258. PMID 8917674.
- ↑ IPCS. 1984. International Programme on Chemical Safety. Aquatic (Marine and Freshwater) Biotoxins. Environmental Health Criteria 37. World Health Organization. ISBN 92 4 154097 4.
- ↑ Mons M.N., van Egmond H.P., Speijers G.J.A. Paralytic shellfish poisoning: a review. National Institute of Public Health and the Environment, 1998.
Volumen 388802005 de RIVM report - ↑ Gago‐Martinez A., Rodriguez‐Vazquez J.A., Thibault P., Michael A. Simultaneous occurrence of diarrhetic and paralytic shellfish poisoning toxins in Spanish mussels in 1993. Quilliam Natural Toxins, March, 1996. 10.1002/19960402NT3
- ↑ EU-NRL 1998. Minutes of the 2nd meeting of the EU National Reference Laboratories (EU-NRL) on marine biotoxins. September-October 1998. Vigo, Spain.
- ↑ EU-NRL 2001. Minutes of the 4th meeting of EU National Reference Laboratories (EU-NRL) on marine biotoxins. 29-31 October 2001. Vigo, Spain.
- ↑ Forteza, V., Quetglas, G., Delgado, M., Reyero, MI., Fraga, S., Franco, JM. & Cacho, E. Toxic Alexandrium minutum bloom in Palma de Mallorca harbour, (Balearic Islands), western mediterranean. 1998. In Reguera, B., Blanco, J., Fernandez, M. & T. Wyatt, eds. 1997. Harmful Algae, Proceedings of the VIII International Conference on Harmful Algae (June 1999, Vigo, Spain), pp. 270-273. Xunta de Galicia and IOC of UNESCO
