Lepidoptera
| Lepidópteros | ||
|---|---|---|
| Rango temporal: 199 Ma - 0 Ma Jurásico-Reciente | ||
 | ||
| Taxonomía | ||
| Reino: | Animalia | |
| Filo: | Arthropoda | |
| Subfilo: | Hexapoda | |
| Clase: | Insecta | |
| Orden: |
Lepidoptera Linnaeus, 1758 | |
| Subórdenes | ||
Los lepidópteros (Lepidoptera, del griego λεπίς, lepís, 'escama', y πτερόν, pteron, 'ala') son un orden de insectos holometábolos, casi siempre voladores, conocidos comúnmente como mariposas; las más conocidas son las mariposas diurnas, pero la mayoría de las especies son nocturnas (polillas, esfinges, pavones, etc.) y pasan muy inadvertidas. Sus larvas se conocen como orugas y se alimentan típicamente de materia vegetal, con lo que algunas especies pueden ser plagas muy dañinas para la agricultura. Muchas especies cumplen el papel de polinizadoras de plantas y cultivos.
Este taxón representa el segundo orden con más especies entre los insectos (siendo superado solamente por el orden Coleoptera); de hecho, cuenta con más de 165 000 especies[1]clasificadas en 127 familias y 46 superfamilias.[2] La mariposa diurna más grande que existe es la Ornithoptera alexandrae hembra, que puede llegar a tener 31 cm de envergadura, el macho es un poco más pequeño, vive al sudeste de Nueva Guinea. El lepidóptero más grande que la ciencia ha descubierto es la conocida mariposa Atlas o polilla Atlas (Attacus atlas), originaria de las zonas tropicales del sudeste asiático y es un heterocero (polillas o mariposas nocturnas) aunque es de hábitos diurnos.
Sistemática
[editar]Taxonomía
[editar]Hay unas ciento veintisiete familias dentro del orden Lepidoptera, pero las opiniones de cuáles son estas cambian con frecuencia entre los científicos. El tratamiento que se da aquí es el adoptado por la base de datos del Museo de Historia Natural de Londres.
Durante muchos años, el orden de los lepidópteros fue subdividido en dos subórdenes, los ropalóceros, o mariposas diurnas, y los heteróceros, polillas o mariposas nocturnas. La cladística moderna ha demostrado que esta antigua clasificación es artificial y, en la actualidad se admiten los subórdenes Aglossata, Heterobathmiina, Zeugloptera y Glossata. Los tres primeros contienen unas pocas especies, mientras que Glossata incluye el 99 % de los lepidópteros actuales.[3]
- Suborden Zeugloptera
- Suborden Aglossata
- Suborden Heterobathmiina
- Suborden Glossata
- Infraorden Heteroneura
- División Ditrysia
- División Monotrysia
- Infraorden Dacnonypha
- Infraorden Lophocoronina
- Infraorden Exoporia
- Infraorden Neopseustina
- Infraorden Heteroneura
Filogenia
[editar]Las relaciones filogenéticas de los cuatro subórdenes son las siguientes:[3]
| Lepidoptera |
| ||||||||||||||||||



Lepidópteros fósiles
[editar]Hay muy pocos fósiles de mariposas cuando se los compara con otros grupos de insectos. La distribución y abundancia de los fósiles más comunes indican que debe haber habido grandes migraciones de mariposas durante el Paleógeno en el Mar del Norte, que es donde se encuentran muchos fósiles de este grupo.[4] También se encuentran algunos fósiles en ámbar y en algunos sedimentos finos. Los restos dejados por larvas de minadores de hojas pueden ser valiosos, pero su interpretación no es fácil.[5]
Características
[editar]


Las mariposas poseen dos pares de alas membranosas cubiertas de escamas coloreadas, que utilizan en la termorregulación, el cortejo y la señalización. Su aparato bucal es de tipo probóscide provisto de una larga trompa que se enrolla en espiral (espiritrompa) que permanece enrollada en estado de reposo y que les sirve para libar el néctar de las flores que polinizan.
El cortejo de los machos es muy variable en las diferentes familias del orden, pero básicamente consiste en exhibiciones y en la producción de feromonas sexuales. Con las maniobras de vuelo, los machos cubren a las hembras con el olor de estas feromonas. Tras el apareamiento, los machos pueden evitar que la hembra tenga una nueva cópula taponando su genitalia con una secreción pegajosa.
Su desarrollo es holometábolo: del huevo sale una larva u oruga que se transformará en pupa y esta dará lugar al adulto. La larva, a diferencia del adulto, presenta un aparato bucal de tipo masticador; la mayoría de las larvas son fitófagas. En menos del 1 % las larvas son carnívoras o aun caníbales. Podemos distinguir las larvas de lepidópteros de las de otros insectos porque poseen una serie de cinco patas falsas —las de los himenópteros sínfitos poseen siete o más— al final del abdomen,[6] lo que en algunos casos conlleva que su forma de caminar sea como la de un acordeón abriéndose y cerrándose alternativamente. Los lepidópteros son insectos terrestres y solo ocasionalmente algunas larvas son acuáticas.
Coloración
[editar]En el orden Lepidoptera la coloración, especialmente la de las alas, alcanza la máxima especialización. Morfológicamente, la superficie alar está recubierta de escamas cuya superficie posee multitud de aristas longitudinales (separadas a veces a menos de 1 μm, es decir, la milésima parte de un milímetro) que alteran la reflexión de la luz produciendo colores muy llamativos y frecuentemente tornasolados e iridiscentes.[2]

Venación alar
[editar]
Las venas de las alas de las mariposas forman un diseño característico y único según las especies o familias de las que se trate. Conocer este patrón es, en algunos casos, imprescindible para la correcta determinación de una especie concreta de mariposa. Para poder describir con claridad y precisión este diseño se utiliza la siguiente terminología entomológica:[7][8]
- Tanto en las alas anteriores como en las posteriores se encuentran las siguientes zonas o áreas: basal, es la más próxima al cuerpo, subdividida a veces en basal y postbasal; submarginal, premarginal o, simplemente, marginal, es la más alejada. Entre ambas se encuentra la zona discal que, a su vez, se divide en discal y postdiscal o postmedial. Finalmente, la zona apical se encuentra en la parte distal y superior de ambas alas.
- En el perímetro del ala anterior se encuentra el borde de ataque que se denomina costa o borde costal. A continuación, el ápice seguido del margen externo o termen. Inmediatamente después, en las alas anteriores aparece el ángulo dorsal y, en las posteriores, el ángulo anal. Se completa la periferia del ala con el margen interno o dorso.
- Entre las zonas basal y discal de ambas alas, próxima a la costa, aparece un área alargada, enmarcada por venas y casi siempre cerrada, denominada célula o celda discal, discoidal, discocelular, o, simplemente, celda. En su parte superior se encuentra delimitada por la vena subcostal, por la parte inferior por la vena mediana, y por la postdiscal por las tres venas discoidales. Cuando falta alguna de estas venas, se denomina celda abierta.
- Las venas no son siempre fáciles de observar, a veces es mejor observarlas desde el reverso o emplear técnicas de humidificación con alcohol para que se hagan visibles entre las escamas y pelos androconiales. Las del ala anterior se numeran de la 1 a la 12 (V1, V2, …, V12), de abajo arriba. La vena V1 o submediana, de las más difíciles de apreciar, nace en la base y discurre de forma paralela al dorso. La V2 o mediana arranca hacia la mitad del borde inferior de la celda. La vena V12 o costal nace en la base del ala y discurre paralela a la costa. Las del ala posterior son 8, aunque muchas veces aparecen dos venas anales V1, V1a y V1b. También se numeran de abajo arriba, siendo la V8 la vena costal. En algunas mariposas pueden faltar venas, tanto de un ala como de la otra, normalmente entre la V6 y la V9. En esos casos se numeran de forma sucesiva, de tal manera que puede haber mariposas en las que la última vena sea la V9.
- Entre las venas aparecen los espacios llamados células que también están numerados. Así, entre el dorso y V1 se encuentra la célula E1a; entre V1 y V2 aparece E1b; entre V2 y V3 E2; y así sucesivamente hasta llegar a E12 en el ala anterior, y E8 en la posterior, entre la última vena y la costa. Como en el caso de las venas, la numeración siempre es correlativa, pudiendo acabar en E9.
Patrón de formación en el color
[editar]El ala de la mariposa se desarrolla en la larva como una bolsa epidermal (disco imaginal) la cual se invagina en la metamorfosis para formar un ala inmóvil durante el estado de pupa. Las escamas pigmentadas son secretadas en el estadio tardío de la pupa, pero la interacción epidermal de la célula se determina en estadios más tempranos y determina el color de la escama definiendo el patrón en el adulto. Por su parte la mancha ocular es especificada a partir de una señalización en la región central (French, 1997). Por otro lado se cree que el patrón de coloración se organiza alrededor de un foco hipotético y que este sirve como fuente de información para la posición y síntesis del pigmento apropiado. El patrón específico aparece por las variaciones en el número de focos en el ala y la variación en la que la información de la posición es interpretada.[9]
En otro estudio se evidenció la existencia de un foco que determina el largo de la mancha ocular en el ala posterior de Precis coenia. Al cauterizar trescientas células en el centro de la supuesta mancha ocular en el desarrollo temprano del ala, puede inhibirse completamente el desarrollo de este. Estas mismas células pueden ser trasplantadas a otra región del ala e inducir un pigmento en forma de anillo en el tejido alrededor del injerto. Este estudio demostró que el foco es una entidad fisiológica.[10]
En estudios histológicos en el epitelio del ala se reveló que la formación de las escamas siempre ocurre en filas paralelas, próximas al eje del ala. Esta formación celular de las alas parece estar formada por diferenciación in situ y no por migración. Los pigmentos que generan el patrón de coloración en las alas son sintetizados exclusivamente en las escamas. Este patrón es formado por cuatro colores de melanina diferentes; las enzimas específicas para la síntesis de esta son incorporadas en formas insolubles en la cutícula de las escamas. La síntesis de estos pigmentos comienzan cuando el sustrato de melanización comienza a ser suministrado por el sistema circulatorio.[11]
Finalmente se ha encontrado que la expresión de genes homólogos en el patrón de apéndices de Drosophila también están involucrados en el patrón de coloración. El gen angrailed es expresado en la parte posterior y apterous en la superficie dorsal del disco del ala. Por su parte wingless es expresada alrededor de la margen dorso-ventral en el disco del ala. La proteína Wg junto con el gen Decapentaplegic han mostrado tener una función como gradiente de morfógenos en Drosophila controlando la expresión génica y consecuentemente el patrón morfológico en los ejes dorso-vetral y antero-posterior.[12]

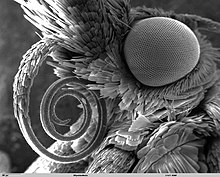
Alimentación
[editar]Las orugas se alimentan de la materia vegetal que las rodea: hojas, flores, frutos, tallos, raíces, lo que les da gran importancia agrícola al constituir plagas importantes de cultivos. Algunas especies son especializadas en una o unas pocas especies relacionadas, otras son polífagas, pueden alimentarse de una gran variedad de plantas de diferentes familias.[13] Algunas especies son capaces de minar (generar túneles) en las superficies de las que se alimentan. Otras, en cambio, aprovechan las manufacturas humanas, o bien productos almacenados (harinas, granos, …).
Un pequeño número de especies son carnívoras. Son de destacar las familias Epipyropidae y Lycaenidae.[14][15]
Los adultos, a excepción de los representantes de la familia Micropterigidae (cuya alimentación, derivada de su capacidad masticatoria, abarca a polen, esporas de hongos, etc.), se alimentan libando, es decir, absorbiendo néctar u otras sustancias líquidas mediante su aparato bucal lamedor-chupador (espiritrompa). No obstante, existen especies cuyo ciclo vital exige una corta fase de imago: en estos casos, el adulto ni se alimenta, sino que destina todas sus energías a la reproducción.[2]




Ciclo de vida
[editar]Reproducción y desarrollo
[editar]Los lepidópteros son insectos holometábolos, es decir que tienen metamorfosis completa y pasan por los estadios: huevo, larva, pupa y adulto o imago. La gran mayoría de las mariposas son herbívoras, es decir que se alimentan de plantas. Solo unas pocas especies son carnívoras o comen lana u otros materiales.[16]
Huevo
[editar]La mayoría de los lepidópteros son ovíparos, aunque algunos pocos son ovovivíparos. La hembra puede colocar el huevo en una variedad de sustratos. Algunas especies ponen los huevos al vuelo. En este caso se trata de especies que pueden alimentarse de una gran variedad de plantas (polífagas).[17] Las especies más especializadas depositan los huevos en o cerca de la planta hospedera. Algunas especies depositan huevos aislados, otras lo hacen en masas.[18] Las hembras seleccionan las plantas huéspedes por instinto, usando, principalmente señales química u odoríferas.[19]: 564
El estadio de huevo puede durar unas semanas o menos; en otros casos, el huevo entra en diapausa durante el invierno y la larva emerge recién la primavera siguiente.
Larva u oruga
[editar]Nacen como larvas semejantes a gusanos, llamadas orugas.[20] El cuerpo consiste de trece segmentos, tres torácicos y diez abdominales.[21]
La mayoría de las especies se alimentan de las hojas, tallos u otras partes de las plantas a la vez que crecen rápidamente. Muchas especies requieren una o unas pocas especies de plantas para su alimentación, y la extinción de una planta puede arrastrar la de una especie de mariposa. Otras especies se alimentan de una gran variedad de plantas de diferentes familias, son polífagas. Aun otras (muy pocas) son carnívoras o detritivoras.[22][23]
Pupa
[editar]Al completar el desarrollo, la oruga se protege en un lugar resguardado y allí se transforma en pupa. La pupa puede estar envuelta en un capullo de seda, como en la mayoría de las mariposas nocturnas, o carecer de esta envoltura, como en las mariposas diurnas. En este estadio no se alimenta, y sufre grandes cambios metabólicos y morfológicos, cuyo conjunto es llamado metamorfosis. La mariposa adulta sale rompiendo el esqueleto externo de la crisálida.
Adulto o imago
[editar]

La mayoría de las mariposas adultas se alimentan libando el néctar de las flores con su espiritrompa, una estructura bucal extensible evolucionada a partir de algunas de las piezas bucales articuladas típicas de los insectos. Los adultos de unas pocas especies tienen una vida muy corta, carecen de piezas bucales y no se alimentan.
Esta "lengua enrollada" es flexible y muy sensible. Puede introducirse dentro de una flor, pero también puede inclinarse abruptamente, de manera que la mariposa puede alimentarse desde diferentes ángulos sin tener que moverse. Una vez que la mariposa ha terminado de alimentarse, la lengua se retrae enroscándose y encaja exactamente debajo de la cabeza del insecto. Machos y hembras se buscan activamente, usando como guía visual su aleteo característico, y empleando el sentido del olfato. Tras la fecundación, la hembra pone varios cientos o miles de huevos. En algunos casos la vida adulta es breve, no durando más que el tiempo necesario (a veces un solo día) para asegurar la reproducción.
Migración
[editar]Algunas especies son migratorias. Entre ellas algunas se cuentan entre los insectos que cubren las mayores distancias en sus viajes.[24][25][26]
Entre las especies migratorias mejor conocidas se cuentan la mariposa monarca (Danaus plexippus plexippus), el esfíngido picaflor (Macroglossum stellatarum), la vanesa de los cardos (Vanessa cardui), el almirante rojo (Vanessa atalanta) y Colias croceus. Otro ejemplo es Urania fulgens que puede tener migraciones explosivas en ciertos años en el Neotrópico.[27]
Véase también
[editar]- Diferencias entre mariposas diurnas y nocturnas
- Mariposas de la península ibérica
- Fisiología (insectos)
Referencias
[editar]- ↑ «¿Cuántos insectos existen en la península Ibérica?». Consultado el 21 de octubre de 2016.
- ↑ a b c de Viedma, M. G., Baragaño, J. R. & Notario, A. 1985. Introducción a la entomología. Ed. Alhambra. ISBN 84-205-1031-9
- ↑ a b Scoble, M. J. (1995). The Lepidoptera, form, function and diversity. London: The Natural history Museum & Oxford University Press. ISBN 0-19-854952-0
- ↑ Rust, Jest (2000). «Palaeontology: Fossil record of mass moth migration». Nature 405 (6786): 530-531. PMID 10850702. doi:10.1038/35014733.
- ↑ Grimaldi, D.; Engel, M. S. (2005). Evolution of the Insects. Cambridge University Press. ISBN 0-521-82149-5.
- ↑ Aguado Martín, L. O. (2007), p. 52
- ↑ Aguado Martín, L. O. (2007). Capítulo 3 Anatomía del imago, p. 79
- ↑ Higgins, L. G. y N. D. Riley (1980), p. 15
- ↑ Otaki, J. M. (1998). "Color-pattern modifications of butterfly wings induced by transfusion and oxyanions". Journal of Insect Phisiology 44(12): 1181-1190.
- ↑ Nijhout, F. (1980). "Ontogeny of the color pattern on the wings of Precis coenia (Lepidoptera: Nymphalidae)". Developmental Biology 80(2)
- ↑ Nijhout, F. (1980). "Pattern formation on lepidopteran wings: Determination of an eyespot Developmental Biology". Developmental Biology 80(2): 267-274.
- ↑ French, V. (1997). "Pattern formation in colour on butterfly wings". Current Opinion in Genetics & Development 7(4): 524-529
- ↑ Bastidas, Rodolfo y Zavala, Yanet. 1995. Principios de Entomología Agrícola. Ediciones Sol de Barro. ISBN 980-245-006-5
- ↑ Moisset, B. Bugguide.net. Carnivorous Lepidoptera
- ↑ Rubinoff, Daniel; Haines, William P. (2005). «Web-spinning caterpillar stalks snails». Science 309 (5734): 575. PMID 16040699. doi:10.1126/science.1110397.
- ↑ Carnivorous Lepidoptera. Bugguide.net
- ↑ Wiklund, Christer (July 1984). «Egg-laying patterns in butterflies in relation to their phenology and the visual apparency and abundance of their host plants». Oecologia 63 (1): 23-29. Bibcode:1984Oecol..63...23W. PMID 28311161. S2CID 29210301. doi:10.1007/BF00379780.
- ↑ Gullan, P. J.; P. S. Cranston (13 de septiembre de 2004). «7». The insects: an outline of entomology (3 edición). Wiley-Blackwell. pp. 198–199. ISBN 978-1-4051-1113-3.
- ↑ Resh, Vincent H.; Ring T. Carde (1 de julio de 2009). Encyclopedia of Insects (2 edición). U. S. A.: Academic Press. ISBN 978-0-12-374144-8.
- ↑ Gullan, P. J.; Cranston, P. S. (2010). «Life-history patterns and phases». The Insects: an Outline of Entomology (4th edición). Wiley-Blackwell. pp. 156–164. ISBN 978-1-4443-3036-6.
- ↑ Triplehorn, Charles A.; Johnson, Norman F. (2005). Borror and Delong's Introduction to the Study of Insects. Belmont, California: Thomson Brooks/Cole. ISBN 978-0-03-096835-8.
- ↑ Bugguide.net. Carnivorous Lepidoptera
- ↑ Dugdale, J. S. (1996). «Natural history and identification of litter-feeding Lepidoptera larvae (Insecta) in beech forests, Orongorongo Valley, New Zealand, with especial reference to the diet of mice (Mus musculus)». Journal of the Royal Society of New Zealand 26 (4): 251-274. doi:10.1080/03014223.1996.9517513. Consultado el 14 de noviembre de 2010.Uso incorrecto de la plantilla enlace roto (enlace roto disponible en Internet Archive; véase el historial, la primera versión y la última).
- ↑ Scoble, MJ. (1995) "Migration" in The Lepidoptera: form, function and diversity. 68-71. Previewed in Google Books [1] on 09 Oct 2009.
- ↑ Meerman, J.C. (1987) "Dutch Sphingidae" Wet. meded. KNNV 180.
- ↑ Species composition and dynamics in abundance of migrant and sedentary butterflies (Lepidoptera) at Gibraltar during the spring period
- ↑ Smith, N. G. (1983). Janzen, D. H., ed. Urania fulgens (Calipato Verde, Green Urania). Costa Rican Natural History. Chicago: University of Chicago Press. p. 816.
Bibliografía
[editar]- Aguado Martín, L. O. (2007). Las mariposas diurnas de Castilla y León (Lepidópteros ropalóceros) Especies, biología, distribución y conservación I. Valladolid: Junta de Castilla y León. p. 1041. ISBN 978-84-9718-473-1.
- Arnett, R. H. Jr. (2000) Segunda edición. American insects. CRC Press, Boca Ratón, Londres, New York, Washington, D. C. ISBN 0-8493-0212-9
- Borror, D. J., DeLong, D. M., Triplehorn, C. A.(1976) cuarta edición. An introduction to the study of insects. Holt, Rinehart and Winston. New York, Chicago. ISBN 0-03-088406-3
- Higgins, L. G. y N. D. Riley (1980). Guía de campo de las mariposas de España y Europa. Barcelona: Omega. p. 452. ISBN 84-282-0327-X.
Enlaces externos
[editar]- European Butterflies and Moths. European Butterflies and Moths.
- Natural History Museum. Lista de Lepidoptera del mundo
- Bugguide. Universidad Estatal de Iowa
- Mariposario Mariposario de Chapultepec
- Mariposario Mariposario NY
- Historic Moth illustrations
- «Lepidoptera (TSN 117232)». Sistema Integrado de Información Taxonómica (en inglés).
- Caught Between the Pages: Treasures from the Franclemont Collection Colección virtual de Lepidoptera de la Biblioteca Entomológica Comstock de la Universidad Cornell
- Japmoth Lepidoptera del Japón.
- Insect Life Forms Orden Lepidoptera
