Ácido escuárico
| ácido escuárico | ||
|---|---|---|
 | ||
| Nombre IUPAC | ||
| 3,4-Dihidroxiciclobut-3-en-1,2-diona | ||
| General | ||
| Otros nombres | ácido cuadrático, 3,4-Dihidroxi-3-ciclobuteno-1,2-diona | |
| Fórmula semidesarrollada | C4H2O4 | |
| Fórmula estructural |
 | |
| Fórmula molecular | ? | |
| Identificadores | ||
| Número CAS | 2892-51-5[1] | |
| Número RTECS | GU1800000 | |
| ChEBI | 52141 | |
| ChemSpider | 16919 | |
| PubChem | 17913 | |
| UNII | SVR9D0VODW | |
| Propiedades físicas | ||
| Apariencia | polvo blanco cristalino | |
| Masa molar | 11 406 g/mol | |
| Peligrosidad | ||
| Frases R | R36/R37/R38/R43 | |
| Frases S | S26/S36 | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
El ácido escuárico, también llamado ácido cuadrático debido a que sus cuatro átomos de carbono forman aproximadamente un cuadrado, es un compuesto orgánico con fórmula química C4H2O4. Es uno de los ácidos oxocarbónicos (ácidos que tienen un anión oxocarbono como su base conjugada). El ácido escuárico es usado también para sintetizar tintes de escuareína fotosensibles, e inhibidores de protein tirosin fosfatasa.
Propiedades químicas
[editar]La estructura del ácido escuárico no es un cuadrado perfecto, puesto que la longitud de los enlaces carbono-carbono no es exactamente igual.
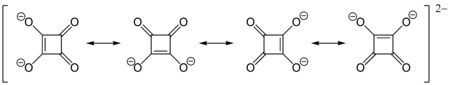
La alta acidez con pKa = 1,5 para el primer protón, y pKa = 3,4 para el segundo es atribuible a la estabilización por resonancia del anión.[2] Debido a que la carga negativa está distribuida por igual en los cuatro átomos de oxígeno, el dianión del ácido escuárico es completamente simétrico (a diferencia del ácido escuárico mismo) con todas las longitudes de enlace C-C y C-O idénticas.
Otra descripción, mecánica cuántica, es colocar ambos electrones π de los átomos de oxígeno enlazados doblemente en un anión en los átomos de oxígeno. Esto resultará en una carga negativa en dichos átomos, pero también en una doble carga positiva en el anillo de átomos de carbono. De esta forma, satisface la regla de Hückel (2 electrones π = 4n + 2, con n = 0) con respecto a la aromaticidad. La simetría total del dianión es una consecuencia de la distribución de carga y la aromaticidad.
Síntesis
[editar]La síntesis original empezaba con la reacción del 1-cloro-1,2,2-trifluoroetileno con zinc para producir perfluorociclobuteno. Este compuesto fue convertido a 1,2-dietoxi-3,3,4,4-tetrafluoro-1-ciclobuteno con etanol. La hidrólisis da el ácido escuárico.[3]
Usos médicos
[editar]Médicamente, puede ser usado para el tratamiento de verrugas. También es usada para la alopecia areata o alopecia totalis/universalis (caída del cabello autoinmune) a través de inmunoterapia tópica que involucre la producción de alérgenos.[4]
Véase también
[editar]Referencias
[editar]- ↑ Número CAS
- ↑ New Aromatic Anions. III. Molecular Orbital Calculations on Oxygenated Anions Robert West, David L. Powell J. Am. Chem. Soc.; 1963; 85(17); 2577-2579.
- ↑ J. D. Park, S. Cohen, and J. R. Lacher (1962). «Hydrolysis Reactions of Halogenated Cyclobutene Ethers: Synthesis of Diketocyclobutenediol». J. Am. Chem. Soc. 84 (15): 2919-2922. doi:10.1021/ja00874a015.
- ↑ A. M. Holzer, L. L. Kaplan, W. R. Levis (2006). «Haptens as drugs: contact allergens are powerful topical immunomodulators». J. Drugs. Dermatol. 5 (5): 410-416. PMID 16703776.