Serina proteasa
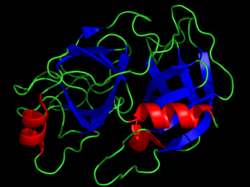
Las proteasas de serina son hidrolasas que degradan enlaces peptídicos de péptidos y proteínas y que poseen en su centro activo un aminoácido serina esencial para la catálisis enzimática. Esta clase de enzimas (clasificadas como EC|3.4.21.) incluye a la tripsina, quimotripsina, subtilisina granzima y otras.
Las serina proteasas cortan la cadena polipeptídica en el lado carboxilo de aminoácidos específicos, esto es, reconocen secuencias en la estructura primaria. Por ejemplo, la tripsina corta en el lado carboxilato de los residuos básicos como la lisina o la arginina, mientras que la quimiotripsina lo hace junto a residuos hidrófobos, como la fenilalanina.
Existe una cierta homogeneidad estructural en cuanto a conformación estructural de las serina proteasas, lo que sugiere una relación evolutiva entre ellas. Por ejemplo, las serina proteasas siempre poseen una tríada catalítica de aspartato, histidina y serina ubicadas en la grieta catalíca del sitio activo. Además, estas enzimas siempre poseen un «bolsillo» situado cerca de la serina del lugar activo. En el caso de la tripsina, este bolsillo le permite captar y mantener aminoácidos básicos (cargados positivamente), gracias a que la enzima posee en ese lugar el grupo carboxilo de la cadena lateral de un ácido aspártico; es decir, la presencia de un residuo ácido en el bolsillo es el que confiere su especificidad a la tripsina, la afinidad hacia el corte en aminoácidos básicos de las proteínas diana, aminoácidos que interactúan mediante interacción electrostática con el grupo ácido del bolsillo.
Enlaces externos
Listado sistemático de las Proteasas de Serina en la página de ExPassy (en inglés)
Referencias
- Mathews, C. K.; Van Holde, K.E et Ahern, K.G (2003). Bioquímica (3 edición). ISBN 84-7892-053-2.
