Reacción de Michael
La reacción de Michael o adición de Michael consiste en una adición nucleófila de un carbanión a un compuesto carbonílico α,β-insaturado. Pertenece a la clase más grande de las adiciones conjugadas. Es uno de los métodos más útiles de formación de enlaces C-C en condiciones suaves. Existen muchas variantes asimétricas.[1][2]
En este esquema los sustituyentes R y R' en el nucleófilo son grupos electroaceptores tales como los acilo y ciano convirtiendo al hidrógeno metilénico en ácido, que al reaccionar con la base B: da lugar al carbanión. El sustituyente en el alqueno activado es normalmente una cetona, lo que la convierte en una enona, pero puede ser también un grupo nitro.
Definición[editar]
Tal como fue definida originalmente por Michael,[3] la reacción es una adición de un enolato de una cetona o aldehído sobre el carbono β de un compuesto carbonílico α,β-insaturado (el "aceptor" de Michael). Una definición posterior, propuesta por Kohler,[4] es la adición 1,4 de un carbono nucleófilo doblemente estabilizado a un compuesto carbonílico α,β-insaturado. Algunos ejemplos de nucleófilos incluyen a beta-cetoesteres, malonatos y beta-cianoesteres. El producto resultante contiene un altamente útil patrón de dos carbonilos (C=O) en 1,5.
Mecanismo[editar]
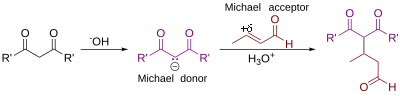
El mecanismo de reacción es esbozado a continuación con un compuesto 1,3-dicarbonilo 1, (siendo p.ej. R un residuo alcoxi), como nucleófilo:
La desprotonación de 1 por la base conduce al carbanión 2 estabilizado por sus grupos electroaceptores. Las estructuras 2A, 2B y 2C son tres estructuras de resonancia que pueden ser dibujadas para esta especie, dos de las cuales son iones enolato (2B y 2C). Este nucleófilo reacciona con el alqueno eletrofílico 3 dando 4 en una reacción de adición conjugada. La abstracción del protón de la base protonada (o del solvente) por el enolato conduce al producto 5, siendo este el paso final.
Referencias[editar]
- ↑ http://www.chem.ucalgary.ca/courses/351/Carey5th/Ch18/ch18-4-3.html.
- ↑ Clayden et al, Organic Chemistry
- ↑ Michael, Arthur. J. Prakt. Chem. 1887, 36, 349-356; ibid.,1894, 49, 20
- ↑ Kohler. (J. Am. Chem. Soc., 1907, 37, 385; ibid., 1935, 57, 1316.
Bibliografía[editar]
- K. Peter C. Vollhardt (1994). Química Orgánica. Barcelona: Ediciones Omega S.A. ISBN 84-282-0882-4.
- W.R. Peterson (1996). Formulación y nomenclatura química orgánica. Barcelona: EDUNSA - Ediciones y distribuciones universitarias S.A. ISBN 84-85257-03-0.