Reacción de Cannizzaro
La reacción de Cannizzaro, llamada así por su inventor Stanislao Cannizzaro, es una reacción química que consiste en la dismutación de un aldehído sin hidrógeno en alfa (no enolizable) catalizado por una base.[1][2] Esta transformación fue llevada a cabo por Cannizzaro en 1853, cuando al tratar benzaldehído con hidróxido de potasio obtuvo alcohol bencílico y ácido benzoico.


El producto de oxidación es ácido carboxílico y el producto de reducción-oxidación es un alcohol. Si el aldehído fuera enolizable, i.e. RCHR'CHO, tendría lugar la condensación aldólica, debido a la desprotonación del hidrógeno en alfa. Ver los siguientes reviews.[3]
Mecanismos de reacción[editar]
La primera etapa consiste en una adición nucleófila de la base (el anión hidróxido) al carbono carbonílico del aldehído. El alcóxido resultante desprotona para dar un di-anion, conocido como Intermedio de Cannizzaro. Para que este intermedio se forme se requiere un medio fuertemente básico. Este es un proceso de auto oxidación-reducción en el cual los alcoholes son el resultado de la reducción y las sales del ácido carboxílico de la oxidación.
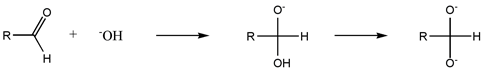
Ambos intermedios pueden bien reaccionar con el aldehído o transferir un hidruro, H−. La negatividad de este C-H se ve aumentada por el carácter electro-donante del oxígeno en alfa. Esta transferencia de hidruro genera simultáneamente un anión alcóxido (RCH2O-) y un ácido carboxílico, que desprotona rápidamente para formar el carboxilato. Evidencias adicionales del carácter de hidruro del intermedio de la reacción de Cannizzaro se encuentran en la formación de H2 al hacerlo reaccionar con agua.

Solo los aldehídos que no pueden formar un enolato dan la reacción de Cannizzaro. Porque en las condiciones (básicas) de esta reacción los aldehídos que pueden formar un enolato reaccionan vía condensación aldólica. Ejemplos de aldehídos que pueden reaccionar vía Cannizzaro son formaldehído y aldehídos aromáticos como el benzaldehído.
Procedimiento[editar]
En un matraz erlenmeyer de 250 ml se colocan 10 ml (10.4 g, 98 mmol) de benzaldehído y 9 g de NaOH disueltos en 5 ml de agua. Tapar con un tapón firmemente, y agitar vigorosamente hasta que aparezcan un producto sólido y un líquido incoloro. Adicionar agua suficiente para disolver el sólido (benzoato sódico) pero evitar un exceso. Llevar la disolución a un embudo de decantación, lavar el matraz con unos mililitros de cloruro de metileno y extraer la solución con tres porciones de 15 ml de cloruro de metileno. Guardar ambas fases. Reunir los extractos orgánicos y lavarlos con NaHS03 al 10 % (2 x 20 ml) y conNa2CO3al 10 % (1 x 20 ml). Secar sobre Na2SO4anhidro, filtrar y evaporar en rotavapor. Destilar a vacío. Calcular el rendimiento en alcohol. La capa acuosa alcalina de la primera extracción se acidifica con HCI, precipitando el ácido benzoico como una masa blanca. Enfriar la mezcla, filtrar por succión y lavar con agua. Llevar el ácido benzoico a un vaso y añadir agua y calentar hasta disolución del producto. filtrar en caliente con filtro de pliegues. Enfriar y filtrar por succión, secando concorriente de aire durante un rato.
Variaciones[editar]
Se ha descrito una versión sin disolvente que se basa en el uso de 2-chlorobenzaldehído con hidróxido potásico en un mortero:[4]
Referencias[editar]
- ↑ Cannizzaro, S. (1853). «Ueber den der Benzoësäure entsprechenden Alkohol». Liebigs Annalen 88: 129-130. doi:10.1002/jlac.18530880114.
- ↑ List, K.; Limpricht, H. (1854). «Ueber das sogenannte Benzoëoxyd und einige andere gepaarte Verbindungen». Liebigs Annalen 90 (2): 190-210. doi:10.1002/jlac.18540900211.
- ↑ Geissman, T. A. Org. React. 1944, 2, 94. (Review)
- ↑ A Facile Solvent-Free Cannizzaro Reaction Phonchaiya, Sonthi; Panijpan, Bhinyo Rajviroongit, Shuleewan; Wright, Tony; Blanchfield, Joanne T. J. Chem. Educ. 2009, 86, 85.

