Nitróxido

Un óxido de amina, también conocido como amina-N-óxido y nitróxido es un compuesto orgánico que contiene el grupo funcional R3N+-O−, un enlace N-O con tres enlaces adicionales a hidrógeno o a cadenas laterales de hidrocarburos unidos al nitrógeno. A veces se escribe como R3N→O.
En sentido estricto, el término óxido de amina sólo se aplica a óxidos de aminas terciarias. A veces se usa también para derivados análogos de aminas primarias y secundarias.
Ejemplos de óxidos de amina incluyen el N-óxido de piridina, un sólido cristalino soluble en agua con un punto de fusión de 62-67 °C y el N-óxido de N-metilmorfolina, que es un oxidante.
Propiedades[editar]
Los nitróxidos se usan como grupo protector para aminas e intermedios de síntesis. Los óxidos de amina de cadenas alquílicas largas se usan como surfactantes no iónicos y como estabilizadores de espumas.
Las aminas-N-óxido son moléculas altamente polares, con una polarizabilidad cercana a las de las sales de amonio cuaternario. Los nitróxidos pequeños son muy hidrofílicos y tienen una solubilidad acuosa excelente, acompañada de una solubilidad muy baja en la mayoría de disolventes orgánicos.
Los nitróxidos son bases débiles, con constantes de disociación pKa de alrededor de 4,5 , que resultan en hidroxilaminas catiónicas R3N+-OH cuando se protonan a pH inferior a su pKa.
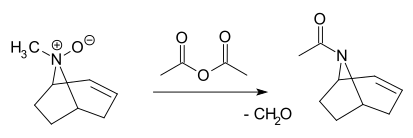
En la reacción de Polonovski un N-óxido terciario se rompe por la acción de anhídrido acético a su acetamida correspondiente y un aldehído:[1][2][3]
Referencias[editar]
- ↑ Grierson, D. Org. React. 1990, 39, 85. (doi: 10.1002/0471264180.or039.02)
- ↑ M. Polonovski, M. Polonovski, Bull. Soc. Chim. France 41, 1190 (1927).
- ↑ Strategic Applications of Named Reactions in Organic Synthesis (Paperback) by Laszlo Kurti, Barbara Czako ISBN 0-12-429785-4
Enlaces externos[editar]
- Chemistry of amine oxides
- Surfactants, types and uses Archivado el 31 de julio de 2020 en Wayback Machine. (pdf)
- The amine oxides homepage
- Nomenclature of nitrogen compounds
- IUPAC definition (pdf)