Nailon
| Densidad | 1150 kg/m³ |
| Conductividad eléctrica(σ) | 10-12 (m·ohm)-1 |
| Conductividad térmica | 0,25 W/(m·K) |
El nailon[1] o nilón[2] (grafías en español del nombre comercial Nylon, marca registrada)[3] es un polímero sintético que pertenece al grupo de las poliamidas. El nailon es una fibra textil elástica y muy resistente, no lo ataca la polilla, no precisa planchado y se utiliza en la confección de medias, tejidos y telas de punto, cerdas, sedales y redes de pesca. El nailon moldeado se utiliza como material duro en la fabricación de diversos utensilios, como mangos de cepillos, peines, etc.
El descubridor del nailon y quien lo patentó por primera vez fue Wallace Hume Carothers. Lo descubrió en 1933,[4] pero no lo patentó hasta el 20 de septiembre de 1938 (patentes 2130523, 2130947 y 2130948 de los EE. UU.). A la muerte de Carothers, la empresa DuPont conservó la patente. Los Laboratorios DuPont, en 1938, produjeron esta fibra sintética fuerte y elástica, que reemplazaría en parte a la seda y el rayón.
Con este invento se revolucionó en 1938 el mercado de las medias, con la fabricación de las medias de nailon, pero pronto se hicieron muy difíciles de conseguir, porque al año siguiente los Estados Unidos entraron en la Segunda Guerra Mundial y el nailon fue necesario para hacer material de guerra, como cuerdas y paracaídas. Pero antes de las medias o de los paracaídas, el primer producto de nailon fue el cepillo de dientes con cerdas de nailon. Las primeras partidas llegaron a Europa en 1945.
Etimología[editar]
Son varias las interpretaciones del nombre. Una de ellas es que es un juego de palabras, haciendo referencia a NY (Nueva York) y Lon (Londres), dos ciudades que conjugadas en idioma inglés dan como resultado NyLon, ya que lo descubrirían dos investigadores que vivían uno en cada ciudad y registraron las patentes casi al mismo tiempo.
Según John W. Eckelberry (DuPont),[cita requerida] "nyl" fue una sílaba elegida al azar y "on", en inglés, es un sufijo usado en muchas fibras.
Otra es que cuando se realizaban los envíos desde Nueva York (NY) a Londres (LON), aparecían las iniciales de las ciudades en las hojas de envío y era más fácil de identificar para los trabajadores de los puertos como NY-LON que con su nombre real.
Otra más es que son las iniciales de los nombres de las esposas de los investigadores que descubrieron la fibra: Norma, Yolanda, Laura, Olaya y Natalia.[5]
Otra versión dice que el nombre debería haber sido “no-run”, indicando que las medias hechas por este material no se rompían con facilidad pero por razones jurídicas fue cambiado a Nylon.
Otra leyenda atribuye el nombre a abreviaciones de exclamaciones como «Now You Lousy Old Nipponese» (o «Now You Look Old Nippon» o «Now You Lose Old Nippon») en contra de los japoneses al tratarse de un sustituto de la seda que se había importado de China ocupada por los japoneses en la Segunda Guerra Mundial.
Propiedades[editar]
Durante la fabricación las fibras de nailon se someten a extrusión, texturizado e hilado en frío hasta alcanzar cerca de 4 veces su longitud original, lo cual aumenta su cristalinidad y resistencia a la tracción.
Resistencia[editar]
| Compuesto | Valor |
| Alcoholes | Buena |
| Cetonas | Buena |
| Grasas y aceites | Mala |
| Halógenos | Mala |
| Hidrocarburos aromáticos | Buena |
Su viscosidad de fundido es muy baja, lo cual puede acarrear dificultades en la transformación industrial, y su exposición a la intemperie puede causar una fragilización y un cambio de color salvo si hay estabilización o protección previa.
Al nailon se le puede agregar fibra de vidrio para proporcionar un incremento en la rigidez.
Es un polímero cristalino ya que se le da un tiempo para que se organice y se enfríe lentamente, siendo por esto muy resistente.
Las cadenas de nailon con un número par de átomos de carbono entre los grupos amida son más compactas y sus puntos de fusión también son más altos que aquellas con un número impar de átomos de carbono. El punto de fusión disminuye y la resistencia al agua aumenta a medida que aumenta el número de grupos metileno entre los grupos amida.
Punto de fusión y solubilidad[editar]
El nailon es soluble en fenol, cresol y ácido fórmico. Su punto de fusión es de 263,12 °C.
Síntesis[editar]
El nailon se genera formalmente por policondensación de un diácido con una diamina. La cantidad de átomos de carbono en las cadenas de la amina y del ácido se puede indicar detrás de las iniciales de poliamida. El más conocido, el PA6.6 o nailon 6,6, es el producto formal del ácido hexanodioico (ácido adípico) y la hexametilendiamina.
Por razones prácticas no se prepara a partir del ácido y la amina, sino de disoluciones de la amina y del cloruro del diácido. Entre las dos fases, se forma el polímero que se puede expandir hasta formar el hilo de nailon.
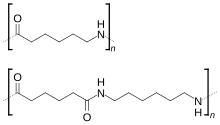
Un polímero parecido es el «perlón» (Nailon 6), que se forma por apertura y polimerización de una lactama, generalmente la caprolactama. La diferencia reside en que en el nailon las cadenas están formadas por polímeros con la fórmula general (..-NH-C(=O)-(CH2)n-C(=O)-NH-(CH2)m-...), mientras que en el perlón las cadenas tienen la secuencia (..-NH-C(=O)-(CH2)n-NH-C(=O)-(CH2)n-...).
Mecanismo de reacción[editar]
El nailon 6,6 tiene un monómero que se repite n veces, cuanto sea necesario para dar forma a una fibra. El primer 6 que acompaña al nailon representa el número de carbonos de la amida y la segunda cifra es el número de carbonos de la cadena ácida.
El nailon 6,6 se sintetiza por condensación en el laboratorio a partir de cloruro de adipoílo y hexametilenodiamina. Pero en una planta industrial de nailon se fabrica generalmente haciendo reaccionar el ácido adípico (derivado del fenol) con la hexametilenodiamina (derivado del amoníaco).
Cinética[editar]
Como el nailon se produce por condensación, la cinética es por pasos. Debido a que hay menos masa en el polímero que en los monómeros originales, se dice que el polímero está condensado con respecto a los monómeros. El subproducto es agua y se le denomina condensado.
Las polimerizaciones por condensación generan subproductos. Las polimerizaciones por adición, no.
Estado[editar]
De acuerdo con la funcionalidad F=2, el nailon es una fibra, generalmente de alta fusión.
La organización de las moléculas y el enfriamiento cuidadoso con que se hace para este fin determinan que el polímero sea cristalino.
Fuerzas moleculares[editar]
Las fuerzas moleculares del nailon son secundarias. Presenta fuerzas de London (no polar) y múltiples puentes de hidrógeno, como se puede ver en la figura anterior.
Los enlaces por puente de hidrógeno y otras interacciones secundarias entre cadenas individuales mantienen fuertemente unidas las cadenas poliméricas, lo que dificulta el deslizamiento de una sobre otra.
Esto significa que cuando se estiran las fibras de nailon no se extienden mucho, si es que lo hacen. Ello explica por qué las fibras son ideales para emplearlas en hilos y sogas.
Las fibras también tienen sus inconvenientes. Si bien poseen buena fuerza tensil, es decir que son resistentes cuando se las estira, por lo general tienen baja fuerza compresional, o sea, son débiles cuando se aprietan o se comprimen. Además, las fibras tienden a ser resistentes en una dirección, aquella en la cual están orientadas. Si se las estira en ángulos rectos a la dirección de su orientación, tienden a debilitarse.
Debido a esta extraña combinación de resistencias y debilidades, a menudo resulta una buena idea emplear las fibras juntamente con otro material, como un termorrígido.
Las fibras se usan frecuentemente para reforzar los termorrígidos. Compensan las falencias de los termorrígidos y, a su vez, las resistencias de los termorrígidos hacen lo propio con las falencias de las fibras.
Cuando un termorrígido o cualquier otro polímero se refuerza de este modo con una fibra, se dice que es un material compuesto.
Policondensación y etapas[editar]
El nailon se produce por medio de policondensación. Cuando el oxígeno del carbonilo es protonado, se vuelve mucho más vulnerable al ataque del nitrógeno de la diamina. El oxígeno protonado atrae los electrones que comparte con el carbonilo, lo que deja al carbono del carbonilo deficiente de electrones y listo para que el nitrógeno de la amina le done un par. El dímero también puede reaccionar con otros dímeros para formar un tetrámero. O puede reaccionar con un trímero para formar un pentámero y a su vez reaccionar con oligómeros más grandes. Finalmente, cuando esto sucede, los dímeros se transforman en trímeros, tetrámeros y oligómeros más grandes y estos oligómeros reaccionan entre sí para formar oligómeros aún más grandes. Esto sigue así hasta que se hacen lo suficientemente grandes como para ser considerados polímeros.
Para que las moléculas crezcan lo suficiente como para ser consideradas polímeros, hay que hacer esta reacción bajo vacío. En este caso, todo el subproducto de agua se evaporará y será eliminado del medio de reacción. Hay que deshacerse del agua para favorecer la reacción de Le Châtelier. Como se dijo antes, la reacción no necesita un catalizador ácido para llevarse a cabo; la razón por la que se sabe esto es que, al acercarse al final de la polimerización, donde no hay muchos grupos ácidos remanentes para comportarse como catalizadores, la reacción aún prosigue. Es decir, la amina puede reaccionar con los ácidos carboxílicos no protonados. Si no fuera así, no se podría obtener nailon 6,6 de alto peso molecular sin un catalizador externo, ya que la reacción se detendría a conversiones más altas, cuando no hubiese suficientes grupos ácidos para actuar como catalizadores.
La materia prima para la producción de nailon 6,6 es el benceno, el cual se deriva del craqueo y de la reformación del petróleo.
Usos del nailon[editar]

Además de como fibra textil, el nailon se utiliza para:
- Redes y líneas de pesca
- Piezas de autos (como el depósito de gasolina)
- Piezas de máquinas (como engranes y cojinetes)
- Cuerdas de guitarra
- Cremalleras
- Palas de ventiladores industriales
- Tornillos
- Suturas (cirugía)
- Pulseras de reloj (principalmente de uso militar y para buceo)
- Pulseras
Véase también[editar]
Referencias[editar]
- ↑ Real Academia Española. «nailon». Diccionario de la lengua española (23.ª edición).
- ↑ Real Academia Española. «nilón». Diccionario de la lengua española (23.ª edición).
- ↑ Audra J. Wolfe (ed.). «Nylon: A Revolution in Textiles». Chemical Heritage Magazine (en inglés). Filadelfia (Estados Unidos): Chemical Heritage Foundation. Consultado el 17 de julio de 2012. «The company then decided not to trademark the name, hoping instead to encourage consumers to think of nylon as a generic preexisting material, like wood or glass.»
- ↑ Klaus., Weissermel, (1981). Química orgánica industrial: productos de partida e intermedios más importantes. Reverté. ISBN 8429179895. OCLC 53782395.
- ↑ Silva Rodríguez, Francisco; Sanz Aragonés, José Emilio (1996). «Tema 13. Las fibras textiles. 13.6. Fibras sintéticas». Tecnología Industrial I (1.ª edición). Aravaca (Madrid, España): McGraw-Hill/Interamericana de España, S.A.U. pp. 194-205. ISBN 84-481-0444-7. «En 1938, cinco investigadores de la firma Du Pont de Nemours (USA) consiguieron la primera fibra textil por policondensación, que se patentó con el nombre de nylon. Dicha fibra fue bautizada con ese nombre en honor a las esposas de los integrantes del grupo: Nina, Yolanda, Lucy, Olga, Norma = NYLON».
Enlaces externos[editar]
 Wikimedia Commons alberga una galería multimedia sobre Nailon.
Wikimedia Commons alberga una galería multimedia sobre Nailon.
