Hidrosililación
La hidrosililación, también llamado hidrosilación catalítica, describe la adición de enlaces Si-H a través de enlaces insaturados. Normalmente la reacción se lleva a cabo catalíticamente y por lo general los sustratos insaturados son compuestos orgánicos. Los alquenos y los alquinos dan alquilos y silanos de vinilo; aldehídos y cetonas dan éteres de sililo. La hidrosililación se ha llamado la "aplicación más importante de platino en catálisis homogénea".[1] El proceso fue reportado por vez primera en la literatura científica en 1947[2] y fue anunciada por primera vez en 1972.[3]

Ámbito de aplicación y el mecanismo
[editar]La transformación catalítica representa un importante método para la preparación de compuestos orgánicos de silicio. Una transformación idealizada se ilustra mediante la adición de trietilsilano a difenilacetileno:[4]
- Et3SiH + PhC≡CPh → Et3Si(Ph)C=CH(Ph)
La reacción se relaciona mecánicamente a hidrogenación , y catalizadores similares se emplean a veces para los dos procesos catalíticos. En la industria "catalizador de Speier," ácido cloroplatínico (H2PtCl6) es importante.[5] El mecanismo por lo general supone un complejo de metal intermedio que contiene un hidruro, un enlace sililo (R3 Si), y el alqueno o alquino del sustrato.
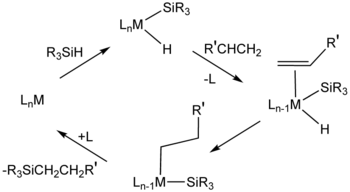
Estas reacciones también puede ser catalizada utilizando catalizadores a base de nanomaterial.
hidrosililación asimétrica
[editar]Usando fosfinas quirales como espectador ligando s, catalizadores se han desarrollado para hidrosilación asimétrica catalítica. Una reacción bien estudiado es la adición de triclorosilano al estireno para dar 1-fenil-1-(triclorosilil) etano:
- Cl3SiH + PhCHCH2 → (Ph)(CH3)CHSiCl3
Se puede lograr una casi perfecta enantioselectividades (ee) utilizando catalizadores de paladio soportados por binaftilo sustituidos con enlaces monofosfina.[6]
Hidrosililación de superficie
[editar]Las obleas de silicio se pueden grabar con ácido fluorhídrico (HF) para eliminar el óxido nativo, y forman una superficie de silicio terminado en hidrógeno. A continuación, las superficies terminadas en hidrógeno puede reaccionar con compuestos insaturados (tales como alquenos y alquinos terminales), para formar una monocapa estable sobre la superficie. Por ejemplo:
H:Si(100) + CH=CH(CH2)7CH3 → Si(100)-(CH2)9CH3
La reacción de hidrosililación se puede iniciar con luz UV a temperatura ambiente, o con aplicando calor (temperatura de reacción típica de 120-200 grados C), en virtud de las condiciones de humedad y del oxígeno libre.[7][8]
La monocapa resultante es estable e inerte, y evitar la oxidación de la capa de silicio base. La superficie de este tipo podría encontrar aplicaciones en áreas como la electrónica molecular, bioquímica y sensores electrónicos directos de biomoléculas.[9][10][11][12]
Referencias
[editar]- ↑ Renner, H.; Schlamp, G.; Kleinwächter, I.; Drost, E.; Lüschow, H. M.; Tews, P.; Panster, P.; Diehl, M.; Lang, J.; Kreuzer, T.; Knödler, A.; Starz, K. A.; Dermann, K.; Rothaut, J.; Drieselman, R. (2002). «Platinum group metals and compounds». Ullmann's Encyclopedia of Industrial Chemistry. Wiley. doi:10.1002/14356007.a21_075.
- ↑ Sommer, L.; Pietrusza, E.; Whitmore, F. «Peroxide-catalyzed addition of trichlorosilane to 1-octene». J. Amer. Chem. Soc. 69 (1): 188. doi:10.1021/ja01193a508.
- ↑ Ojima, I.; Nihonyanagi, M.; Nagai, Y. "Rhodium Complex Catalysed Hydrosilylation of Carbonyl Compounds" J. Chem. Soc., Chem. Commun. 1972, 938a. doi 10.1039/C3972000938A
- ↑ James L. Fry, Ronald J. Rahaim Jr., Robert E. Maleczka Jr. "Triethylsilane", Encyclopedia of Reagents for Organic Synthesis, John Wiley & Sons, 2007. doi 10.1002/047084289X.rt226.pub2
- ↑ C. Elschenbroich, Organometallics (2006) Wiley and Sons-VCH: Weinheim. ISBN 978-3-527-29390-2
- ↑ T. Hayashi and K. Yamasaki, "C–E Bond Formation through Asymmetric Hydrosilylation of Alkenes", Comprehensive Organometallic Chemistry III, Robert H. Crabtree and D. Michael P. Mingos, Editors. Amsterdam: Elsevier, 2007
- ↑ "Photoreactivity of Unsaturated Compounds with Hydrogen-Terminated Silicon (111)," R. L. Cicero, M. R. Linford, C. E. D. Chidsey, Langmuir 16, 5688-5695 (2000)
- ↑ "Alkyl Monolayers on Silicon Prepared from 1-Alkenes and Hydrogen-Terminated Silicon," M. R. Linford, P. Fenter, P. M. Eisenberger and C. E. D. Chidsey, J. Am. Chem. Soc. 117, 3145-3155 (1995).
- ↑ "Synthesis and characterization of DNA-modified Si(111) Surfaces," T. Strother, W. CAi, X. Zhao, R.J. Hamers, and L.M. Smith, J. Am. Chem. Soc. 122, 1205-1209 (2000).
- ↑ "T. Strother, R.J. Hamers, and L.M. Smith, "Surface Chemistry of DNA Covalent Attachment to the Silicon(100) Surface". Langmuir, 2002, 18, 788-796.
- ↑ Covalently Modified Silicon and Diamond Surfaces: Resistance to Non-Specific Protein Adsorption and Optimization for Biosensing," T.L. Lasseter, B.H. Clare, N.L. Abbott, and R.J. Hamers. J. Am. Chem. Soc. 2004, 126, 10220-10221.
- ↑ "Direct electrical detection of DNA Hybridization at DNA-modified silicon surfaces," W.Cai, J. Peck, D. van der Weide, and R.J. Hamers, Biosensors and Bioelectronics 19, 1013-1019 (2004).
