Etanoato de etilo
| Acetato de etilo | ||
|---|---|---|
 | ||
 | ||
| Nombre IUPAC | ||
| Etanoato de etilo | ||
| General | ||
| Otros nombres |
Acetato de etilo Acetidina Oxometileno de acetona | |
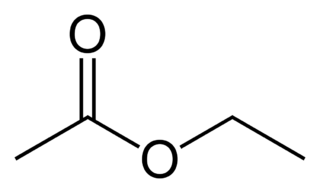
| Fórmula semidesarrollada | CH3-COO-CH2-CH3 | |
| Fórmula molecular | C4H8O2 | |
| Identificadores | ||
| Número CAS | 141-78-6[1] | |
| Número RTECS | AH5425000 | |
| ChEBI | 27750 | |
| ChEMBL | CHEMBL14152 | |
| ChemSpider | 8525 | |
| PubChem | 8857 | |
| UNII | 76845O8NMZ | |
| KEGG | C01883 D02319, C01883 | |
| Propiedades físicas | ||
| Densidad | 900 kg/m³; 0,9 g/cm³ | |
| Masa molar | 8811 g/mol | |
| Punto de fusión | 189 K (−84 °C) | |
| Punto de ebullición | 350 K (77 °C) | |
| Viscosidad | 0,45 cP a 20 °C | |
| Índice de refracción (nD) | 1,3724 a 20 °C | |
| Propiedades químicas | ||
| Solubilidad en agua | 8,7% a 20 °C | |
| Momento dipolar | 1,88 a 25 °C D | |
| Peligrosidad | ||
| SGA |
  | |
| Punto de inflamabilidad | 280 K (7 °C) | |
| NFPA 704 |
3
1
0
| |
| Temperatura de autoignición | 700 K (427 °C) | |
| Límites de explosividad | 2.2 - 11.0%[2] | |
| Riesgos | ||
| Riesgos principales | Altamente inflamable. | |
| Ingestión | Dolor abdominal, vértigo, náusea, dolor de garganta, debilidad. | |
| Inhalación | Tos, vértigo, somnolencia, dolor de cabeza, náusea, jadeo, dolor de garganta, pérdida de conocimiento, debilidad. | |
| Piel | Enrojecimiento, dolor. | |
| LD50 | 11,3 g/kg, rat | |
| Compuestos relacionados | ||
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
El etanoato de etilo según la IUPAC, también llamado acetato de etilo, y de otras formas (ver tabla) es un éster de fórmula CH3-COO-CH2-CH3. Su nombre antiguo es éter de vinagre, en alemán Essig-Äther, de donde proviene el término "esther" o éster.
El acetato de etilo es un líquido incoloro, característico de los ésteres, no residual. Es miscible con hidrocarburos, cetonas, alcoholes y éteres y poco soluble en agua. Se emplea en arte como disolvente universal.
Se obtiene de la reacción entre el ácido acético y el alcohol etílico.
Síntesis
[editar]La principal forma de sintetizar es mediante la esterificación de Fischer, esterificación directa mediante ácido acético y etanol en presencia de un catalizador.
- CH3CH2OH + CH3COOH ⇌ CH3COOCH2CH3 + H2O

Síntesis de Acetato de Etilo mediante esterificación de Fischer
Otro método de preparar ésteres es emplear no el ácido en sí, sino su cloruro, el etanoato de etilo se puede obtener por la acción del alcohol sobre el cloruro del ácido etanoico (cloruro de acetilo).

Puede obtenerse también, aunque no económicamente viable, al hacer reaccionar las sales de plata de los ácidos con halogenuro de alquilo, el etanoato de etilo se puede preparar en presencia de etanoato de plata y yoduro de etilo.

Es insoluble en agua y se disuelve con facilidad en disolventes orgánicos.
Reacciona con el agua para formar ácido acético y etanol, una reacción que es catalizada por la presencia de ácidos..
Aplicaciones
[editar]Química Industrial
[editar]- Producción de tintas de impresión para la industria gráfica.
- Remoción de la cafeína en los granos de café para la producción de café descafeinado[3]
- Producción de thinners y solventes de pinturas en industria de pinturas.
- En la industria de adhesivos y colas derivados de la celulosa.
- En la industria alimentaria, en productos de confitería, bebidas, dulces.
- En esencias artificiales de frutas.
- Remoción de sustancias resinosas en la industria del caucho.
- En la elaboración de cueros artificiales y para revestir y decorar artículos de cuero.
- Disolvente de compuestos utilizados para revestir y decorar objetos de cerámica.
- Solvente para la elaboración de varios compuestos explosivos.
- En la industria fotográfica, como solvente para la fabricación de películas a base de celulosa.
- Ingrediente de preparaciones cosméticas (perfumes, esmaltes, tónicos capilares) y farmacéutica.
- En la industria del papel, para la elaboración de papeles aprestados y para recubrir y decorar objetos de papel.
- En la industria textil, para la preparación de tejidos de lana para teñido, en procesos de limpieza y para la elaboración de textiles aprestados.
- Reactivo para la manufactura de pigmentos.
- En la industria tabacalera, su función es saborizante.
El uso directo en el procesado de medicamentos y de alimentos no se recomienda.
Aplicaciones en el laboratorio
[editar]En el laboratorio, el acetato de etilo es comúnmente usado en mezclas para cromatografía líquida y extracción. Es raramente seleccionado como un disolvente de reacción porque es propenso a la hidrólisis y a la transesterificación. El acetato de etilo es muy volátil y tiene un bajo punto de ebullición. Debido a estas propiedades, puede recuperarse de una muestra por calentamiento de la misma en un baño de agua y ventilando con aire comprimido.
Presencia en el vino
[editar]El acetato de etilo es uno de los componentes del vino, forma parte de la serie disolvente, también conocida como etérea, junto con alcoholes de menos peso y algunos ésteres más pesados. Se produce principalmente en una crianza de tipo oxidativo, y por tanto se encuentra en una mayor proporción en los vinos olorosos.
Síntesis química
[editar]Es un prometedor disolvente para la síntesis comercial de la vitamina E. Además, el acetato de etilo posee una muy buena capacidad de solvatación con respecto al reactivo y permite reducir la temperatura de proceso a 80 °C, que ciertamente incrementaría la calidad del producto (vitamina E). Sin embargo, hay algunos problemas relativos a la regeneración del acetato de etilo, en comparación con los anteriores disolventes utilizados en este proceso (acetato de butilo), ya que es más soluble en agua, más volátil, y está más sujeto a hidrólisis bajo las condiciones de síntesis.
Seguridad
[editar]Producto inflamable, no almacenar o mezclar con oxidantes fuertes, tales como cloro líquido y oxígeno concentrado. No manipular o almacenar cerca de llamas abiertas, calor, chispas, requiere ventilación adecuada. Es irritante de piel y vías respiratorias. Para conocer más información consultar la ficha internacional de seguridad química.
Referencias
[editar]- É. Yu. Bulychev, Yu. A. Pisarenko, and D. L. Efremov (2001). «Solvent regeneration in the synthesis of Vitamin E». Pharmaceutical Chemistry Journal 35 (9). p. 51-52. (enlace roto disponible en Internet Archive; véase el historial, la primera versión y la última).
- Breda, Evangelina (2008). Esterificación de Fischer.
- ↑ Número CAS
- ↑ Matheson Gas Data Book. «Lower and Upper Explosive Limits for Flammable Gases and Vapors (LEL/UEL)» (en inglés). Matheson Gas Products. p. 443. Archivado desde el original el 30 de septiembre de 2019. Consultado el 2 de octubre de 2016.
- ↑ Ramalakshmi, K.; Raghavan, B. (1 de julio de 1999). «Caffeine in Coffee: Its Removal. Why and How?». Critical Reviews in Food Science and Nutrition 39 (5): 441-456. ISSN 1040-8398. PMID 10516914. doi:10.1080/10408699991279231. Consultado el 26 de mayo de 2021.
Enlaces externos
[editar]- [1] Ficha internacional de seguridad química. Consultado el 9 de marzo de 2010.
- [2] Archivado el 28 de noviembre de 2016 en Wayback Machine. Propiedades del acetato de etilo. Consultado el 9 de marzo de 2010.
- [3] (enlace roto disponible en Internet Archive; véase el historial, la primera versión y la última). Ficha técnica del acetato de etilo. Consultado el 24 de marzo de 2010.
- [4] Federación Española de Asociaciones de Enólogos. Consultado el 18 de marzo de 2010.
- [5] Atanor. Consultado el 11 de marzo de 2010.


