Distrofia neuroaxonal infantil
| Distrofia neuroaxonal infantil | ||
|---|---|---|
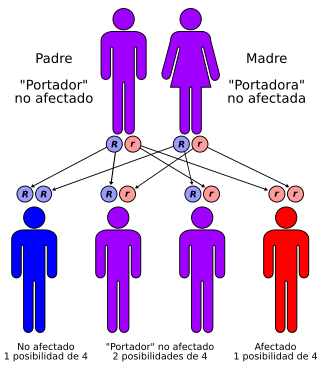 La distrofia neuroaxonal infantil tiene un patrón de herencia autosómico recesivo. | ||
| Especialidad | neurología | |
La distrofia neuroaxonal infantil es un trastorno generalizado del desarrollo raro que principalmente afecta el sistema nervioso. Los niños con distrofia neuroaxonal infantil no suelen presentar ningún síntoma al nacer, pero entre los 6 y los 18 meses de edad empiezan a experimentar retrasos en la adquisición de nuevas habilidades motoras e intelectuales, como gatear o empezar a hablar. Con el tiempo, pierden las habilidades previamente adquiridas.
Causa[editar]
Esta enfermedad se hereda con un patrón autosómico recesivo, lo que significa que hay dos copias del gen (PLA2G6) alteradas en cada célula. Lo más frecuente es que los padres de un individuo con un trastorno autosómico recesivo sean portadores cada uno de una copia del gen alterado, pero no muestran signos ni síntomas del trastorno[cita requerida]
Fisiopatología[editar]
Las mutaciones en el gen PLA2G6 deterioran la función de la enzima PLA2 grupo VI. Esta alteración de la función de la enzima puede interrumpir el mantenimiento de la membrana celular y contribuir al desarrollo de cuerpos esferoides en los axones nerviosos. Aunque se desconoce cómo los cambios en la función de esta enzima conducen a los signos y síntomas de la distrofia neuroaxonal infantil, se han observado problemas en el metabolismo de los fosfolípidos tanto en este trastorno como en otro relacionado llamado neurodegeneración asociada a la pantotenato quinasa. Estos trastornos, así como la enfermedad de Alzheimer y la de Parkinson, más comunes, también están asociados a cambios en el metabolismo del hierro en el cerebro. Los investigadores están estudiando los vínculos entre los defectos de los fosfolípidos, el hierro cerebral y el daño a las células nerviosas, pero no han determinado cómo la acumulación de hierro que se produce en algunos individuos con distrofia neuroaxonal infantil puede contribuir a las características de este trastorno.[1]
En algunos individuos con distrofia neuroaxonal infantil no se han encontrado mutaciones en el gen PLA2G6. Se desconoce la causa genética de la enfermedad en estos casos; hay indicios de que al menos otro gen puede estar implicado.[cita requerida]
Las mutaciones en el gen NAGA, que dan lugar a una deficiencia de alfa-N-acetilgalactosaminidasa, causan una distrofia neuroaxonal infantil conocida como enfermedad de Schindler.[1]
Diagnóstico[editar]
En algunos casos, los signos y síntomas de la distrofia neuroaxonal infantil aparecen por primera vez más tarde en la infancia o durante la adolescencia y progresan más lentamente. Los niños con distrofia neuroaxonal infantil experimentan dificultades progresivas de movimiento. Por lo general, tienen músculos que al principio son débiles y "flojos" (hipotónicos), y luego se vuelven gradualmente muy rígidos (espásticos). Al final, los niños afectados pierden la capacidad de moverse de forma independiente. La falta de fuerza muscular provoca dificultades para alimentarse y problemas respiratorios que pueden conducir a infecciones frecuentes, como la neumonía. En algunos niños afectados se producen convulsiones.[cita requerida]
Los movimientos oculares rápidos e involuntarios (nistagmo), los ojos que no miran en la misma dirección (estrabismo) y la pérdida de visión debido al deterioro (atrofia) del nervio óptico son característicos de la distrofia neuroaxonal infantil. También puede desarrollarse una pérdida de audición. Los niños con este trastorno experimentan un deterioro progresivo de las funciones cognitivas (demencia) y acaban perdiendo la conciencia de su entorno. [cita requerida]
La distrofia neuroaxonal infantil se caracteriza por el desarrollo de hinchazones llamadas cuerpos esferoides en los axones, las fibras que se extienden desde las células nerviosas (neuronas) y transmiten los impulsos a los músculos y a otras neuronas. Una parte del cerebro llamada cerebelo, que ayuda a controlar los movimientos, también puede estar dañada. En algunos individuos con distrofia neuroaxonal infantil, se acumulan cantidades anormales de hierro en una región específica del cerebro llamada ganglios basales.
Manejo[editar]
En la actualidad, sólo se dispone de tratamiento paliativo: alivio de la espasticidad y las convulsiones, baclofeno para aliviar la distonía, tratamiento fisioterapéutico y medidas como la sonda de alimentación gástrica o la traqueotomía para prevenir la neumonía por aspiración[2]
Investigación[editar]
En el verano de 2018 se inició un estudio clínico abierto para la evaluación a largo plazo de la eficacia, la seguridad, la tolerabilidad y la farmacocinética de un ácido graso poliinsaturado mejorado con deuterio, el RT001, que, tomado con alimentos, puede proteger las células neuronales de la degeneración.[3]
La pérdida de iPLA2-VIA, el homólogo de PLA2G6 en la mosca, reduce el tiempo de vida, perjudica la transmisión sináptica y provoca la neurodegeneración. Las fosfolipasas suelen hidrolizar los fosfolípidos de glicerina, pero la pérdida de iPLA2-VIA no afecta a la composición de fosfolípidos del tejido cerebral, sino que provoca un aumento de las ceramidas. La reducción de las ceramidas con fármacos, como la miriocina o la desipramina, alivia el estrés lisosomal y suprime la neurodegeneración.[4]
Actualmente, se está llevando a cabo una campaña a través de inadcure.org para recaudar 7 millones de dólares para financiar la investigación y realizar terapia génica en un grupo de niños. Una terapia génica que ha dado buenos resultados en ratones.
Referencias[editar]
- ↑ a b «Schindler disease: the molecular lesion in the alpha-N-acetylgalactosaminidase gene that causes an infantile neuroaxonal dystrophy». J. Clin. Invest. 86 (5): 1752-6. November 1990. PMC 296929. PMID 2243144. doi:10.1172/JCI114901.
- ↑ RESERVADOS, INSERM US14 -- TODOS LOS DERECHOS. «Orphanet: Infantile neuroaxonal dystrophy». www.orpha.net. Consultado el 11 de marzo de 2022.
- ↑ Retrotope, Inc. (6 de octubre de 2021). A Prospective Open-label Study to Assess Efficacy and Safety of RT001 in Subjects With Infantile Neuroaxonal Dystrophy (NCT03570931). clinicaltrials.gov. Consultado el 9 de marzo de 2022.
- ↑ Bellen, Hugo J.; Wang, Liping; Lin, Wen-Wen; Zuo, Zhongyuan; Tan, Kai Li; Mao, Dongxue; Chen, Kuchuan; Lee, Pei-Tseng et al. (2 de octubre de 2018). «Phospholipase PLA2G6, a Parkinsonism-Associated Gene, Affects Vps26 and Vps35, Retromer Function, and Ceramide Levels, Similar to α-Synuclein Gain». Cell Metabolism (en inglés) 28 (4): 605-618.e6. ISSN 1550-4131. PMID 29909971. doi:10.1016/j.cmet.2018.05.019.
Enlaces externos[editar]
- Esta obra contiene una traducción derivada de «Infantile neuroaxonal dystrophy» de Wikipedia en inglés, concretamente de esta versión, publicada por sus editores bajo la Licencia de documentación libre de GNU y la Licencia Creative Commons Atribución-CompartirIgual 4.0 Internacional.
