Fibronectina
| Fibronectina 1 | ||||
|---|---|---|---|---|
 | ||||
| Estructuras disponibles | ||||
| PDB | ||||
| Identificadores | ||||
| Símbolos | FN1 (HGNC: 3778) CIG; ED-B; FINC; FN; FNZ; GFND; GFND2; LETS; MSF | |||
| Identificadores externos | ||||
| Locus | Cr. 2 q34-36 | |||
| Patrón de expresión de ARNm | ||||
 | ||||
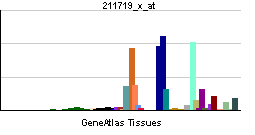 | ||||
 | ||||
| Más información | ||||
| Ortólogos | ||||
| Especies |
| |||
| Entrez |
| |||
| Ensembl |
| |||
| UniProt |
| |||
| RefSeq (ARNm) |
| |||
| RefSeq (proteína) NCBI |
| |||
| Ubicación (UCSC) |
| |||
| PubMed (Búsqueda) |
| |||
La fibronectina es una glucoproteína presente en todos los vertebrados.
Estructura
[editar]La fibronectina es una glucoproteína de unos 440 kDa que puede presentarse en forma monomérica o dimérica y está presente en la matriz extracelular (MEC) de la mayoría de los tejidos celulares animales. Está formada por dos subunidades de unos 250 kDa cada una unidas por puentes disulfuro situados cerca del extremo carboxilo. Cada subunidad está formada por tres tipos de dominios, I, II y III funcionalmente distintos separados por regiones polipeptídicas flexibles. Estos dominios están compuestos por módulos más pequeños que, al repetirse secuencialmente y estar codificados por un exón diferente, sugieren que el exón de la fibronectina se originó por duplicaciones exónicas múltiples. La fibronectina contiene 12 dominios de tipo I, dos de tipo II y entre 15 y 17 de tipo III, los cuales dan cuenta de aproximadamente un 90% de su secuencia polipeptídica. Los dominios de tipo I tienen una longitud de unos 40 residuos y contienen dos puentes disulfuro, los de tipo II abarcan unos 60 residuos y también contienen dos puentes disulfuro, mientras que los de tipo III tienen unos 90 residuos de longitud sin puentes disulfuro. Estos tres tipos de dominio también se encuentran en otras moléculas, lo que sugiere que la fibronectina pudo haber evolucionado mediante exon shuffling.
La transcripción produce una única y enorme molécula de ARN mensajero que madurará alternativamente dando lugar a las diferentes isoformas de fibronectina, dando lugar hasta 20 isoformas diferentes: el módulo principal es la repetición de fibronectina tipo III, cuya repetición número 9 contiene el sitio de unión a integrinas RGD, un tripéptido formado por arginina, glicina y ácido aspártico. Aparte de dicho sitio, contiene un sitio de unión a colágeno (dominios I6 a I9 incluyendo los II1 y II2) y a heparina (III12-14), el cual también une factores de crecimiento como la proteína morfogénica ósea o el factor de crecimiento vascular endotelial, entre otros. Los dominios I10 a I12 contienen un sitio de unión a fibrina tipo II.
Función
[editar]Existen hasta 20 isoformas diferentes. Una, la denominada fibronectina plasmática, es soluble y circula por la sangre donde parece incrementar la coagulación de la sangre, la cicatrización y la fagocitosis.
El resto se organizan en la superficie celular depositándose en la matriz extracelular como fibrillas de fibronectina muy insolubles, con dímeros que presentan enlaces disulfuro adicionales. Este proceso, donde las células organizan las moléculas de fibronectina estirándolas y formado fibrillas, se denomina fibrilogénesis.
Las moléculas de fibronectina solo se organizan en fibrillas en la superficie de ciertas células. Ello se debe a que para su formación son necesaria proteínas complementarias, especialmente las integrinas que reconocen la propia fibronectina. En los fibroblastos, las fibrillas de fibronectina se asocian con las integrinas en regiones de la membrana denominadas adhesiones focales donde las fibrillas localizadas en asociación con la superficie celular se hallan muy estiradas y sometidas a fuerzas de tracción. Estas fuerzas son ejercidas por las propias células y resultan esenciales para la formación de las fibrillas. Por otra parte, algunas de las proteínas de secreción tienen como función impedir el ensamblaje de la fibronectina en lugares inapropiados.
Las fibrillas de fibronectina que se forman en o cerca de la superficie de los fibroblastos suelen alinearse con las fibras de estrés adyacentes, siendo los filamentos de actina intracelulares los que estimulan el ensamblaje de las moléculas de fibronectina una vez secretadas y regulan la orientación de las fibrillas.
Las interacciones que se establecen en la membrana de los fibroblastos entre las fibrillas extracelulares de fibronectina y los filamentos intercelulares de actina están mediadas en su mayor parte por integrinas. Así es como el citoesqueleto contráctil de actina y miosina tira de la matriz de fibronectina generando fuerzas de tracción. El resultado es el estiramiento de la fibrillas que provoca la exposición de un lugar de unión críptico (no accesible) mediante el que las moléculas de fibronectina pueden unirse directamente unas a otras. De esta forma el citoesqueleto de actina estimula la polimerización de la fibronectina y el ensamblaje de la matriz. Las señales extracelulares pueden regular este ensamblaje alterando el citoesqueleto de actina, modificando así la fuerza de tracción de las fibrillas.
La fibronectina no solo juega un papel importante en la adhesión de las células a la matriz, sino que también actúa como guía de las migraciones celulares que tiene lugar en los embriones de los vertebrados. Por ejemplo, en células mesodérmicas durante la gastrulación de anfibios, siendo el único tipo de células que presenta esta característica en embriones tempranos. La importancia de la fibronectina en el desarrollo animal ha sido demostrada en experimentos de inactivación génica, los ratones que no pueden expresar fibronectina mueren en los primeros estadios de la embriogénesis, ya que sus células endoteliales son incapaces de formar vasos sanguíneos funcionales.
