Diosgenina
| Diosgenina | ||
|---|---|---|
 | ||
 | ||
| Nombre IUPAC | ||
| (20α,22R,25R)-espirosta-5-en-3β-ol | ||
| General | ||
| Fórmula estructural |
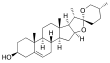 | |
| Fórmula molecular | C27H42O3 | |
| Identificadores | ||
| Número CAS | 512-06-1[1] | |
| ChEBI | 4629 | |
| ChEMBL | 412437 | |
| ChemSpider | 89870 | |
| PubChem | 99474 | |
| UNII | K49P2K8WLX | |
| KEGG | C08898 | |
|
O1[C@@H]4[C@H]([C@@H]([C@]12OC[C@@H](CC2)C)C)[C@@]5(C)CC[C@@H]3[C@@]6(C(=C/C[C@H]3[C@@H]5C4)\C[C@@H](O)CC6)C
| ||
| Propiedades físicas | ||
| Masa molar | 41 462 g/mol | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
La diosgenina es un Δ5 espirostano obtenido por hidrólisis de la saponina dioscina. Se encuentra en abundancia significativa en las raíces de las especies Dioscorea composita y Dioscorea floribunda.
Usos
[editar]Debido a su semejanza estructural, se utiliza como materia prima en la producción sintética de hormonas esteroidales.
Síntesis de esteroides
[editar]Síntesis del precursor común
[editar]1) Protección del doble enlace
[editar]Como primer paso de la síntesis de esteroides se procede a la protección del doble enlace con bromo (Br2).
2) Clivaje espiroacetálico
[editar]El clivaje del sustituyente espiroacetal se produce con anhídrido acético a altas temperaturas.
3) Oxidación
[editar]Se produce la oxidación del doble enlace, abriéndose de este modo el anillo E.
4) Hidrólisis
[editar]Con una base en condiciones suaves se produce la hidrólisis de los ésteres y la posterior eliminación del protón del carbono 17, formándose un doble enlace. La 5α,6β-dibromo-3β-hidroxipregn-16-en-20-ona producida es el precursor común en la síntesis de hormonas esteroidales.
Referencias
[editar]- (20α,22R,25S)-Spirosta-5-ene-3β-ol. Chemical Book.

