Porfirina
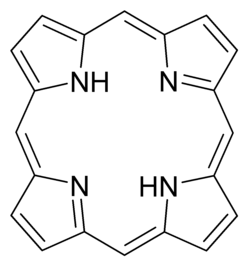
Se denomina porfirina al grupo prostético de las cromoproteínas porfirínicas.[1] Están compuestas por un anillo tetrapirrólico con sustituyentes laterales y un átomo metálico en el centro, unido mediante cuatro enlaces de coordinación. Se clasifican basándose en los sustituyentes laterales del anillo, de modo que se distinguen meso porfirinas, uroporfirinas, etio porfirinas y protoporfirinas. Estas últimas son las más relevantes. Presentan como sustituyentes 4 metilos, 2 vinilos y 2 grupos propiónicos.
Existen 15 isómeros de protoporfirinas, pero en la naturaleza solo aparece el IX, que se caracteriza por disponer cuatro grupos metilo en posición 1,3,5 y 8, grupos vinilo en posición 2 y 4 y en posición 6 y 7 grupos propiónicos. A este grupo pertenecen la hemoglobina, la mioglobina y los citocromos, entre otros.

Estructura de las porfirinas
[editar]
La estructura de las porfirinas posee anillos formados por hidrocarburos en su mayoría causantes de las reacciones electrolíticas (nucleofílicas y electrofílicas) a las que se ven sometidas las porfirinas que de acuerdo con la densidad electrónica se experimentan en las posiciones meso y el anillo reducido del pirrol. Estos anillos son estructuras compartidas entre la clorofila y la hemoglobina. En el centro del anillo se encuentra un átomo de hierro que conforma lo que se llama el grupo Hemo. La estructura permite que en su interior puedan fluir libremente electrones, los cuales son transportados y localizados en otros sitios, actuando en dos procesos fundamentales de la vida: la fotosíntesis y la respiración aeróbica.
Las interacciones con otras moléculas pueden causar que la porfirina sea metalizada o desmetalizada. En este último caso, se convierte en agente que cataliza la síntesis en forma tóxica de oxígeno. De esta forma las porfirinas se excitan cuando incide sobre su superficie radiación electromagnética de ciertas longitudes de onda, haciendo que sus electrones salten de un nivel energético a otro con mayor energía, trasmitiendo su energía a otras moléculas con enlaces apropiados para la producción de oxígeno monoatómico, y radicales libres; es decir que las porfirinas no metálicas no son agentes sino mediadoras de la destrucción: catalizan la síntesis de formas tóxicas de oxígeno.
Síntesis química
[editar]En la obtención de porfirinas ocurren dos procesos fundamentales. Uno de ellos consiste en la modificación de sustitutos del grupo hemo; el otro proceso consiste en la síntesis de la porfirina que sugiere una modificación natural como en el hemo, pero es más selectiva respecto a la absorción de sustitutos periféricos ya que algunos de ellos no permiten ser modificados. La síntesis que se desarrolla en las porfirinas se puede clasificar en:
Tetramerización del monopirrol
[editar]
Se realiza sobre las porfirinas que contienen solamente un sustituto. Allí se somete a reacción un pirrol 2-5 y un aldehído (Síntesis de Rothemund). También se utiliza para sintetizar el meso-tetrafenilporfil. Otro acercamiento de la tetramerización del monopirrol, implica la doble-condensación de un 2-acetoximetilpirrol o de 2-N,N-dimetilaminometilpirrol. y posteriormente la condensación similar con 2-hidroximetilpirrol, se ha realizado la sintetización de varias porfirinas, incluyendo los porfirinas con centro-simétrico, (conteniendo dos tipos de sustitutos situados en posiciones alternas).
Condensación de los intermediarios de los dipirroles
[editar]Utilizados en las porfirinas que poseen un centro simétrico en donde los sustituyentes tienen esa misma simetría a una de las mitades de las moléculas, los intermediarios más utilizados para la síntesis son los dipirrometinos, donde la doble condensación de 1-bromo-9-metildipirrometino, en un fundimiento de ácido orgánico, como el ácido succínico, que funde a la temperatura de 189 °C da buenas producciones de porfirinas. Condensando un 1,9-dibromodipirrometina y un 1,9-dimetildipirrometina, este método se puede utilizar también para la sinterización de las porfirinas, en los cuales una o ambas mitades de la molécula son simétricas (esquema 1,5). Una variación de este método implica la reacción de 1-bromo-9-bromometildipirrometino en ácido fórmico para dar las porfirinas para producciones relativamente altas.
La síntesis de porfirinas implica la condensación de un sustituto de 1-9-formildipirrometano o la condensación de un sustituyente y de un 1,9-diformildipirrometano en la presencia de un catalizador ácido tal como ácido yodhídrico o ácido p-toluenosulfónico.Esta ruta se utiliza extensamente hoy también porque los dipirrometanos requeridos para la síntesis de porfirinas a menudo están preparados y purificados más fácilmente que los dipirrometinos correspondientes.
Compuestos de la porfirina
[editar]Dentro de los diversos componentes de la porfirina tenemos a la clorofila la cual es principalmente un pigmento encargado de la fotosíntesis absorbiendo energía en todas las longitudes de onda del espectro visible, excepto las del verde, detectado por nuestros ojos. Posee cuatro anillos pirrólicos complejos.
Otro componente fundamental es la hemoglobina, que es una molécula encargada de trasportar el oxígeno y dióxido de carbono. Está en los glóbulos rojos y consta de cuatro unidades (cadenas polipeptídicas). Las cuatro cadenas siempre están agrupadas en pares. En el humano adulto, hay dos cadenas idénticas alfa, y dos cadenas beta. Cada una de las cuatro cadenas tiene un átomo de Fe2+ en su centro. Los cuatro átomos de hierro permiten que la molécula de hemoglobina ligue cuatro moléculas de oxígeno. Se encuentra en los eritrocitos (glóbulos rojos) y es la encargada de transportar el O2 molecular en sangre arterial y captar el CO2 para pasar a sangre venosa y oxigenarse nuevamente en los pulmones. Si las moléculas de hemoglobina se combinan con el oxígeno se produce los que se denomina como oxihemoglobina, que es roja y pigmenta la sangre. Sin embargo, cuando la moléculas de oxígeno ingresan a los tejidos, la hemoglobina se torna verdosa. El producto de la degradación de la Hb en el humano es la bilirrubina. Los valores normales en sangre en el hombre son de 13 a 18 mg/100 ml, mientras que para la mujer son de 12 a 16 mg /100 ml.
Características fundamentales
[editar]En toda la estructura de la porfirina se encuentra un sistema de enlaces conjugados, aspecto que la hace rígida sin permitirle cambiar de estado fácilmente, también permite la intensa banda de absorción cerca de 400nm seguida por otra banda de absorción más débil 450–700 nm. Estas absorciones cambian debido a las mutaciones de los sustitutos del anillo pirrólico. El anillo de pirrol es estable con ácidos concentrados. Las bases fuertes tales como los alcóxidos pueden quitar los dos protones (pKa ~16) a los átomos internos del nitrógeno de una porfirina para formar un di-anión. Por otra parte, los dos átomos libres del nitrógeno de la porfirina (pKb ~9) pueden ser protonados fácilmente con ácidos, como el trifluoroacético.
Psoralenos
[editar]Son los primeros fotosensibilizadores utilizados en la piel con los que se demostró que sus reacciones frente a la luz no son siempre de carácter maligno. Estos al ser radiados con luz, reaccionan con la estructura del ADN de las células infecciosas, destruyéndolas. Un estudio realizado por Aarón B. Lerner y Thomas Fizpatric de la universidad de Harvard, analizo el comportamiento de los psoralenos concluyendo que el potencial al cual actúan estos es relativamente alto, al incidir luz sobre su superficie de varias longitudes de onda demostraron que estos reaccionaban bajo la incidencia de rayos ultravioleta; posteriormente se comenzó a aplicar esta técnica como terapia en personas con disfunciones en la piel. Este método se conoce actualmente como PUVA. Bajo la extraordinaria aplicación de la técnica PUVA surgió la inquietud (en Thomas Doughety del instituto Roswell Park del cáncer) de generar algún cambio en la estructura de los psoralenos para verificar si su comportamiento se mantenía acorde con los resultados anteriores, realizando una comparación del potencial de foto sensibilización entre los psoralenos y la porfirina, se dio cuenta de que esta última presenta un potencial elevado con respecto a los psoralenos, frente a esta verificación era viable pensar que las porfirinas podrían matar tumores completos en vez de células sueltas como lo hacían los psoralenos. De esta manera fue como surgió la terapia foto dinámica TFD en la cual ciertos fotosensibilizadores catalizan la producción de radicales libres de oxígeno.
También se encontró que las porfirinas presentan un carácter selectivo atribuido a la formación de enlaces y fuerzas eléctricas, y un proceso de aglomeración en la célula a tratar. Contrario a lo que sucede con los psoralenos, estas reaccionan bajo la incidencia de luz roja, debido a que su frecuencia le permite incidir con mayor energía en tejidos profundos. Con el fin de lograr mejores resultados de colimo el rayo de luz roja incidente de manera que solo llegase a la zona a tratar. Sin embargo, a pesar de la opción que presenta en el tratamiento del cáncer, algunas de las porfirinas quedan el tejido aun después de haber atacado las células cancerígenas, en esta media bajo la exposición a la luz solar se presentan sarpullidos en la piel, para quienes se han expuesto a la TFD, que son índice de que las porfirinas están atacando el tejido biológico. Sobre la base de dichos efectos secundarios se planteó implantar en el tejido una mezcla de soluto con porfirina pero los resultados fueron nefastos ya que la mezcla al no ser pura no tenía la energía suficiente para entrar en las células totalmente y no eliminar completo el tumor. Otro factor importante que impedía el éxito rotundo de la técnica fue que debido al carácter de aglomeración de las porfirinas, ya que la energía de la radiación incidente sería absorbida por estas, cuando son demasiadas, y no sería suficiente para activarlas. Aunque los resultados en contra de la técnica superaban su viabilidad, estos representaban datos aforos acerca de los lineamientos de se debían seguir para implantar una técnica efectiva, dados los resultados anteriores se sugirió realizar porfirinas sintéticas.
Porfiria
[editar]Las sustancias que desempeñan un papel en la Porfiria y en la terapia fotodinámica se encuentran entre las más antiguas e importantes de las moléculas biológicas. Allí se combinan los dos procesos críticos de generación de energía en los seres vivos: la fotosíntesis y la respiración aeróbica. En el primero la energía lumínica es captada por clorofilas (porfirinas) y convertida en energía química; en la respiración, el grupo Hemo de la Hemoglobina transporta el oxígeno a los tejidos. Hemos y clorofilas son hierro y magnesio derivados de la protoporfirina.
La porfiria resulta de una alteración del mecanismo productor de Hemo en el organismo. Todas las células vivas tienen la capacidad de sintetizar porfirinas. El camino de biosíntesis de las porfirinas en el cuerpo humano consiste en sintetizar hemo y otras porfirinas, en una serie de ocho estados coordinados catalizado cada uno por una enzima diferente, comenzando por moléculas pequeñas hasta las complejas moléculas de los tetrapirroles cíclicos o porfirinas.
Las porfirias constituyen un grupo heterogéneo de trastornos afines, en los cuales las porfirinas se acumulan en la piel. La porfiria puede ser genética o adquirida, en la porfiria se omite uno de los pasos de la biosíntesis del Hemo, lo que produce un exceso de los compuestos intermedios generados en etapas anteriores a la secuencia, allí el organismo no ha evolucionado como para eliminar metabolismos intermedios, como consecuencia de esos desórdenes enzimáticos, se van a cumular en el organismo y se excretan las moléculas llamadas precursores, ácido aminolevulínico () y porfobilinógeno o bien distintas porfirinas.
Referencias
[editar]- ↑ Scribd (s/f). «Porfirina». Consultado el 23 de junio de 2024.
