Ecuación química
Una ecuación química es la descripción simbólica de una reacción química (es decir, como se representa de forma escrita, por medio de símbolos, un proceso químico de la naturaleza). Muestra las sustancias que reaccionan (llamadas reactivos) y las sustancias que se originan (llamadas productos).[1] La ecuación química ayuda a visualizar más fácilmente los reactivos y los productos. Además, se pueden ubicar los símbolos químicos de cada uno de los elementos o compuestos que estén dentro de la ecuación y poder balancearlos con mayor facilidad.
En 1615 Jean Beguin publicó Tyrocinium Chymicum, uno de los primeros trabajos escritos sobre química, en donde escribió la primera ecuación química de la historia.[2]
Requisitos para una ecuación química
[editar]Una ecuación química debe satisfacer una serie de leyes, de forma simultánea:[3][4]
- Cumplir con la ley de conservación de la materia.
- Cumplir con la ley de conservación de la carga.
- Cumplir con la ley de conservación de la energía.
Nótese que no se especifica que el proceso en cuestión ocurra realmente en la naturaleza o el laboratorio. Por ejemplo, la ecuación química global de la formación del agua gaseosa, a partir de las sustancias dihidrógeno y dioxígeno (presentada posteriormente), en realidad ocurre en una serie de pasos intermedios (denominados mecanismo de reacción), correspondiéndose con la sucesión de reacciones químicas que ocurren para producir el producto dado.
Estructura
[editar]Una ecuación química (véase un ejemplo más abajo) consiste en una lista de reactivos (las sustancias de partida) en el lado izquierdo, una símbolo de flecha, y una lista de productos (sustancias formadas en la reacción química) en el lado derecho. Cada sustancia se especifica mediante su fórmula química, opcionalmente precedida de un número llamado coeficiente estequiométrico'.[5]. El coeficiente especifica cuántas entidades (por ejemplo, moléculas) de esa sustancia intervienen en la reacción sobre una base molecular. Si no se escribe explícitamente, el coeficiente es igual a 1. Las sustancias múltiples en cualquier lado de la ecuación están separadas entre sí por un signo más.
Como ejemplo, la ecuación para la reacción de ácido clorhídrico con sodio puede denotarse:
Dado que las fórmulas son bastante simples, esta ecuación podría leerse como "dos H-C-L más dos N-A rendimientos[6] dos N-A-C-L y H dos". Alternativamente, y en general para las ecuaciones que implican productos químicos complejos, las fórmulas químicas se leen utilizando nomenclatura IUPAC, lo que podría verbalizar esta ecuación como "dos moléculas de ácido clorhídrico y dos átomos de sodio reaccionan para formar dos unidad de fórmulas de cloruro de sodio y una molécula de gas hidrógeno."
Interpretación de una ecuación química
[editar]Un caso general de ecuación química sería:
donde:
- A, B, C, D, representan los símbolos químicos o la fórmula molecular de los átomos o moléculas que reaccionan (lado izquierdo) y los que se producen (lado derecho).
- a, b, c, d, representan los coeficientes estequiométricos, que deben ser ajustados de manera directa a la ley de conservación de la masa.
La interpretación física de los coeficientes estequiométricos, si estos son números enteros y positivos, puede ser en átomos o moles. Así, se diría de la ecuación de geometría estequiométrica se subdivide en la siguiente:
- Cuando "a" moléculas de A reaccionan con "b" moléculas de B producen "c" moléculas de C, y "d" moléculas de D.
- Cuando "a" moles de moléculas de A reaccionan con "b" moles de moléculas de B producen "c" moles de moléculas de C, y "d" moles de moléculas de D.
Por ejemplo el gas dihidrógeno (H2) puede reaccionar con dioxígeno (O2) para dar agua en fase (termodinámica) gas (H2O). La ecuación química para esta reacción se escribe:
El símbolo + se lee como «reacciona con», mientras que el símbolo → se lee como «produce». Para ajustar la ecuación planteada (hacer que se cumpla la ley de conservación de la materia), ponemos los coeficientes estequiométricos:
La ecuación está ajustada y puede ser interpretada como 2 mol de moléculas de dihidrógeno reaccionan con 1 mol de moléculas de dioxígeno, produciendo 2 mol de moléculas de agua.
Las fórmulas químicas a la izquierda de la flecha de reacción (→) representan las sustancias reaccionantes o reactantes; a la derecha de la flecha de reacción están las fórmulas químicas de las sustancias producidas, denominadas productos.
Los números delante de las fórmulas son llamados coeficientes estequiométricos. Estos deben ser tales para que la ecuación química esté balanceada, es decir, que el número de átomos de cada elemento de las sustancias reaccionantes y de los productos de la reacción sea el mismo. Los coeficientes deben ser enteros positivos, y el uno se omite. En las únicas reacciones que esto no se produce es en las reacciones nucleares.
Finalmente (pero no menos importante), se deben agregar (entre paréntesis y como subíndice) los estados de agregación molecular de cada sustancia participante: sólido (s), líquido (l), acuoso (aq) o gaseoso (g).
En el ejemplo del agua:
Tipos de reacciones
[editar]Diferentes tipos del símbolo flecha se utilizan para indicar el tipo de reacción química:[1]
reacción directa neta 
reacción en ambas direcciones [8] equilibrio[10] relación estequiométrica resonancia (no es una reacción)
Equilibrio de ecuaciones químicas
[editar]Dado que en una reacción química no se produce ninguna reacción nuclear, los elementos químicos atraviesan la reacción sin cambios. Así, cada lado de la ecuación química debe representar el mismo número de átomos de cualquier elemento particular (o nucleido, si se tienen en cuenta diferentes isótopos). Lo mismo ocurre con la carga eléctrica total, tal y como establece la ley de conservación de la carga. Se dice que una ecuación que cumple estos requisitos está equilibrada.
Una ecuación química se equilibra asignando valores adecuados a los coeficientes estequiométricos. Las ecuaciones sencillas pueden equilibrarse por inspección, es decir, por ensayo y error. Otra técnica consiste en resolver un sistema de ecuaciones lineales.
Las ecuaciones equilibradas suelen escribirse con los coeficientes de número-natural más pequeños. Sin embargo, a veces puede ser ventajoso aceptar un coeficiente fraccionario, si simplifica los otros coeficientes. Así, el ejemplo introductorio puede reescribirse como
En algunas circunstancias, los coeficientes fraccionarios son incluso inevitables. Por ejemplo, la reacción correspondiente a la entalpía estándar de formación debe escribirse de forma que se forme una molécula de un único producto. Esto requerirá a menudo que algunos coeficientes de los reactantes sean fraccionarios, como es el caso de la formación de fluoruro de litio:
Método de inspección
[editar]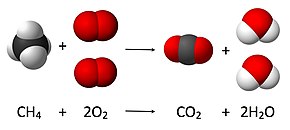
4 + 2 O
2 → CO
2 + 2 H
2O, hay que anteponer un coeficiente 2 al gas oxígeno en el lado de los reactantes y al agua en el lado de los productos para que, según la ley de conservación de la masa, la cantidad de cada elemento no varíe durante la reacción.
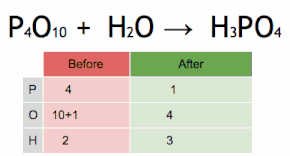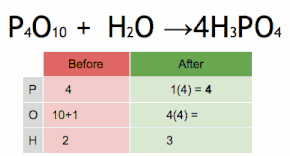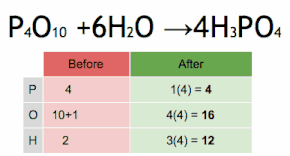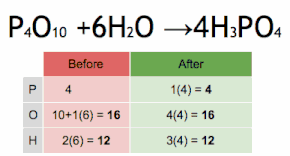
Esta ecuación química se equilibra multiplicando primero H3PO4 por 4 para igualar el número de átomos de P, y luego multiplicando a H2O por seis para equilibrar el número de átomos de H y O.
El método de inspección puede resumirse fijando el coeficiente estequiométrico de la sustancia más compleja en 1 y asignando valores a otros coeficientes paso a paso, de forma que ambos lados de la ecuación acaben con el mismo número de átomos para cada elemento. Si durante este proceso surge algún coeficiente fraccionario, la presencia de fracciones puede eliminarse (en cualquier momento) multiplicando todos los coeficientes por su mínimo común denominador.
- Ejemplo
Balance de la ecuación química para la combustión total de metano
se realiza mediante los siguientes pasos:
- Un coeficiente de uno se coloca en la fórmula más compleja (CH4):
- El lado izquierdo tiene un átomo de carbono, por lo que una molécula de CO2 lo equilibra. El lado izquierdo también tienes cuatro átomos de hidrógeno, lo cual se equilibra con dos moléculas de H2O:
- El equilibrio de cuatro átomos de oxígeno del lado derecho mediante dos moléculas de O2 conduce a la ecuación
- Se omiten los coeficientes iguales a 1, ya que no es necesario especificarlos explícitamente:
- Es conveniente comprobar que la ecuación final está equilibrada, es decir, que para cada elemento hay el mismo número de átomos en el lado izquierdo y en el derecho: 1 carbono, 4 hidrógeno y 4 oxígeno.
Sistema de ecuaciones lineales
[editar]Para cada elemento químico (o nucleído o resto no modificado o carga) i, el requerimiento de su conservación se puede expresar mediante la ecuación matemática:
donde
- aij es el número de átomos del elemento i en una molécula de sustancia j (según la fórmula en la ecuación química), y
- sj es el coeficiente esteiquimétrico de la sustancia j.
Los resultados son un sistema de ecuaciones lineales homogéneas, las cuales se resuelven directamente utilizando métodos matemáticos. Tal sistema tiene la solución trivial de todos ceros, que no es de interés, pero si es que existen soluciones adicionales, existirá un número infinito de ellas. Cualquier solución no trivial equilibrará la ecuación química. Una solución "preferida" es una con un número entero, mayormente positivo [11]
Ejemplo
[editar]Asignemos variables a los coeficientes estequiométricos de la ecuación química del apartado anterior y escribamos las ecuaciones lineales correspondientes:
Todas las soluciones a este sistema de ecuaciones lineales son de la siguiente forma, donde r es cualquier número real:
La elección de r = 1 produce la solución preferida,
que corresponde a la ecuación química equilibrada:
Catálisis y otras condiciones
[editar]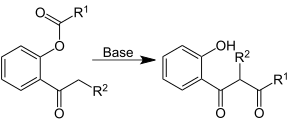
Si la reacción requiere energía, lo mismo se indica encima de la flecha. Una letra griega delta (Δ) mayúscula a un triángulo (△)[12] se coloca en la flecha de la reacción para indicar que se agrega energía en forma de calor a la reacción. La expresión hν[13] es utilizada como símbolo para el agtregado de energía en forma de luz. Se utilizan otros símbolos para otros tipos específicos de energía o radiación.
Del mismo modo, si una reacción requiere un determinado medio con ciertas características específicas, entonces el nombre del ácido o la base que se utiliza como medio puede colocarse encima de la flecha. Si no se requiere un ácido o una base específicos, otra forma de denotar el uso de un medio ácido o básico es escribir H+ o OH− (o aún "ácido" o "base") arriba de la flecha. Las condiciones específicas de temperatura y presión, así como la presencia de catalizadores, pueden indicarse del mismo modo.
Véase también
[editar]Referencias
[editar]- ↑ a b Unión Internacional de Química Pura y Aplicada. «chemical reaction equation». Compendium of Chemical Terminology. Versión en línea (en inglés).
Error en la cita: Etiqueta
<ref>no válida; el nombre «goldbook» está definido varias veces con contenidos diferentes - ↑ Crosland, M. P. (1959). «The use of diagrams as chemical 'equations' in the lectures of William Cullen and Joseph Black.» Annals of Science, Vol 16, No. 2, Junio.
- ↑ R, Petrucci. et al. (2011). Química General (10° ed). Madrid: PEARSON EDUCATION, S.A.. pp.35,255
- ↑ F, Carey. (2006). Química orgánica (6ta ed). México: The McGraw-Hill Companies, Inc. p.34
- ↑ No confundir con una cantidad relacionada llamada número estequiométrico.
- ↑ Que no debe confundirse con rendimiento (química), una cuantificación de la eficiencia de síntesis.
- ↑ van 't Hoff, J.H. (1884). Études de Dynamique Chemique [Studies of chemical dynamics] (en francés). Amsterdam, Netherlands: Frederik Muller & Co. pp. 4-5. «Or M. Pfaundler a relié ces deux phénomênes … s'accomplit en même temps dans deux sens opposés.»
- ↑ La notación ⇄ fue propuesta en 1884 por el químico neerlandés Jacobus Henricus van't Hoff. Van't Hoff denominó a la reacción que no se realiza por completo "reacciones limitadas". Al respecto escribió (traducido del francés):[7] "Ahora el Sr. Pfaundler ha unido estos dos fenómenos en un solo concepto al considerar el límite observado como el resultado de dos reacciones opuestas, conduciendo la del ejemplo citado a la formación de sal marina. [o sea ClNa] y ácido ´nítrico, [y] el otro al ácido clorhídrico y al nitrato de sodio. Esta consideración, que la experiencia valida, justifica la expresión "equilibrio químico", que se utiliza para caracterizar el estado final de las reacciones limitadas. Propondría traducir esta expresión por el siguiente símbolo:
- HCl + NO3 Na ⇄ NO3 H + Cl Na.
- ↑ Marshall, Hugh (1902). «Suggested Modifications of the Sign of Equality for Use in Chemical Notation». Proceedings of the Royal Society of Edinburgh 24: 85-87. doi:10.1017/S0370164600007720.
- ↑ La notación fue propuesta por Hugh Marshall en 1902.[9]
- ↑ Un coeficiente estequiométrico negativo significa una sustancia colocada en el lado incorrecto de la ecuación química. stoichiometric coefficients sj with greatest common divisor equal to one.
- ↑ El triángulo (△) era originalmente el símbolo químico del fuego.
- ↑ Esta expresión proviene de la ecuación de Planck para la energía del fotón, E = hν. La letra griega ν ("nu") que a veces es reemplazada por error por la letra latina v ("vee").
Bibliografía
[editar]- Seese, William S. & G. William Daub: Química. En Google Books
Enlaces externos
[editar]- Descripción de un algoritmo para igualar ecuaciones químicas utilizando el método algebraico, y su implementación en el lenguaje de programación Logo
- Aplicación en línea para balanceo de ecuaciones moleculares





















