Síntesis química
Síntesis química es el proceso por el cual se producen compuestos químicos a partir de compuestos simples o precursores químicos.[1] Su rama más amplia es la síntesis orgánica. También es realizada por los organismos vivientes en su metabolismo, como ejemplo están las proteínas.[1]
El objetivo principal de la síntesis química, además de producir nuevas sustancias químicas, es el desarrollo de métodos más económicos y eficientes para sintetizar sustancias naturales ya conocidas, como por ejemplo el ácido acetilsalicílico (presente en las hojas del sauce) o el ácido ascórbico o vitamina C, que se encuentra de forma natural en muchos vegetales.
La respiración celular, proceso utilizado por la mayoría de las células animales y vegetales, es la degradación de biomoléculas (glucosa, lípidos, proteínas) para que se produzca la liberación de energía necesaria, y así el organismo pueda cumplir con sus funciones vitales. Mediante la degradación de la glucosa (glucólisis) se forma ácido pirúvico. Este ácido se desdobla a dióxido de carbono y agua, generándose 36 moléculas de ATP.
También la síntesis química permite obtener productos que no existen de forma natural, como el acero, los plásticos o los adhesivos.
Actualmente hay catalogados unos once millones de productos químicos de síntesis y se calcula que cada día se obtienen unos 2000 más.
El progreso científico ha permitido un gran desarrollo de las técnicas de síntesis química, como la síntesis en fase sólida o la química combinatoria.
Inicialmente estos productos se obtenían de manera casual mientras que, en la actualidad, es posible realizar simulaciones por ordenador antes de experimentar en el laboratorio..

Procedimiento
[editar]La síntesis química comienza seleccionando los compuestos químicos que se conocen como reactivos. Varios tipos de reacciones químicas se pueden aplicar para sintetizar un producto final o un producto intermedio y puede que se requiera una serie de pasos antes de aislar los productos.[2] El rendimiento es la cantidad de producto obtenido y se expresa en gramos o en porcentaje de la cantidad teórica que debería haberse producido. Puede haber reacciones indeseadas que disminuyen los rendimientos.
Estrategias
[editar]Existen muchas estrategias en la síntesis química que son más complicadas que simplemente convertir un reactivo A en un producto de reacción B directamente. Para la síntesis de varios pasos, un compuesto químico se sintetiza mediante una serie de reacciones químicas individuales, cada una con su propio procesamiento.[3] Por ejemplo, una síntesis de laboratorio de paracetamol puede constar de tres partes secuenciales. Para las reacciones en cascada, ocurren múltiples transformaciones químicas dentro de un solo reactivo, para las reacciones de múltiples componentes, hasta 11 reactivos diferentes forman un solo producto de reacción y para una " síntesis telescópica"un reactivo experimenta múltiples transformaciones sin aislamiento de intermedios.
Síntesis orgánica
[editar]La síntesis orgánica es un tipo especial de síntesis química que se ocupa de la síntesis de compuestos orgánicos. Para la síntesis total de un producto complejo, se pueden requerir múltiples procedimientos en secuencia para sintetizar el producto de interés, requiriendo una gran cantidad de tiempo. Habilidad en la síntesis orgánica es muy apreciado entre los químicos y la síntesis de compuestos excepcionalmente valiosos o difíciles ha ganado químicos tales como Robert Burns Woodward un Premio Nobel de Química. Si una síntesis química parte de compuestos básicos de laboratorio, se considera un proceso puramente sintético. Si parte de un producto aislado de plantas o animales y luego procede a nuevos compuestos, la síntesis se describe como un proceso semisintético .
Síntesis inorgánica
[editar]La síntesis inorgánica y la síntesis organometálica se aplican a la preparación de compuestos con un contenido no orgánico significativo. Un ejemplo ilustrativo es la preparación del fármaco contra el cáncer cisplatino a partir de tetracloroplatinato de potasio. [4]
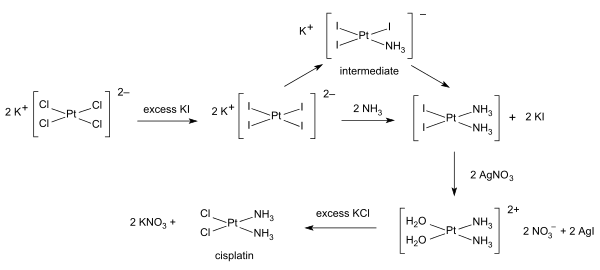
Síntesis de gases
[editar]En principio, el gas de síntesis se puede producir a partir de eductos (materiales de partida) sólidos (s - sólido), líquidos (l - líquido) y gaseosos (g - gaseosos).
Gas de síntesis a partir de eductos sólidos
[editar]En la producción de gas de síntesis a partir de materiales de partida sólidos, la gasificación del carbón es particularmente importante. Carbón - C(s) se produce en una mezcla de oxidación parcial (parcial/incompleta) con aire u oxígeno puro - O2(g) y gasificación con vapor - H2O(g) a una mezcla de monóxido de carbono - CO(g) e hidrógeno - H2(g). Debido al equilibrio de Boudouard, el CO(g) todavía está en equilibrio con C(s) y dióxido de carbono – CO2(g):
Además, hay que tener en cuenta el equilibrio gas de agua:
La reacción exotérmica con el oxígeno proporciona la energía necesaria para alcanzar la alta temperatura de reacción para la reacción endotérmica. reacción de gasificación del carbón con vapor de agua.
La composición del gas de síntesis puede controlarse mediante una hábil selección de la materia prima (en función del contenido deseado de monóxido de carbono e hidrógeno).
Dado que el carbón contiene otros elementos además del carbono (azufre, nitrógeno, vanadio, ...), el gas de síntesis obtenido aún debe limpiarse y procesarse después del reactor. Sobre todo hay que eliminar el agua, el CO2, el hollín y el H2S.
Además del carbón, se prevé el uso de otros sólidos como: La biomasa (madera, paja) es concebible, pero también es necesario un tratamiento previo de los materiales de entrada y un tratamiento posterior o limpieza del gas de síntesis.
Gas de síntesis a partir de eductos líquidos
[editar]Diversos destilados del petróleo crudo pueden utilizarse como reactivos líquidos para el gas de síntesis, tanto las fracciones de bajo punto de ebullición como las de alto punto de ebullición. Los destilados de bajo punto de ebullición pueden convertirse tras eliminar el azufre mediante reacción con vapor utilizando el proceso de reformado con vapor. El proceso de reformado con vapor es una reacción endotérmica que se lleva a cabo en un catalizador heterogéneo (reacción que utiliza pentano como ejemplo):
Cuando se utilizan fracciones de aceite de alto punto de ebullición (residuo viscoso flasheado, véase craqueo), se lleva a cabo una oxidación parcial, que no requiere catalizador (reacción utilizando pentano como ejemplo):
Gas de síntesis a partir de reactantes gaseosos
[editar]El reactante gaseoso más importante para la producción de gas de síntesis es el gas natural. En comparación con los demás eductos, el gas natural suministra la mayor proporción de hidrógeno en relación con el monóxido de carbono.
Reformado con vapor
[editar]El gas natural se hace reaccionar con vapor mediante el proceso de reformado con vapor:
La empresa Linde es uno de los mayores fabricantes con 4.000 sistemas construidos y los llama planta HyCO, al igual que SynGas como HyCO (hidrógeno-CO).[4]
Convertidor de plasma
[editar]Un proceso de dos etapas desarrollado en 2012 produce gas de síntesis, que se compone únicamente de monóxido de carbono e hidrógeno. En el primer paso, el metano se descompone en una mezcla de carbono e hidrógeno utilizando plasma a más de 1000 °C[5] (reacción: CH4 + energía → C + 2 H2 ). En el segundo paso, se añade CO2 a la mezcla de carbono e hidrógeno. El carbono y el CO2 reaccionan a altas temperaturas para formar monóxido de carbono (reacción: C + CO2 → 2 CO). Alternativamente, se puede utilizar agua en lugar de CO2 para obtener una mayor concentración de hidrógeno en el gas de síntesis. [6] En este caso la segunda reacción es: C + H2O → CO + H2.
Junto con el hidrógeno del primer paso, ambas alternativas producen un gas de síntesis de alta pureza, que se compone únicamente de CO y H2.[7]
La proporción de CO a H2 se puede variar en cada caso. Si el gas de síntesis se adapta a un proceso de síntesis posterior (p. ej., síntesis de Fischer-Tropsch, DME, gasolina y alcohol), se produce un proceso PGtL (PGtL - Power-and-Gas-to-Liquid). [8]
Síntesis industriales
[editar]Las reacciones de síntesis química más importantes se utilizan para producir una materia prima (por ejemplo: proceso de Haber-Bosch para la síntesis de amoníaco; producción de metilclorosilanos como intermedio para la producción de siliconas), o para la producción de un ingrediente activo ( por ejemplo: síntesis de ácido acetilsalicílico a partir de fenol). La síntesis de sustancias quirales (fármacos, pesticidas, etc.) con una estructura tridimensional uniforme se puede realizar mediante síntesis enantioselectiva o catálisis enantioselectiva. Las síntesis a menudo reciben el nombre de sus descubridores, por ejemplo, la síntesis de Reppe, la Síntesis de Fischer-Tropsch o síntesis de Asinger.[9]
Ámbitos en los que la síntesis es esencial
[editar]Catalizadores
[editar]La catálisis es fundamental para una amplia gama de procesos industriales, que abarcan tanto la fabricación de productos químicos a granel como de productos químicos finos. El diseño racional, la síntesis y la optimización de sistemas catalizadores son, por tanto, cruciales para el desarrollo de procesos más eficientes, selectivos y tolerantes con el medio ambiente. La investigación en este campo se centra tanto en los sistemas que contienen metales como en los que no, y su objetivo no es sólo mejorar los catalizadores de los procesos existentes, sino también lograr transformaciones catalíticas totalmente nuevas.[10]
Medicina y descubrimiento de fármacos
[editar]El desarrollo de nuevos productos farmacéuticos es un aspecto sumamente importante de la síntesis orgánica. Esta tarea permite descubrir y optimizar moléculas complejas con una actividad biológica potente y selectiva. La comprensión de la química sintética permite equilibrar las propiedades químicas para que las moléculas se comporten como se desea en células y pacientes. El desarrollo de nuevas reacciones es otra faceta esencial de este trabajo, porque abre rutas antes inaccesibles a nuevos compuestos.[10]
Nuevos materiales
[editar]La preparación de materiales funcionales con propiedades diseñadas a medida (por ejemplo, electrónicas, ópticas, magnéticas) es fundamental para lograr avances en ámbitos como las baterías, el desarrollo de células solares, los superconductores, los materiales inteligentes, etc., que son muy prometedores para las tecnologías del futuro. Numerosos laboratorios cuentan con una larga trayectoria en este campo.[10]
Biología química
[editar]La síntesis de moléculas diseñadas para interactuar con sistemas biológicos y sondearlos es muy útil para investigar y comprender los procesos que intervienen en los sistemas vivos. Estos compuestos nos permiten comprender mejor los procesos biológicos fundamentales y contribuir al descubrimiento de fármacos mediante la validación eficaz de dianas.[10]
Productos naturales
[editar]La historia de los medicamentos, los aromas y los productos agroquímicos ilustra la importancia capital de los productos naturales. La química sintética es muy útil para imitar a la Naturaleza y nos permite preparar moléculas complejas que se producen de forma natural pero sin alterar la propia fuente. Estos productos naturales, y sus análogos, tienen innumerables usos como fármacos, aromatizantes y agroquímicos.[10]
Obtención de imágenes
[editar]Los tintes y sondas sintéticos han tenido una gran importancia en los últimos avances en el campo de la imagen, lo que permite utilizar técnicas más potentes y menos intrusivas en la búsqueda de tejidos enfermos o dañados.[10]
Véase también
[editar]Referencias
[editar]- ↑ a b Física y Química 4o ESO. Escrito por Dulce María Andrés Cabrerizo ,Dulce María Andrés, Javier Barrio, Juan Luis Antón, Juan Luis Antón Bozal, Javier Barrio Pérez, p. 214, en Google Libros
- ↑ Vogel, A.I. B.S., Hannaford, A.J. and P.W.G. Smith. Vogel's Textbook of Practical Organic Chemistry, 5th Edition. Prentice Hall, 1996. ISBN 0582462363.
- ↑ Carey, Francis A.; Sundberg, Richard J. (2013). Advanced Organic Chemistry Part B: Reactions and Synthesis. Springer.
- ↑ «HYCO Registernummer 896361 DPMA». Consultado el 28 de octubre de 2022.
- ↑ «dieBrennstoffzelle.de – Proceso de Kvaerner». Consultado el 21 de noviembre de 2019.
- ↑ Patente(https://worldwide.espacenet.com/patent/search/family/048522145/publication/EP2794467B1?q=pn%3DEP2794467B1), No 2794467, B1. Proceso y sistema para producir gas de síntesis. 23 noviembre 2016- Technology GmbH. Olaf Kühl
- ↑ Patente (https://worldwide.espacenet.com/patent/search/family/048522145/publication/EP2794466B1?q=pn%3DEP2794466B1), No 794466, B1. Proceso y sistema para convertir dióxido de carbono en monóxido de carbono. 26 agosto 2015. CCP Technology GmbH- Olaf Kühl
- ↑ Patente (https://worldwide.espacenet.com/patent/search/family/053191665/publication/EP3160899B1?q=pn%3DEP3160899B1), No 3160899 B1. Método y dispositivo para producir gas de síntesis rico en H2. 12 diciembre 2018. CCP Technology GmbH - Olaf Kühl
- ↑ Brockhaus ABC Chemie, VEB F. A. Brockhaus Verlag Leipzig 1965, pag 1370.
- ↑ a b c d e f E.J.Corey. The Logic of Chemical Synthesis. (1995), 455 pag. ISBN 0471115940, ISBN 9780471115946
Bibliografía
[editar]- Nicolaou, K. C.; Sorensen, E. J. (1996). Classics in Total Synthesis. New York: VCH. (requiere registro).
- «Taxol – The Drama behind Total Synthesis». www.org-chem.org. Archivado desde el original el 27 de julio de 2011. Consultado el 20 de noviembre de 2016.
- March, J.; Smith, D. (2001). Advanced Organic Chemistry, 5th ed. New York: Wiley.
- Carey, J.S.; Laffan, D.; Thomson, C.; Williams, M.T. (2006). «Analysis of the reactions used for the preparation of drug candidate molecules». Org. Biomol. Chem. 4 (12): 2337-2347. PMID 16763676. S2CID 20800243. doi:10.1039/B602413K.
- Nicolaou, K. C.; Hale, Christopher R. H.; Nilewski, Christian; Ioannidou, Heraklidia A. (9 de julio de 2012). «Constructing molecular complexity and diversity: total synthesis of natural products of biological and medicinal importance». Chemical Society Reviews (en inglés) 41 (15): 5185-5238. ISSN 1460-4744. PMC 3426871. PMID 22743704. doi:10.1039/C2CS35116A.





