Histona deacetilasa 7A
| Histona deacetilasa 7A | ||||
|---|---|---|---|---|
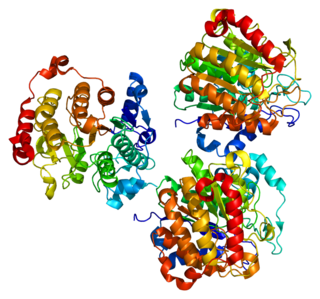 Estructura tridimensional de la proteína HDAC7A. | ||||
| Estructuras disponibles | ||||
| PDB |
Lista de códigos PDB 2nvr
| |||
| Identificadores | ||||
| Símbolos | HDAC7A (HGNC: 14067) HDAC7; DKFZP586J0917 | |||
| Identificadores externos | ||||
| Locus | Cr. 12 q13.11 | |||
| Ortólogos | ||||
| Especies |
| |||
| Entrez |
| |||
| UniProt |
| |||
| RefSeq (ARNm) |
| |||
La histona deacetilasa 7A (HDAC7A) es una enzima codificada en humanos por el gen hdac7A.[1][2][3]
Función[editar]
Las histonas juegan un papel crucial en la regulación de la transcripción, en la progresión del ciclo celular y en procesos de desarrollo. La acetilación/desacetilación de histonas altera la estructura del cromosoma, variando así la accesibilidad de los factores de transcripción al ADN. La HDAC9 presenta homología de secuencia con los miembros de la familia de histona deacetilasas. Este gen es ortólogo del gen hdac7 de ratón, cuya proteína promueva la represión vía transcripcional del correpresor SMRT. Se han descrito diversas variantes transcripcionales de este gen, que codifican diferentes isoformas de la proteína.[3]
Interacciones[editar]
La histona deacetilasa 7A ha demostrado ser capaz de interaccionar con:
Véase también[editar]
Referencias[editar]
- ↑ Marks PA, Richon VM, Rifkind RA (Aug de 2000). «Histone deacetylase inhibitors: inducers of differentiation or apoptosis of transformed cells». J Natl Cancer Inst 92 (15): 1210-6. PMID 10922406.
- ↑ Kao HY, Downes M, Ordentlich P, Evans RM (Feb de 2000). «Isolation of a novel histone deacetylase reveals that class I and class II deacetylases promote SMRT-mediated repression». Genes Dev 14 (1): 55-66. PMC 316336. PMID 10640276.
- ↑ a b «Entrez Gene: HDAC7A histone deacetylase 7A».
- ↑ Lee, H J; Chun M, Kandror K V (mayo. de 2001). «Tip60 and HDAC7 interact with the endothelin receptor a and may be involved in downstream signaling». J. Biol. Chem. (United States) 276 (20): 16597-600. ISSN 0021-9258. PMID 11262386. doi:10.1074/jbc.C000909200.
- ↑ a b Fischle, W; Dequiedt F, Fillion M, Hendzel M J, Voelter W, Verdin E (Sep. de 2001). «Human HDAC7 histone deacetylase activity is associated with HDAC3 in vivo». J. Biol. Chem. (United States) 276 (38): 35826-35. ISSN 0021-9258. PMID 11466315. doi:10.1074/jbc.M104935200.
- ↑ Xiao, Hui; Chung Jin, Kao Hung-Ying, Yang Yu-Chung (Mar. de 2003). «Tip60 is a co-repressor for STAT3». J. Biol. Chem. (United States) 278 (13): 11197-204. ISSN 0021-9258. PMID 12551922. doi:10.1074/jbc.M210816200.
- ↑ Lemercier, Claudie; Brocard Marie-Paule, Puvion-Dutilleul Francine, Kao Hung-Ying, Albagli Olivier, Khochbin Saadi (Jun. de 2002). «Class II histone deacetylases are directly recruited by BCL6 transcriptional repressor». J. Biol. Chem. (United States) 277 (24): 22045-52. ISSN 0021-9258. PMID 11929873. doi:10.1074/jbc.M201736200.
- ↑ Koipally, Joseph; Georgopoulos Katia (Aug. de 2002). «A molecular dissection of the repression circuitry of Ikaros». J. Biol. Chem. (United States) 277 (31): 27697-705. ISSN 0021-9258. PMID 12015313. doi:10.1074/jbc.M201694200.
Enlaces externos[editar]
- MeSH: HDAC7A+protein,+human (en inglés)
