Bifenilo
| Bifenilo | ||
|---|---|---|
 | ||
 | ||
| Nombre IUPAC | ||
| 1,1'-Bifenilo | ||
| General | ||
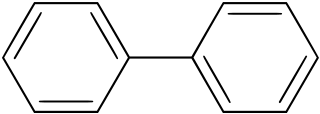
| Fórmula estructural |
| |
| Fórmula molecular | C12H10 | |
| Identificadores | ||
| Número CAS | [92-52-4][1] | |
| Número RTECS | DU8050000 | |
| ChEBI | 17097 | |
| ChEMBL | CHEMBL14092 | |
| ChemSpider | 6828 | |
| PubChem | 7095 | |
| UNII | 2L9GJK6MGN | |
| KEGG | C06588 | |
| Propiedades físicas | ||
| Densidad | 1040 kg/m³; 1,04 g/cm³ | |
| Masa molar | 15 421 g/mol | |
| Punto de fusión | 343 K (70 °C) | |
| Punto de ebullición | 529 K (256 °C) | |
| Punto de descomposición | 342 K (69 °C) | |
| Peligrosidad | ||
| Punto de inflamabilidad | 386 K (113 °C) | |
| NFPA 704 |
1
2
0
| |
| Temperatura de autoignición | 813 K (540 °C) | |
| Frases R | R36/37/38, R50/53 | |
| Frases S | S2, S23, S60, S61 | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
El bifenilo (difenilo, fenilbenceno o 1,1'-bifenilo) es un compuesto orgánico sólido cristalino desde incoloro a amarillo claro. Posee un aroma muy agradable. El bifenilo es un hidrocarburo aromático con una fórmula molecular C12H10. Es conocido por ser un producto inicial en la producción de bifenilos policlorados (PCB), que fue usado ampliamente como fluido dieléctrico y agente de transferencia de calor. También es un intermediario para la producción como anfitrión de otros compuestos orgánicos como emulsificantes, iluminadores ópticos, productos insecticidas y plásticos.
Propiedades[editar]
El bifenilo se encuentra de manera natural en alquitrán mineral, crudo y gas natural, y puede ser producido con esos materiales a partir de la destilación. Es insoluble en agua, pero es soluble en solventes orgánicos comunes. La molécula bifenilo consiste en dos anillos de benceno conectados, sin ninguna funcionalidad adicional, y en consecuencia no es muy reactiva. El punto de inflamabilidad es de 113 °C y su temperatura de autoignición es de 540 °C.
Estereoquímica[editar]
Hay una rotación en el enlace C-C entre los dos fenilos, y especialmente en sus derivativos orto-sustituidos, están impedidos estéricamente. Por lo tanto, algunos bifenilos sustituidos presentan atropisomerismo; una condición donde los isómeros individuales C2simétricos son conformacionalmente estables. Algunos derivados, en algunas moléculas afines como el BINAP, tiene aplicación como ligandos en la síntesis asimétrica.
Aspectos biológicos[editar]
El bifenilo previene el crecimiento de moho y hongos, y es usado como conservante (E230, en combinación con E231, E232 y E233), particularmente en la preservación de los cítricos durante su transporte.
Es medianamente tóxico, pero puede ser degradado biológicamente por conversión a componentes no tóxicos. También algunas bacterias posen anillos aromáticos de bifenilo añadidos con moléculas de oxígeno. Se ha demostrado que algunas bacterias que pueden degradar bifenilo, también pueden degradar bifenilos policlorados (PCB), una sustancia sintética que es más dañina al ambiente que sus contrapartes naturales.[2]
Compuestos[editar]
Los bifenilos sustituidos pueden ser preparados de manera sintética con reacciones de acoplamiento tales como la reacción de Suzuki y la reacción de Ullmann. Los bifenilos policlorados actúan como congelantes y los bifenilos polibromados son retardantes del fuego. Un compuesto del bifenilo aparece en algunos fármacos como Valsartán y Telmisartán.
Referencias[editar]
- ↑ [92-52-4 Número CAS]
- ↑ Biphenyl degradation - Streptomyces coelicolor, en GenomeNet Database (en inglés)
 Este artículo incorpora texto de una publicación sin restricciones conocidas de derecho de autor:
Este artículo incorpora texto de una publicación sin restricciones conocidas de derecho de autor:  Varios autores (1910-1911). «Encyclopædia Britannica». En Chisholm, Hugh, ed. Encyclopædia Britannica. A Dictionary of Arts, Sciences, Literature, and General information (en inglés) (11.ª edición). Encyclopædia Britannica, Inc.; actualmente en dominio público.
Varios autores (1910-1911). «Encyclopædia Britannica». En Chisholm, Hugh, ed. Encyclopædia Britannica. A Dictionary of Arts, Sciences, Literature, and General information (en inglés) (11.ª edición). Encyclopædia Britannica, Inc.; actualmente en dominio público.- Wiley/VCH, Weinh (1991). Biphenyl (1,1- Biphenyl). ISBN 3-527-28277-7.
Enlaces externos[editar]
- Instituto Nacional de Seguridad e Higiene en el Trabajo de España: Ficha internacional de seguridad química del Bifenilo.
- Tarjeta de Seguridad Química Internacional 0106 (en inglés)
- Inventario Nacional de Contaminantes – Bifenilo (en inglés)

