Adsorción

Incremento en la concentración de una sustancia en la interfaz de un condensado y una capa líquida o gaseosa debido a la operación de las fuerzas de superficie. Nota 1: La adsorción de proteínas es de gran importancia cuando un material está en contacto con sangre o fluidos corporales. En el caso de sangre, albúmina, la cual es ampliamente predominante, es generalmente primero adsorbida, y entonces el reordenamiento ocurre en favor de otras proteínas menores acorde a la afinidad de la superficie frente a la selección de la ley de masas (efecto Vroman). Nota 2: Las moléculas adsorbidas son aquellas que son resistentes al lavado con el mismo medio disolvente en el caso de adsorción de soluciones. Las condiciones de lavado pueden así modificar los resultados de la medición, particularmente cuando la energía de interacción es baja.[1] |
La adsorción es la adhesión de átomos, iones o moléculas de un gas, líquido o sólido disuelto a una superficie.[2] Este proceso crea una película de adsorbato en la superficie del adsorbente. Este proceso difiere de la absorción, en la que un fluido (el absorbente) se disuelve o penetra en un líquido o sólido (el absorbente), respectivamente.[3] La adsorción es un fenómeno de superficie, mientras que la absorción involucra todo el volumen del material, aunque la adsorción a menudo precede a la absorción.[4] El término sorción engloba ambos procesos, mientras que desorción es lo contrario.
Similar a la tensión superficial, la adsorción es una consecuencia de la energía superficial. En un material a granel, todos los requisitos de enlace (ya sean iónicos, covalentes o metálicos) de los átomos constituyentes del material están llenos de otros átomos en el material. Sin embargo, los átomos en la superficie del adsorbente no están completamente rodeados por otros átomos adsorbentes y por lo tanto pueden atraer adsorbatos. La naturaleza exacta de la unión depende de los detalles de las especies involucradas, pero el proceso de adsorción generalmente se clasifica como fisisorción (característica de las fuerzas débiles de van der Waals) o quimisorción (característica de la unión covalente). También puede ocurrir debido a la atracción electrostática.[5]
La adsorción está presente en muchos sistemas naturales, físicos, biológicos y químicos y se usa ampliamente en aplicaciones industriales como catalizadores heterogéneos,[6][7] carbón activado, captura y uso de calor residual para proporcionar agua fría para el aire acondicionado y otros requisitos del proceso (enfriadores de adsorción), resinas sintéticas, aumento de la capacidad de almacenamiento de carbonos derivados de carburo y purificación de agua. La adsorción, el intercambio iónico y la cromatografía son procesos de sorción en los que ciertos adsorbatos se transfieren selectivamente desde la fase fluida a la superficie de partículas rígidas insolubles suspendidas en un recipiente o empaquetadas en una columna. Aplicaciones de la industria farmacéutica, que utilizan la adsorción como medio para prolongar la exposición neurológica a fármacos específicos o partes de los mismos, son menos conocidos.
La palabra "adsorción" fue acuñada en 1881 por el físico alemán Heinrich Kayser (1853-1940).[8]
Isotermas[editar]

La adsorción de gases y solutos generalmente se describe a través de isotermas, es decir, la cantidad de adsorbato en el adsorbente en función de su presión (si es gas) o concentración (para solutos en fase líquida) a temperatura constante. La cantidad adsorbida casi siempre está normalizada por la masa del adsorbente para permitir la comparación de diferentes materiales. Hasta la fecha, se han desarrollado 15 modelos de isotermas diferentes.[9]
Lineal[editar]
Freundlich[editar]
El primer ajuste matemático a una isoterma fue publicado por Freundlich y Kuster (1906) y es una fórmula puramente empírica para adsorbatos gaseosos:
donde es la masa de adsorbato adsorbido, es la masa del adsorbente, es la presión del adsorbato (esto se puede cambiar a concentración si se investiga una solución en lugar de un gas), y y son constantes empíricas para cada par de adsorbente-adsorbato a una temperatura dada. La función no es adecuada a una presión muy alta porque en realidad tiene un máximo asintótico a medida que la presión aumenta sin límite. A medida que aumenta la temperatura, las constantes y cambiar para reflejar la observación empírica de que la cantidad adsorbida aumenta más lentamente y se requieren presiones más altas para saturar la superficie.
Langmuir[editar]
Irving Langmuir fue el primero en derivar una isoterma de adsorción con base científica en 1918.[10] El modelo se aplica a los gases adsorbidos en superficies sólidas. Es una isoterma semi-empírica con una base cinética y se derivó con base en la termodinámica estadística. Es la ecuación de isoterma más común debido a su simplicidad y su capacidad para adaptarse a una variedad de datos de adsorción. Se basa en cuatro supuestos:
- Todos los sitios de adsorción son equivalentes y cada sitio solo puede albergar una molécula.
- La superficie es energéticamente homogénea y las moléculas adsorbidas no interactúan.
- No hay transiciones de fase.
- En la adsorción máxima, solo se forma una monocapa. La adsorción solo ocurre en sitios localizados en la superficie, no con otros adsorbatos.
Estas cuatro suposiciones rara vez son todas ciertas: siempre hay imperfecciones en la superficie, las moléculas adsorbidas no son necesariamente inertes y el mecanismo claramente no es el mismo para las primeras moléculas que se adsorben en una superficie que para la última. La cuarta condición es la más problemática, ya que con frecuencia se adsorberán más moléculas en la monocapa; este problema es abordado por la isoterma BET para superficies relativamente planas (no microporosas). No obstante, la isoterma de Langmuir es la primera opción para la mayoría de los modelos de adsorción y tiene muchas aplicaciones en la cinética de la superficie (generalmente llamada cinética de Langmuir-Hinshelwood) y en la termodinámica.
Langmuir sugirió que la adsorción tiene lugar a través de este mecanismo: , donde A es una molécula de gas y S es un sitio de adsorción. Las constantes de velocidad directa e inversa son k y k−. Si definimos la cobertura de la superficie, , como la fracción de los sitios de adsorción ocupados, en el equilibrio tenemos:
o
donde es la presión parcial del gas o la concentración molar de la solución. Para presiones muy bajas , y para altas presiones .
El valor de es difícil de medir experimentalmente; generalmente, el adsorbato es un gas y la cantidad adsorbida se da en moles, gramos o volúmenes de gas a temperatura y presión estándar (STP) por gramo de adsorbente. Si llamamos vmon al volumen STP de adsorbato requerido para formar una monocapa en el adsorbente (por gramo de adsorbente), entonces , y obtenemos una expresión para una línea recta:
A través de su pendiente y la intersección con y podemos obtener vmon y K, que son constantes para cada par adsorbente-adsorbato a una temperatura dada. vmon está relacionado con el número de sitios de adsorción a través de la ley de los gases ideales. Si asumimos que el número de sitios es solo el área completa del sólido dividida en la sección transversal de las moléculas de adsorbato, podemos calcular fácilmente el área de superficie del adsorbente. La superficie de un adsorbente depende de su estructura: cuantos más poros tiene, mayor es el área, lo que tiene una gran influencia en las reacciones de las superficies.
Si más de un gas se adsorbe en la superficie, definimos como la fracción de sitios vacíos, y tenemos:
Además, podemos definir como la fracción de los sitios ocupados por el j-ésimo gas:
donde i es cada uno de los gases que se adsorben.
Notas:
1) Para elegir entre las ecuaciones de Langmuir y Freundlich, se deben investigar las entalpías de adsorción.[11] Mientras que el modelo de Langmuir asume que la energía de adsorción permanece constante con la ocupación de la superficie, la ecuación de Freundlich se deriva con el supuesto de que el calor de adsorción disminuye continuamente a medida que se ocupan los sitios de unión.[12] La elección del modelo basado en el mejor ajuste de los datos es un error común.[11]
2) El uso de la forma linealizada del modelo de Langmuir ya no es una práctica común. Los avances en el poder computacional permitieron que la regresión no lineal se realizara rápidamente y con mayor confianza, ya que no se requiere transformación de datos.
BET[editar]
A menudo, las moléculas forman multicapas, es decir, algunas se adsorben en moléculas ya adsorbidas y la isoterma de Langmuir no es válida. En 1938, Stephen Brunauer, Paul Emmett y Edward Teller desarrollaron un modelo de isoterma que tiene en cuenta esa posibilidad. Su teoría se llama teoría BET, después de las iniciales de sus apellidos. Modificaron el mecanismo de Langmuir de la siguiente manera:
- A (g) + S ⇌ AS,
- A (g) + AS ⇌ A 2 S,
- A (g) + A 2 S ⇌ A 3 S y así sucesivamente.

La derivación de la fórmula es más complicada que la de Langmuir (consulte los enlaces para obtener una derivación completa). Obtenemos:
donde x es la presión dividida por la presión de vapor para el adsorbato a esa temperatura (generalmente denotado ), v es el volumen STP de adsorbato adsorbido, v mon es el volumen STP de la cantidad de adsorbato requerido para formar una monocapa y c es la constante de equilibrio K que usamos en la isoterma de Langmuir multiplicada por la presión de vapor del adsorbato. El supuesto clave utilizado para derivar la ecuación BET es que los sucesivos calores de adsorción para todas las capas excepto la primera son iguales al calor de condensación del adsorbato.
La isoterma de Langmuir suele ser mejor para la quimisorción y la isoterma BET funciona mejor para la fisisorción de superficies no microporosas.
Kisliuk[editar]

En otros casos, las interacciones moleculares entre moléculas de gas previamente adsorbidas en una superficie sólida forman interacciones significativas con moléculas de gas en las fases gaseosas. Por lo tanto, es más probable que la adsorción de moléculas de gas a la superficie ocurra alrededor de moléculas de gas que ya están presentes en la superficie sólida, lo que hace que la isoterma de adsorción de Langmuir sea ineficaz a los efectos del modelado. Este efecto fue estudiado en un sistema donde el nitrógeno era el adsorbato y el tungsteno el adsorbente por Paul Kisliuk (1922-2008) en 1957.[13] Para compensar la mayor probabilidad de que se produzca adsorción alrededor de las moléculas presentes en la superficie del sustrato, Kisliuk desarrolló la teoría del estado precursor, según la cual las moléculas entrarían en un estado precursor en la interfaz entre el adsorbente sólido y el adsorbato en la fase gaseosa. A partir de aquí, las moléculas de adsorbato se adsorberían al adsorbente o se desorbirían en la fase gaseosa. La probabilidad de que la adsorción se produzca a partir del estado precursor depende de la proximidad del adsorbato a otras moléculas de adsorbato que ya se han adsorbido. Si la molécula de adsorbato en el estado precursor está muy cerca de una molécula de adsorbato que ya se ha formado en la superficie, tiene una probabilidad de adherencia reflejada por el tamaño de la constante SE y será adsorbida del estado precursor a una velocidad de kEC o se desorberá en la fase gaseosa a una tasa de kES. Si una molécula de adsorbato entra en el estado precursor en un lugar que está alejado de cualquier otras moléculas de adsorbato previamente adsorbidos, la probabilidad de que se pega se refleja por el tamaño de la constante S D.
Estos factores se incluyeron como parte de una única constante denominada "coeficiente de adherencia", kE, que se describe a continuación:
Como SD está dictado por factores que se tienen en cuenta en el modelo de Langmuir, se puede suponer que S D es la constante de velocidad de adsorción. Sin embargo, la constante de velocidad para el modelo de Kisliuk (R') es diferente de la del modelo de Langmuir, ya que R' se usa para representar el impacto de la difusión en la formación de monocapa y es proporcional a la raíz cuadrada del coeficiente de difusión del sistema. La isoterma de adsorción de Kisliuk se escribe de la siguiente manera, donde θ(t) es la cobertura fraccional del adsorbente con adsorbato y t es el tiempo de inmersión:
Resolviendo para θ(t) se obtiene:
Entalpía de adsorción[editar]
Las constantes de adsorción son constantes de equilibrio, por lo que obedecen a la ecuación de van't Hoff:
Como puede observarse en la fórmula, la variación de K debe ser isostérica, es decir, con cobertura constante. Si partimos de la isoterma BET y asumimos que el cambio de entropía es el mismo para licuefacción y adsorción, obtenemos
es decir, la adsorción es más exotérmica que la licuefacción.
Explicación de una sola molécula[editar]
La adsorción de un conjunto de moléculas en una superficie o interfaz se puede dividir en dos procesos: adsorción y desorción. Si la tasa de adsorción gana la tasa de desorción, las moléculas se acumularán con el tiempo dando la curva de adsorción con el tiempo. Si la tasa de desorción es mayor, el número de moléculas en la superficie disminuirá con el tiempo. La tasa de adsorción depende de la temperatura, la tasa de difusión del soluto y la barrera de energía entre la molécula y la superficie. La difusión y los elementos clave de la tasa de adsorción se pueden calcular utilizando las leyes de difusión de Fick y la relación de Einstein (teoría cinética). La desorción de una molécula de la superficie depende de la energía de unión de la molécula a la superficie y de la temperatura.
Mecánica cuántica: modelado termodinámico para área de superficie y porosidad[editar]
Desde 1980 se trabajaron dos teorías para explicar la adsorción y obtener ecuaciones que funcionen. Estos dos se conocen como la hipótesis chi, la derivación mecánica cuántica y el exceso de trabajo superficial, ESW.[14] Ambas teorías producen la misma ecuación para superficies planas:
Donde U es la función de paso unitario. Las definiciones de los otros símbolos son las siguientes:
donde "ads" significa "adsorbido", "m" significa "equivalencia de monocapa" y "vap" es una referencia a la presión de vapor del adsorbente líquido a la misma temperatura que la muestra sólida. La función unitaria crea la definición de la energía molar de adsorción para la primera molécula adsorbida mediante:
La trama de adsorbido versus se conoce como la gráfica chi. Para superficies planas, la pendiente de la gráfica chi produce el área de superficie. Empíricamente, Polanyi[15][16] y también deBoer y Zwikker[17] notaron que esta trama encajaba muy bien con la isoterma, pero no la siguieron. Esto se debió a las críticas en el primer caso de Einstein y en el segundo de Brunauer. Esta ecuación de superficie plana puede usarse como una "curva estándar" en la tradición normal de curvas de comparación, con la excepción de que la parte inicial de la muestra porosa de la gráfica de versus actúa como un estándar propio. Las condiciones ultramicroporosas, microporosas y mesoporosas pueden analizarse utilizando esta técnica. Las desviaciones estándar típicas para ajustes de isotermas completos, incluidas las muestras porosas, suelen ser inferiores al 2 %.
Observe que en esta descripción de la adsorción física, la entropía de adsorción es consistente con el criterio termodinámico de Dubinin, es decir, la entropía de adsorción desde el estado líquido al estado adsorbido es aproximadamente cero.
Adsorbentes[editar]
Características y requisitos generales[editar]

Los adsorbentes se utilizan generalmente en forma de gránulos esféricos, varillas, molduras o monolitos con un radio hidrodinámico entre 0,25 y 5 mm. Deben tener una alta resistencia a la abrasión, alta estabilidad térmica y pequeños diámetros de poro, lo que da como resultado una mayor superficie expuesta y, por lo tanto, una alta capacidad de adsorción. Los adsorbentes también deben tener una estructura de poros distinta que permita el transporte rápido de los vapores gaseosos.
La mayoría de los adsorbentes industriales se dividen en tres clases:
- Compuestos que contienen oxígeno: son típicamente hidrófilos y polares, incluidos materiales como gel de sílice y zeolitas.
- Compuestos a base de carbono: suelen ser hidrófobos y no polares, incluidos materiales como el carbón activado y el grafito.
- Compuestos a base de polímeros: son polares o no polares, según los grupos funcionales de la matriz del polímero.
Gel de sílice[editar]

El gel de sílice es químicamente inerte, no tóxico, polar y dimensionalmente estable (< 400 grados Celsius (752 °F) ) forma amorfa de SiO2. Se prepara mediante la reacción entre silicato de sodio y ácido acético, a la que sigue una serie de procesos de postratamiento como envejecimiento, decapado, etc. Estos métodos de postratamiento dan como resultado varias distribuciones de tamaño de poro.
La sílice se utiliza para secar el aire de proceso (por ejemplo, oxígeno, gas natural) y adsorber hidrocarburos pesados (polares) del gas natural.
Zeolitas[editar]
Las zeolitas son aluminosilicatos cristalinos naturales o sintéticos, que tienen una red de poros repetidos y liberan agua a alta temperatura. Las zeolitas son de naturaleza polar.
Se fabrican mediante síntesis hidrotermal de aluminosilicato de sodio u otra fuente de sílice en un autoclave seguido de intercambio iónico con ciertos cationes (Na+, Li+, Ca2+, K+, NH4+). El diámetro del canal de las jaulas de zeolita suele oscilar entre 2 y 9 Å. El proceso de intercambio iónico va seguido del secado de los cristales, que pueden granularse con un aglutinante para formar gránulos macroporosos.
Las zeolitas se aplican en el secado de aire de proceso, eliminación de CO2 del gas natural, eliminación de CO del gas de reformado, separación de aire, craqueo catalítico y síntesis y reformado catalítico.
Las zeolitas no polares (silíceas) se sintetizan a partir de fuentes de sílice sin aluminio o mediante desaluminación de zeolitas que contienen aluminio. El proceso de desaluminación se realiza tratando la zeolita con vapor a temperaturas elevadas, típicamente superiores a 500 grados Celsius (932 °F). Este tratamiento térmico a alta temperatura rompe los enlaces aluminio-oxígeno y el átomo de aluminio es expulsado de la estructura de la zeolita.
Carbón activado[editar]
El carbón activado es un sólido amorfo muy poroso que consta de microcristalitos con una red de grafito, generalmente preparado en pequeños gránulos o en polvo. Es no polar y barato. Uno de sus principales inconvenientes es que reacciona con el oxígeno a temperaturas moderadas (más de 300 °C).

El carbón activado se puede fabricar a partir de material carbonoso, incluido carbón (bituminoso, subbituminoso y lignito), turba, madera o cáscaras de nueces (por ejemplo, coco). El proceso de fabricación consta de dos fases, carbonización y activación.[18] El proceso de carbonización incluye el secado y luego el calentamiento para separar los subproductos, incluidos los alquitranes y otros hidrocarburos de la materia prima, así como para expulsar los gases generados. El proceso se completa calentando el material a más de 400 grados Celsius (752 °F) en una atmósfera libre de oxígeno que no puede soportar la combustión. Las partículas carbonizadas se "activan" exponiéndolas a un agente oxidante, normalmente vapor o dióxido de carbono a alta temperatura. Este agente quema las estructuras de bloqueo de poros creadas durante la fase de carbonización y, por lo tanto, desarrollan una estructura reticular de grafito tridimensional y porosa. El tamaño de los poros que se desarrollan durante la activación es función del tiempo que pasan en esta etapa. Los tiempos de exposición más largos dan como resultado tamaños de poro más grandes. Los carbones de fase acuosa más populares son de base bituminosa debido a su dureza, resistencia a la abrasión, distribución del tamaño de los poros y bajo costo, pero su efectividad debe probarse en cada aplicación para determinar el producto óptimo.
El carbón activado se utiliza para la adsorción de sustancias orgánicas[19] y adsorbatos no polares y también se suele utilizar para el tratamiento de gases residuales (y aguas residuales). Es el adsorbente más utilizado, ya que la mayoría de sus propiedades químicas (por ejemplo, grupos de superficie) y físicas (por ejemplo, distribución del tamaño de los poros y área de la superficie) se pueden ajustar de acuerdo con lo que se necesite. Su utilidad también se deriva de su gran volumen de microporos (ya veces mesoporos) y la gran superficie resultante.
Adsorción de agua[editar]
La adsorción de agua en las superficies es de gran importancia en la ingeniería química, la ciencia de los materiales y la catálisis. También denominada hidratación de la superficie, la presencia de agua adsorbida física o químicamente en las superficies de los sólidos juega un papel importante en el control de las propiedades de la interfaz, las vías de reacción química y el desempeño catalítico en una amplia gama de sistemas. En el caso del agua adsorbida físicamente, la hidratación de la superficie se puede eliminar simplemente mediante el secado en condiciones de temperatura y presión que permitan la vaporización total del agua. Para el agua adsorbida químicamente, la hidratación puede ser en forma de adsorción disociativa, donde las moléculas de H2O se disocian en -H y -OH adsorbidas en la superficie, o adsorción molecular (adsorción asociativa) donde las moléculas de agua individuales permanecen intactas[20]
Calefacción y almacenamiento solar por adsorción[editar]
El bajo costo ($ 200/tonelada) y la alta tasa de ciclo (2,000 ×) de las zeolitas sintéticas como Linde 13X con adsorbato de agua han ganado mucho interés académico y comercial recientemente para su uso para almacenamiento de energía térmica (TES), específicamente de energía solar de bajo grado de desperdicio de calor. Se han financiado varios proyectos piloto en la UE desde 2000 hasta el 2020. El concepto básico es almacenar energía solar térmica como energía química latente en la zeolita. Normalmente, se hace que el aire seco caliente de los colectores solares de placa plana fluya a través de un lecho de zeolita de manera que se elimine cualquier adsorbato de agua presente. El almacenamiento puede ser diurno, semanal, mensual o incluso estacional según el volumen de zeolita y el área de los paneles solares térmicos. Cuando se necesita calor durante la noche, las horas sin sol o el invierno, el aire humidificado fluye a través de la zeolita. A medida que la zeolita adsorbe la humedad, el calor se libera al aire y, posteriormente, al espacio del edificio. Esta forma de TES, con uso específico de zeolitas, fue enseñada por Guerra por primera vez en 1978.[21]
Captura y almacenamiento de carbono[editar]
Los adsorbentes típicos propuestos para la captura y almacenamiento de carbono son zeolitas y MOF.[22] La personalización de los adsorbentes los convierte en una alternativa potencialmente atractiva a la absorción. Debido a que los adsorbentes se pueden regenerar por cambios de temperatura o presión, este paso puede requerir menos energía que los métodos de regeneración por absorción.[23] Los principales problemas que están presentes con el costo de adsorción en la captura de carbono son: regeneración del adsorbente, relación de masa, solvente/MOF, costo del adsorbente, producción del adsorbente, vida útil del adsorbente.[24]
Adsorción de proteínas y tensoactivos[editar]
La adsorción de proteínas es un proceso que tiene un papel fundamental en el campo de los biomateriales. De hecho, las superficies de biomateriales en contacto con medios biológicos, como sangre o suero, se recubren inmediatamente de proteínas. Por tanto, las células vivas no interactúan directamente con la superficie del biomaterial, sino con la capa de proteínas adsorbidas. Esta capa de proteína media la interacción entre biomateriales y células, traduciendo las propiedades físicas y químicas de los biomateriales a un "lenguaje biológico".[25] De hecho, los receptores de la membrana celular se unen a los sitios bioactivos de la capa de proteína y estos eventos de unión del receptor a la proteína se transducen, a través de la membrana celular, de una manera que estimula procesos intracelulares específicos que luego determinan la adhesión, forma, crecimiento y diferenciación celular. La adsorción de proteínas está influenciada por muchas propiedades de la superficie, como la humectabilidad de la superficie, la composición química de la superficie[26] y la morfología de la superficie a escala nanométrica.[27] La adsorción de surfactante es un fenómeno similar, pero utiliza moléculas de surfactante en lugar de proteínas.[28]
Enfriadores de adsorción[editar]
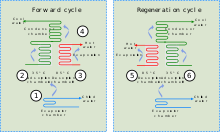
Al combinar un adsorbente con un refrigerante, los enfriadores de adsorción utilizan calor para proporcionar un efecto de enfriamiento. Este calor, en forma de agua caliente, puede provenir de cualquier número de fuentes industriales, incluido el calor residual de los procesos industriales, el calor primario de las instalaciones térmicas solares o del calor de escape o de la camisa de agua de un motor de pistón o turbina.
Aunque existen similitudes entre los enfriadores de adsorción y la refrigeración por absorción, el primero se basa en la interacción entre gases y sólidos. La cámara de adsorción del enfriador está llena de un material sólido (por ejemplo, zeolita, gel de sílice, alúmina, carbón activo o ciertos tipos de sales metálicas), que en su estado neutro ha adsorbido el refrigerante. Cuando se calienta, el sólido desorbe (libera) vapor refrigerante, que posteriormente se enfría y licúa. Este refrigerante líquido proporciona un efecto de enfriamiento en el evaporador a partir de su entalpía de vaporización. En la etapa final, el vapor refrigerante se (re)adsorbe en el sólido.[29] Como un enfriador de adsorción no requiere compresor, es relativamente silencioso.
Adsorción mediada por el sitio del portal[editar]
La adsorción mediada por el sitio del portal es un modelo para la adsorción de gas activado selectivo del sitio en sistemas catalíticos metálicos que contienen una variedad de sitios de adsorción diferentes. En tales sistemas, los sitios similares a defectos de "borde y esquina" de baja coordinación pueden exhibir entalpías de adsorción significativamente más bajas que los sitios de alta coordinación (plano basal). Como resultado, estos sitios pueden servir como "portales" para una adsorción muy rápida al resto de la superficie. El fenómeno se basa en el efecto de "desbordamiento" común (descrito a continuación), en el que ciertas especies adsorbidas exhiben una gran movilidad en algunas superficies. El modelo explica observaciones aparentemente inconsistentes de la termodinámica y cinética de adsorción de gas en sistemas catalíticos donde las superficies pueden existir en una variedad de estructuras de coordinación, y se ha aplicado con éxito a sistemas catalíticos bimetálicos donde se observa actividad sinérgica.
En contraste con el derrame puro, la adsorción en el sitio portal se refiere a la difusión de la superficie a los sitios de adsorción adyacentes, no a las superficies de soporte no adsorbentes.
El modelo parece haber sido propuesto por primera vez para el monóxido de carbono en platino con soporte de sílice por Brandt et al. (1993).[30] King y colaboradores[31][32][33] desarrollaron un modelo similar, pero independiente, para describir la adsorción de hidrógeno en catalizadores bimetálicos de rutenio, plata-rutenio y cobre-rutenio promovidos por álcalis. El mismo grupo aplicó el modelo a la hidrogenación de CO (síntesis de Fischer-Tropsch).[34] Zupanc y col. (2002) posteriormente confirmaron el mismo modelo para la adsorción de hidrógeno en catalizadores bimetálicos de cesio-rutenio soportados por magnesia.[35] Trens y col. (2009) han descrito de manera similar la difusión de CO en la superficie en partículas de Pt soportadas por carbono de morfología variable.[36]
Derrame de adsorción[editar]
En el caso de sistemas catalíticos o adsorbentes en los que una especie de metal se dispersa sobre un material de soporte (o portador) (a menudo óxidos cuasi-inertes, como alúmina o sílice), es posible que una especie adsorbente adsorba indirectamente a la superficie del soporte debajo condiciones en las que dicha adsorción es termodinámicamente desfavorable. La presencia del metal sirve como una vía de menor energía para que las especies gaseosas se adsorban primero en el metal y luego se difundan en la superficie de soporte. Esto es posible porque la especie adsorbida alcanza un estado de energía más bajo una vez que se ha adsorbido al metal, disminuyendo así la barrera de activación entre la especie en fase gaseosa y la especie adsorbida por soporte.
El derrame de hidrógeno es el ejemplo más común de un derrame por adsorción. En el caso del hidrógeno, la adsorción suele ir acompañada de la disociación del hidrógeno molecular (H2) en hidrógeno atómico (H), seguida de un desbordamiento de los átomos de hidrógeno presentes.
El efecto de derrame se ha utilizado para explicar muchas observaciones en catálisis y adsorción heterogéneas.[37]
Adsorción de polímeros[editar]
La adsorción de moléculas en las superficies de los polímeros es fundamental para una serie de aplicaciones, incluido el desarrollo de revestimientos antiadherentes y en varios dispositivos biomédicos. Los polímeros también se pueden adsorber a las superficies mediante la adsorción de polielectrolitos.
Adsorción en virus[editar]
La adsorción es el primer paso en el ciclo de vida viral. Los siguientes pasos son la penetración, el desencubrimiento, la síntesis (transcripción si es necesario y traducción) y la liberación. El ciclo de replicación del virus, a este respecto, es similar para todos los tipos de virus. Factores como la transcripción pueden ser necesarios o no si el virus es capaz de integrar su información genómica en el núcleo de la célula, o si el virus puede replicarse directamente dentro del citoplasma de la célula.
En la cultura popular[editar]
El juego de Tetris es un juego de rompecabezas en el que bloques de 4 se adsorben en una superficie durante el juego. Los científicos han utilizado bloques de Tetris "como proxy de moléculas con una forma compleja" y su "adsorción en una superficie plana" para estudiar la termodinámica de nanopartículas.[38][39]
Véase también[editar]
- Adatom
- Crio-adsorción
- Interferometría de polarización dual
- Concentrador de lecho fluidizado
- Microscopio de fuerza de sonda Kelvin
- Micromeritics
- Tamiz molecular
- Adsorción de Polanyi
- Adsorción por oscilación de presión
- Adsorción secuencial aleatoria
Referencias[editar]
- ↑ «Glossary of atmospheric chemistry terms (Recommendations 1990)». Pure and Applied Chemistry (en inglés) 62: 2167. 1990. ISBN 0-9678550-9-8. doi:10.1351/goldbook.A00155.
- ↑ «Glossary». The Brownfields and Land Revitalization Technology Support Center. Archivado desde el original el 18 de febrero de 2008. Consultado el 21 de diciembre de 2009.
- ↑ «absorption (chemistry)». Memidex (WordNet) Dictionary/Thesaurus. Archivado desde el original el 5 de octubre de 2018. Consultado el 2 de noviembre de 2010.
- ↑ Atkins, P. W.; De Paula, Julio; Keeler, James (2018). Atkins' Physical chemistry (Eleventh edición). Oxford, United Kingdom. ISBN 978-0-19-876986-6. OCLC 1020028162.
- ↑ Ferrari, L.; Kaufmann, J.; Winnefeld, F.; Plank, J. (2010). «Interaction of cement model systems with superplasticizers investigated by atomic force microscopy, zeta potential, and adsorption measurements». J. Colloid Interface Sci. 347 (1): 15-24. Bibcode:2010JCIS..347...15F. PMID 20356605. doi:10.1016/j.jcis.2010.03.005.
- ↑ Czelej, K.; Cwieka, K.; Kurzydlowski, K.J. (May 2016). «CO2 stability on the Ni low-index surfaces: Van der Waals corrected DFT analysis». Catalysis Communications 80 (5): 33-38. doi:10.1016/j.catcom.2016.03.017.
- ↑ Czelej, K.; Cwieka, K.; Colmenares, J.C.; Kurzydlowski, K.J. (2016). «Insight on the Interaction of Methanol-Selective Oxidation Intermediates with Au- or/and Pd-Containing Monometallic and Bimetallic Core@Shell Catalysts». Langmuir 32 (30): 7493-7502. PMID 27373791. doi:10.1021/acs.langmuir.6b01906.
- ↑ Kayser, Heinrich (1881). «Über die Verdichtung von Gasen an Oberflächen in ihrer Abhängigkeit von Druck und Temperatur». Annalen der Physik und Chemie 248 (4): 526-537. Bibcode:1881AnP...248..526K. doi:10.1002/andp.18812480404.. In this study of the adsorption of gases by charcoal, the first use of the word "adsorption" appears on page 527: "Schon Saussure kannte die beiden für die Grösse der Adsorption massgebenden Factoren, den Druck und die Temperatur, da er Erniedrigung des Druckes oder Erhöhung der Temperatur zur Befreiung der porösen Körper von Gasen benutzte." ("Saussaure already knew the two factors that determine the quantity of adsorption – [namely,] the pressure and temperature – since he used the lowering of the pressure or the raising of the temperature to free the porous substances of gases.")
- ↑ Foo, K. Y.; Hameed, B. H. (2010). «Insights into the modeling of adsorption isotherm systems». Chemical Engineering Journal 156 (1): 2-10. ISSN 1385-8947. doi:10.1016/j.cej.2009.09.013.
- ↑ Czepirski, L. (2000). «Some generalization of Langmuir adsorption isotherm». www.semanticscholar.org (en inglés). Consultado el 30 de diciembre de 2020.
- ↑ a b Burke GM, Wurster DE, Buraphacheep V, Berg MJ, Veng-Pedersen P, Schottelius DD. Model selection for the adsorption of phenobarbital by activated charcoal. Pharm Res. 1991;8(2):228‐231. doi:10.1023/a:1015800322286
- ↑ Physical Chemistry of Surfaces. Arthur W. Adamson. Interscience (Wiley), New York 6th ed
- ↑ Kisliuk, P. (1 de enero de 1957). «The sticking probabilities of gases chemisorbed on the surfaces of solids». Journal of Physics and Chemistry of Solids (en inglés) 3 (1): 95-101. ISSN 0022-3697. doi:10.1016/0022-3697(57)90054-9.
- ↑ Condon, James (2020). Surface Area and Porosity Determinations by Physisorption, Measurement, Classical Theory and Quantum Theory, 2nd edition. Amsterdam.NL: Elsevier. pp. Chapters 3, 4 and 5. ISBN 978-0-12-818785-2.
- ↑ Polanyi, M. (1920). «Neueres über Adsorption und Ursache der Adsorptionskräfte». Zeitschrift für Elektrochemie 26: 370-374.
- ↑ Polanyi, M. (1929). «Grundlagen der Potentialtheorie der Adsorption». Zeitschrift für Elektrochemie 35: 431-432.
- ↑ deBoer, J.H.; Zwikker, C. (1929). «Adsorption als Folge von Polarisation». Zeitschrift für Physikalische Chemie. B3: 407-420.
- ↑ Spessato, L. et al. KOH-super activated carbon from biomass waste: Insights into the paracetamol adsorption mechanism and thermal regeneration cycles. Journal of Hazardous Materials, Vol. 371, Pages 499-505, 2019.
- ↑ Malhotra, Milan; Suresh, Sumathi; Garg, Anurag (2018). «Tea waste derived activated carbon for the adsorption of sodium diclofenac from wastewater: adsorbent characteristics, adsorption isotherms, kinetics, and thermodynamics». Environmental Science and Pollution Research 25 (32): 32210-32220. PMID 30221322. doi:10.1007/s11356-018-3148-y.
- ↑ Adsorption of water at TiO2 planes, dissociative vs molecular water adsorption.
- ↑ U.S. Pat. No. 4,269,170, "Adsorption solar heating and storage"; Inventor: John M. Guerra; Granted May 26, 1981
- ↑ Berend, Smit; Reimer, Jeffery A; Oldenburg, Curtis M; Bourg, Ian C (2014). Introduction to carbon capture and sequestration. Imperial College Press. ISBN 9781306496834.
- ↑ D'Alessandro, Deanna M.; Smit, Berend; Long, Jeffrey R. (16 de agosto de 2010). «Carbon Dioxide Capture: Prospects for New Materials». Angewandte Chemie International Edition (en inglés) 49 (35): 6058-82. ISSN 1521-3773. PMID 20652916. doi:10.1002/anie.201000431.
- ↑ Sathre, Roger; Masanet, Eric (18 de marzo de 2013). «Prospective life-cycle modeling of a carbon capture and storage system using metal–organic frameworks for CO2 capture». RSC Advances 3 (15): 4964. ISSN 2046-2069. doi:10.1039/C3RA40265G.
- ↑ Wilson, CJ; Clegg, RE; Leavesley, DI; Pearcy, MJ (2005). «Mediation of Biomaterial-Cell Interactions by Adsorbed Proteins: A Review». Tissue Engineering 11 (1): 1-18. PMID 15738657. doi:10.1089/ten.2005.11.1.
- ↑ Sivaraman B.; Fears K.P.; Latour R.A. (2009). «Investigation of the effects of surface chemistry and solution concentration on the conformation of adsorbed proteins using an improved circular dichroism method». Langmuir 25 (5): 3050-6. PMC 2891683. PMID 19437712. doi:10.1021/la8036814.
- ↑ Scopelliti, Pasquale Emanuele; Borgonovo, Antonio; Indrieri, Marco; Giorgetti, Luca; Bongiorno, Gero; Carbone, Roberta; Podestà, Alessandro; Milani, Paolo (2010). «The effect of surface nanometre-scale morphology on protein adsorption». En Zhang, Shuguang, ed. PLoS ONE 5 (7): e11862. Bibcode:2010PLoSO...511862S. PMC 2912332. PMID 20686681. doi:10.1371/journal.pone.0011862.
- ↑ Cheraghian, Goshtasp (2017). «Evaluation of Clay and Fumed Silica Nanoparticles on Adsorption of Surfactant Polymer during Enhanced Oil Recovery». Journal of the Japan Petroleum Institute 60 (2): 85-94. doi:10.1627/jpi.60.85.
- ↑ Pilatowsky, I.; Romero, R.J.; Isaza, C.A.; Gamboa, S.A.; Sebastian, P.J.; Rivera, W. (2011). «Chapter 5: Sorption Refrigeration Systems». Cogeneration Fuel Cell-Sorption Air Conditioning Systems. Green Energy and Technology. Springer. pp. 99, 100. ISBN 978-1-84996-027-4. doi:10.1007/978-1-84996-028-1_5.
- ↑ Brandt, Robert K.; Hughes, M. R.; Bourget, L. P.; Truszkowska, K.; Greenler, Robert G. (20 de abril de 1993). «The interpretation of CO adsorbed on Pt/SiO2 of two different particle-size distributions». Surface Science (en inglés) 286 (1): 15-25. ISSN 0039-6028. doi:10.1016/0039-6028(93)90552-U.
- ↑ Uner, D. O.; Savargoankar, N.; Pruski, M.; King, T. S. (1 de enero de 1997). Froment, G. F., ed. Studies in Surface Science and Catalysis. Dynamics of Surfaces and Reaction Kinetics in Heterogeneous Catalysis (en inglés) 109. Elsevier. pp. 315-324. doi:10.1016/s0167-2991(97)80418-1.
- ↑ Narayan, R. L; King, T. S (23 de marzo de 1998). «Hydrogen adsorption states on silica-supported Ru–Ag and Ru–Cu bimetallic catalysts investigated via microcalorimetry». Thermochimica Acta (en inglés) 312 (1): 105-114. ISSN 0040-6031. doi:10.1016/S0040-6031(97)00444-9.
- ↑ VanderWiel, David P.; Pruski, Marek; King, Terry S. (15 de noviembre de 1999). «A Kinetic Study on the Adsorption and Reaction of Hydrogen over Silica-Supported Ruthenium and Silver–Ruthenium Catalysts during the Hydrogenation of Carbon Monoxide». Journal of Catalysis (en inglés) 188 (1): 186-202. ISSN 0021-9517. doi:10.1006/jcat.1999.2646.
- ↑ Uner, D. O. (1 de junio de 1998). «A Sensible Mechanism of Alkali Promotion in Fischer−Tropsch Synthesis: Adsorbate Mobilities». Industrial & Engineering Chemistry Research 37 (6): 2239-2245. ISSN 0888-5885. doi:10.1021/ie970696d.
- ↑ Zupanc, C.; Hornung, A.; Hinrichsen, O.; Muhler, M. (25 de julio de 2002). «The Interaction of Hydrogen with Ru/MgO Catalysts». Journal of Catalysis (en inglés) 209 (2): 501-514. ISSN 0021-9517. doi:10.1006/jcat.2002.3647.
- ↑ Trens, Philippe; Durand, Robert; Coq, Bernard; Coutanceau, Christophe; Rousseau, Séverine; Lamy, Claude (9 de noviembre de 2009). «Poisoning of Pt/C catalysts by CO and its consequences over the kinetics of hydrogen chemisorption». Applied Catalysis B: Environmental (en inglés) 92 (3): 280-284. ISSN 0926-3373. doi:10.1016/j.apcatb.2009.08.004.
- ↑ Rozanov, Valerii V; Krylov, Oleg V (28 de febrero de 1997). «Hydrogen spillover in heterogeneous catalysis». Russian Chemical Reviews 66 (2): 107-119. ISSN 0036-021X. doi:10.1070/rc1997v066n02abeh000308.
- ↑ The Thermodynamics of Tetris, Ars Technica, 2009.
- ↑ Barnes, Brian C.; Siderius, Daniel W.; Gelb, Lev D. (2009). «Structure, Thermodynamics, and Solubility in Tetromino Fluids». Langmuir 25 (12): 6702-16. PMID 19397254. doi:10.1021/la900196b.
Otras lecturas[editar]
- Brandt, R. K.; Hughes, M. R.; Bourget, L. P.; Truszkowska, K.; Greenler, R. G. (1993). «The interpretation of CO adsorbed on Pt/SiO2 of two different particle-size distributions». Surface Science (en inglés) 286 (1–2): 15-25. Bibcode:1993SurSc.286...15B. doi:10.1016/0039-6028(93)90552-U.
- Kisliuk, P. (1957). «The sticking probabilities of gases chemisorbed on the surfaces of solids». Journal of Physics and Chemistry of Solids (en inglés) 3 (1–2): 95-101. Bibcode:1957JPCS....3...95K. doi:10.1016/0022-3697(57)90054-9.
- Narayan, R. L.; King, T. S. (1998). «Hydrogen adsorption states on silica-supported Ru-Ag and Ru-Cu bimetallic catalysts investigated via microcalorimetry». Thermochimica Acta (en inglés) 312 (1–2): 105-114. doi:10.1016/S0040-6031(97)00444-9.
- Rozanov, V. V.; Krylov, O. V. (1997). «Hydrogen spillover in heterogeneous catalysis». Russian Chemical Reviews (en inglés) 66 (2): 107-119. Bibcode:1997RuCRv..66..107R. doi:10.1070/RC1997v066n02ABEH000308.
- Czepirski, L.; Balys, M. R.; Komorowska-Czepirska, E. (2000). «Some generalization of Langmuir adsorption isotherm». Internet Journal of Chemistry 3 (14). ISSN 1099-8292. Archivado desde el original el 13 de enero de 2017. Consultado el 10 de enero de 2017.
- Trens, P.; Durand, R.; Coq, B.; Coutanceau, C.; Rousseau, S.; Lamy, C. (2009). «Poisoning of Pt/C catalysts by CO and its consequences over the kinetics of hydrogen chemisorption». Applied Catalysis B: Environmental (en inglés) 92 (3–4): 280-284. doi:10.1016/j.apcatb.2009.08.004.
- Uner, D. O.; Savargoankar, N.; Pruski, M.; King, T. S. (1997). «The effects of alkali promoters on the dynamics of hydrogen chemisorption and syngas reaction kinetics on Ru/SiO2 catalysts». Studies in Surface Science and Catalysis. Studies in Surface Science and Catalysis (en inglés) 109: 315-324. ISBN 9780444826091. doi:10.1016/S0167-2991(97)80418-1.
- Uner, D. O. (1998). «A sensible mechanism of alkali promotion in Fischer Tropsch synthesis:Adsorbate mobilities». Industrial and Engineering Chemistry Research (en inglés) 37 (6): 2239-2245. doi:10.1021/ie970696d.
- VanderWiel, D. P.; Pruski, M.; King, T. S. (1999). «A Kinetic Study of the Adsorption and Reaction of Hydrogen on Silica-Supported Ruthenium and Silver-Ruthenium Bimetallic Catalysts during the Hydrogenation of Carbon Monoxide». Journal of Catalysis (en inglés) 188 (1): 186-202. doi:10.1006/jcat.1999.2646.
- Zupanc, C.; Hornung, A.; Hinrichsen, O.; Muhler, M. (2002). «The Interaction of Hydrogen with Ru/MgO Catalysts». Journal of Catalysis (en inglés) 209 (2): 501-514. doi:10.1006/jcat.2002.3647.
Enlaces externos[editar]
- Derivation of Langmuir and BET isotherms, at JHU.edu
- Carbon Adsorption, at MEGTEC.com































