Sustitución nucleófila aromática
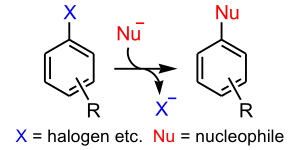
Una sustitución nucleófila aromática es un tipo de reacción de sustitución nucleófila en la que el nucleófilo desplaza a un buen grupo saliente, como un haluro, en un anillo aromático. Esto ocurre fácilmente cuando en las posiciones orto y para hay grupos tractores de Densidad electrónica fuertes con respecto al haluro. Se le da el nombre de sustitución nucleófila aromática porque un nucleófilo sustituye a un grupo saliente en un Anillo aromático.
En la sustitución nucleofílica aromática no interviene el mecanismo de reacción de la reacción de Sustitución nucleófilica , ya que los halogenuros de alquilo no pueden alcanzar la geometría correcta para un desplazamiento por el lado opuesto del alquilo. El anillo aromático bloquea el acercamiento del nucleófilo por detrás del carbono unido al halógeno.[1] Tampoco interviene el mecanismo , la sustitución nucleofílica aromática requiere nucleófilos muy fuertes, y la rapidez de reacción es proporcional a la concentración del nucleófilo, así que el nucleófilo interviene en el paso limitante de la rapidez de reacción.
Los sustituyentes atractores de densidad electrónica, como los grupos nitro, activan al anillo hacia la sustitución nucleofílica aromática, lo que parece indicar que en el estado de transición se está desarrollando una carga negativa en el anillo. De hecho, las sustituciones núcleofílicas aromáticas son difíciles cuando no hay por lo menos un grupo atractor de densidad electrónica fuerte. (Este efecto es lo contrario de la sustitución electrofílica aromática, donde los sustituyentes atractores de densidad electrónica desaceleran o detienen la reacción).[2]
Visión general[editar]
Existen diferentes mecanismos:
- Mecanismo de adición-eliminación:

Esta reacción, con este mecanismo, en el que el nucleófilo se adiciona a la posición del grupo saliente, el cual a continuación es eliminado recuperándose la aromaticidad, es la que se ha quedado con el nombre de sustitución nucleófila aromática (SNAr). Tiene lugar si existen grupos fuertemente atractores de electrones, típicamente grupos nitro (-NO2), en las posiciones orto y para al grupo saliente. Esto tiene dos efectos: consigue que el anillo sea menos rico en electrones, por tanto más susceptible a los ataques nucleófilos, y la estabilización por resonancia de la carga negativa del anión ciclohexadienilo intermedio. Esto hace que en cambio sean anillos aromáticos desactivados frente a la SEAr. Este es el caso también de un compuesto heteroaromático π-deficiente como la piridina, que está desactivada frente a la SEAr, pero que da reacciones de SNAr fácilmente.

- Mecanismo de eliminación-adición (vía bencino):

Sobre un haluro de arilo, la base fuerte arranca el protón contiguo al grupo saliente, produciéndose, a través de un anión fenilo intermedio ([C6H4-X]−), la eliminación de HX, lo que conduce al bencino. El bencino es inestable, de tal modo que inmediatamente el nucleófilo se adiciona por cualesquiera de ambos extremos de igual reactividad del triple enlace, dando lugar al producto.
- A través de sales de diazonio aromáticas:

Las sales de diazonio aromáticas, derivadas de la correspondiente anilina, son relativamente estables a baja temperatura, (baño de hielo, 0 °C), debido a la estabilización por resonancia. Al subir la temperatura se libera nitrógeno y se forma el catión arílico, que inmediatamente reacciona con cualquier nucleófilo presente.
Bibliografía[editar]
- K. Peter C. Vollhardt (1994). Química Orgánica. Barcelona: Ediciones Omega S.A. ISBN 84-282-0882-4.
- L. G. Wade Jr. (2011). Química Orgánica 2. México: Editorial Pearson Educación.


