N-bromosuccinimida
| N-bromosuccinimida | ||
|---|---|---|
| General | ||
| Fórmula estructural | Imagen de la estructura | |
| Fórmula molecular | ? | |
| Identificadores | ||
| Número CAS | 128-08-5[1] | |
| ChEBI | 53174 | |
| ChemSpider | 60528 | |
| PubChem | 67184 | |
| UNII | K8G1F2UCJF | |
| Propiedades físicas | ||
| Masa molar | 176,942540468 g/mol | |
La N-Bromosuccinimida o NBS, es un reactivo químico que es usado en sustitución radicalaria y reacciones de adición electrófila en Química orgánica. El NBS se puede considerar como una fuente de bromo.
Reacciones de la N-bromosuccinimida
[editar]Adición en alquenos
[editar]El NBS reacciona con alquenos en disoluciones acuosas para dar halohidrinas. Las condiciones preferibles son la adición del NBS al alqueno en una disolución acuosa al 50% de DMSO, DME, THF o tert-butanol a 0 °C. Se produce la formación del ion bromonio y el inmediato adición de agua Markownikoff y en anti.
También se forman α-bromo-cetonas y compuestos dibromados, que puede evitarse usando NBS cristalizado.
Con la adición de nucleófilos en vez de agua se pueden sintetizar varios alcanos bifuncionales.
Bromación alílica y bencílica
[editar]Las condiciones estándar para usar el NBS en bromación alílica y/o bencílica requiere que el NBS esté disuelto en anhidro CCl4 con un radical iniciador, generalmente azo-bis-isobutirilnitrilo (AIBN), peróxido de benzoilo, radiación o ambos efectos para conseguir una iniciación radicalaria. También es conocido como reacción de Wohl-Ziegler.
El CCl4 debe mantenerse en anhidro durante toda la reacción dado que la presencia de agua podría hidrolizar el producto deseado. El BaCO3 suele usarse para mantener condiciones de anhidro y libre de ácidos.
Bromación del carbonilo y derivados
[editar]El NBS puede α-bromar derivados carbonílicos bien vía radicalaria (imagen superior) o bien vía de catálisis ácida. Por ejemplo, el 1-clorohexanal puede bromarse en la posición α con NBS usando un ácido como catalizador.
La reacción con enoles, enoléteres o acetato de enoles con NBS es el método preferido de α-bromación gracias a que da pocos productos de mezcla.
Bromación de compuestos aromáticos
[editar]Los compuestos aromáticos pueden ser bromados usando NBS. Usar DMF como disolvente da grandes niveles de paraselectividad.
Transposición de Hofmann
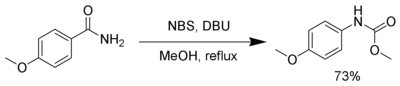
[editar]El NBS en presencia de una base fuerte, como por ejemplo DBU, reacciona con aminas primarias para producir carbamatos mediante la Transposición de Hofmann.
Oxidación selectiva de alcoholes
[editar]Aunque es poco común es posible que el NBS oxide alcoholes. Elias J. Corey descubrió que se puede oxidar alcoholes secundarios en presencia de alcoholes primarios en DME acuoso.
Preparación
[editar]En una disolución con agua helada bien removida de succinimida se le añade NaOH y después bromo. El producto, NBS, precipita y puede ser recogido por filtración. Para purificar el NBS puede recristalizarse con agua.

Purificación por recristalización
[editar]NBS impuro, ligeramente amarillo, puede dar resultados no deseados. Puede recristalizarse[2] del siguiente modo: en un matraz Erlenmeyer se disuelven 10 g de NBS en 125 mL de agua a 90-95 °C. Se agita hasta disolución total y se introduce en un baño de hielo. Se filtra a vacío y se deja secar al aire o haciendo fuerte vacío.
Precauciones
[editar]- Aunque el NBS es más fácil y seguro de usar que el bromo se debe evitar la inhalación.
- Debe guardarse en una nevera.
- El NBS se descompone con el tiempo liberando bromo.
- El NBS puro es blanco, aunque a menudo se puede encontrar blanco apagado o algo marrón debido al bromo.
- En general las reacciones con NBS son exotérmicas.
- Además deben tenerse especial precaución cuando es usado en abundancia.
Referencias
[editar]- ↑ Número CAS
- ↑ L. Kohnen, Amanda; R. Dunetz, Joshua; L. Danheiser, Rick (2007). «Synthesis of ynamides by n-alkynylation of amine derivatives. Preparation of n-allyl-n- (methoxycarbonyl) -1,3-decadiynylamine». Organic Syntheses (Organic Syntheses, Inc.) 84: 88. doi:10.15227/orgsyn.084.0088. Consultado el 13 de diciembre de 2022.