Lesión del ligamento cruzado anterior
| Lesión del ligamento cruzado anterior | ||
|---|---|---|
 Dibujo de la rodilla derecha | ||
| Especialidad | Traumatología | |
| Síntomas | Chasquido acompañado de dolor, inestabilidad e hinchazón de la rodilla[1] | |
| Causas | Lesión sin contacto, lesión por contacto directo[2] | |
| Factores de riesgo | Deportistas, sexo femenino[1] | |
| Diagnóstico | Exploración física, RM[1] | |
| Prevención | Entrenamiento neuromuscular,[3] fortalecimiento del tronco[4] | |
| Tratamiento | Dispositivos ortopédicos, fisioterapia, cirugía[1] | |
| Frecuencia | aprox. 200 000 al año (EE. UU.)[2] | |
La lesión del ligamento cruzado anterior se produce cuando el ligamento cruzado anterior (LCA) se distiende o se desgarra parcial o completamente.[1] La lesión más habitual es el desgarro completo.[1] Los síntomas de la rotura del LCA son dolor, un chasquido en el momento de la lesión, inestabilidad de la rodilla e hinchazón de la articulación,[1] que suele instaurarse en las dos horas posteriores a la lesión.[2] En la mitad de los casos aproximadamente, también se dañan otras estructuras de la rodilla, como los ligamentos circundantes, el cartílago o el menisco[1]
Entre los mecanismos causantes más frecuentes se encuentran un cambio rápido de dirección, una parada brusca, la caída tras un salto o un impacto directo contra la rodilla.[1] Es más común en deportistas, en particular en aquellos que practican esquí alpino, fútbol, fútbol americano o baloncesto.[1][5] Por lo general, el diagnóstico se realiza mediante una exploración física y, a veces, se complementa con imágenes de resonancia magnética (RM).[1] En la exploración física, a menudo, se observa dolor, disminución del rango de movimiento y aumento en la laxitud de la rodilla.[6]
La prevención de la lesión se consigue mediante el entrenamiento neuromuscular y el'''fortalecimiento del tronco'''[3][4] La elección del tratamiento dependen del nivel de actividad del paciente.[1] En pacientes con previsión de nivel bajo de actividad física puede ser suficiente el tratamiento no quirúrgico, que incluye '''dispositivos ortopédicos''' y fisioterapia.[1] Sin embargo, en personas con altos niveles de actividad se suele recomendar la reparación quirúrgica mediante la reconstrucción artroscópica del ligamento cruzado anterior.[1] La reconstrucción consiste en el reemplazo con un tendón obtenido en otra parte del cuerpo o procedente de un cadáver.[6] Tras la operación, la rehabilitación incluye incrementos progresivos del rango de movimiento de la articulación y el fortalecimiento de los músculos alrededor de la rodilla.[1] En los casos en los que se indica el tratamiento quirúrgico, éste no se lleva a cabo hasta que la inflamación ha remitido.[1]
En Estados Unidos unas 200.000 personas al año se ven afectadas por esta lesión.[2] En algunos deportes, las mujeres presentan un mayor riesgo de lesión del LCA, mientras que en otros deportes la distribución por sexos es similar.[5][7] Aunque los adultos con un desgarro completo presentan mayor tasa de osteoartritis de rodilla, no se ha comprobado que la elección terapéutica modifique el riesgo de sufrir dicha complicación.[8]
Signos y síntomas[editar]
Ante una lesión del LCA es común oír un chasquido en la rodilla seguido de dolor e hinchazón. Además, puede aparecer inestabilidad en la rodilla al reanudar la marcha y hacer otras actividades pues el ligamento ya no puede estabilizar la articulación de la rodilla ni evitar que la tibia se desplace hacia adelante.[9]
Otros signos habituales de una lesión aguda del LCA son la disminución del rango de movimiento de la rodilla y el dolor a lo largo de la línea articular. El dolor y la hinchazón pueden desaparecer por sí solos; sin embargo, la rodilla permanecerá inestable y reanudar la actividad deportiva sin tratamiento puede agravar los daños en la articulación.[1]
Causas[editar]

Las principales causas son:
- Un cambio rápido de dirección (también conocido como "fintar")
- Una caída en mala posición tras un salto
- Una parada brusca en carrera
- Un impacto directo o colisión contra la rodilla (p. ej., durante una entrada de fútbol o el choque en un vehículo)[1]
Estos movimientos hacen que la tibia se separe del fémur rápidamente, ejerciendo presión sobre la articulación de la rodilla, lo que favorece la ruptura del LCA. Alrededor del 80% de las lesiones del LCA ocurren sin traumatismo directo.[10] Algunos de los factores de riesgo son: la anatomía femenina, determinados deportes, una mala condición física, la fatiga y practicar deporte en un campo de césped.[11]
Predominio femenino[editar]
Las deportistas tienen de dos a ocho veces más probabilidades de lesionarse el LCA en deportes que incluyen fintas y saltos, en comparación con los hombres que practican esos mismos deportes.[12] A continuación se muestran los datos de la NCAA sobre la tasa relativa de lesión por cada 1 000 exposiciones/atleta
- Baloncesto masculino: 0,07; baloncesto femenino: 0,23
- Lacrosse masculino 0,12; lacrosse femenino 0,17
- Fútbol masculino 0,09; fútbol femenino 0,28
La gimnasia era el deporte que presentaba los valores más altos de lesión del LCA en mujeres, con una tasa de lesión de 0,33 por cada 1000 exposiciones/ deportista. De los cuatro deportes con la tasa más alta de lesión del LCA, tres eran femeninos: gimnasia, baloncesto y fútbol.[13]
Las diferencias entre hombres y mujeres que se han identificado como posibles causas son: la protección muscular activa de la articulación de la rodilla, las diferencias en la alineación de la pierna/pelvis y la laxitud relativa de los ligamentos. causada por las diferencias en la actividad hormonal del estrógeno y la relaxina.[12][14] Parece que las píldoras anticonceptivas disminuyen el riesgo de lesión.[15]
Teorías de la dominancia[editar]

En algunos estudios se ha planteado la existencia de cuatro desequilibrios neuromusculares que predisponen al sexo femenino a presentar mayor incidencia de lesión del LCA. En el caso de las deportistas es más probable que, tras un salto, caigan con las rodillas relativamente rectas e inclinadas hacia dentro, mientras que la mayor parte del peso corporal recae sobre un pie y el tronco se inclina hacia un lado.[16] Se han planteado diferentes teorías para explicar estos desequilibrios. Entre ellas se encuentran las teorías de la dominancia ligamentosa, de la dominancia del cuádriceps, de la dominancia de una pierna y de la dominancia del tronco.
Según la teoría de la dominancia ligamentosa, cuando una deportista cae tras un salto, su musculatura no absorbe suficientemente la energía del impacto contra el suelo y son los ligamentos de la rodilla los que deben absorber la fuerza, lo que aumenta el riesgo de lesión.[17] La dominancia del cuádriceps hace referencia a que en las deportistas el músculo del cuádriceps es el principal responsable de estabilizar la rodilla.[17] Puesto que la musculatura del cuádriceps empuja la tibia hacia delante, una contracción de alta intensidad puede ejercer mucha presión sobre el LCA, lo que aumenta el riesgo de lesión.
La dominancia de una pierna describe al hecho observado de que las mujeres tienden a colocar más peso en una pierna que en otra.[18] Por último, según la dominancia del tronco los hombres suelen mostrar un mayor control del tronco durante la actividad física, pues muestran una mayor activación del músculo oblicuo interno.[17] En el caso de las deportistas, es más probable caigan con la parte superior del cuerpo inclinada hacia un lado y apoyando más peso en una pierna que en la otra, por lo que ejercen una mayor fuerza de rotación sobre las rodillas.[19]
Diferencias hormonales y anatómicas[editar]
Antes de la pubertad, no se han observado diferencias según el sexo en la frecuencia de desgarros del LCA. Para intentar explicar la predisposición a la rotura del LCA se ha planteado una posible relación con los cambios en los niveles de hormonas sexuales. La elevación de los estrógenos y la relaxina en mujeres durante el ciclo menstrual podrían aumentar la laxitud articular y la extensibilidad de los tejidos blandos que rodean la articulación de la rodilla.[12]
En un estudio se ha demostrado que las atletas universitarias con niveles de concentración de relaxina superiores a 6,0 pg/ml presentan un riesgo cuatro veces mayor de sufrir un desgarro del LCA que aquellas que mostraban concentraciones más bajas.[20]
Además, durante la pubertad la pelvis femenina se ensancha por el efecto de las hormonas sexuales. Este ensanchamiento de la pelvis provoca un aumento del ángulo del fémur con respecto a la rodilla, el llamado ángulo Q. El promedio para los hombres es de 14° y para las mujeres es de 17°. Se pueden tomar medidas para reducir el ángulo Q, como el uso de dispositivos ortopédicos.[21] La cadera femenina, relativamente más ancha, y el ángulo Q mayor podrían aumentar la probabilidad de desgarros del LCA en las mujeres.[22]
LCA, rigidez muscular y fuerza[editar]
Durante la pubertad, las hormonas sexuales también causan remodelación de los tejidos blandos del cuerpo. La remodelación tisular en las mujeres genera LCA más pequeños y que pueden fallar (es decir, romperse) con fuerzas de carga más bajas. Además, también provoca diferencias en la rigidez muscular y ligamentosa entre hombres y mujeres. Durante la activación muscular, las mujeres presentan menor rigidez en la articulación de la rodilla. Cuando se aplica fuerza sobre una rodilla menos rígida existe mayor probabilidad de causar desgarros del LCA.[23]
Por otra parte, el músculo cuádriceps femoral es un antagonista del LCA. Según un estudio realizado en mujeres deportistas en la Universidad de Míchigan, en el 31% de los casos, las mujeres presentaron activación del músculo cuádriceps femoral en primer lugar, en comparación con el 17% de los hombres. Debido a una intensa contracción del músculo cuádriceps femoral durante la actividad física, se ejerce una mayor tensión sobre el LCA debido a la «traslación anterior de la tibia».[24]
Fisiopatología[editar]
La articulación de la rodilla está formada por tres huesos: el fémur (hueso del muslo), la tibia (hueso de la espinilla) y la rótula. Estos huesos se mantienen unidos por los ligamentos, que son fuertes bandas de tejido que mantienen la estabilidad de la articulación al caminar, correr, saltar... En la rodilla existen dos tipos de ligamentos: los ligamentos colaterales y los ligamentos cruzados.
Los ligamentos colaterales son el ligamento colateral tibial (en la región medial de la rodilla) y el ligamento lateral externo (en la región lateral de la rodilla). La función de estos ligamentos es limitar el desplazamiento lateral de la rodilla.[6]
Los ligamentos cruzados forman una «X» dentro de la articulación de la rodilla: el ligamento cruzado anterior se extiende desde la cara frontal de la tibia hasta la parte posterior del fémur mientras que el ligamento cruzado posterior se extiende desde la parte posterior de la tibia hasta la parte frontal del fémur. El ligamento cruzado anterior evita que la tibia se deslice sobre del fémur y aporta estabilidad rotacional.[6]
También hay dos estructuras cartilaginosas en forma de «C» llamadas menisco medial y menisco lateral que se asientan sobre la tibia y que actúan como amortiguadores entre los huesos.[1]

|
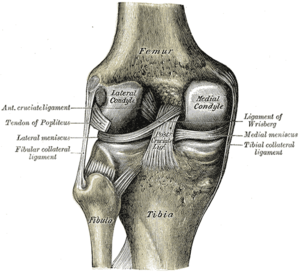
|
| Rodilla derecha, vista frontal, muestra los ligamentos interiores. | Rodilla izquierda, vista dorsal, muestra los ligamentos interiores. |
Diagnóstico[editar]
Pruebas manuales[editar]
La mayoría de las lesiones de LCA se pueden diagnosticar explorando la rodilla y comparándola con la rodilla sana. Ante la sospecha de una lesión del LCA en una persona que relata un chasquido en la rodilla, seguido de hinchazón, dolor e inestabilidad de la articulación, el médico puede practicar diferentes pruebas para evaluar el grado de lesión. Entre estas pruebas se encuentran la prueba del desplazamiento del pivote, la prueba del cajón anterior y la prueba de Lachman. Para hacer la prueba del desplazamiento del pivote hay que doblar la rodilla sosteniendo el tobillo y rotar ligeramente la tibia hacia dentro.[25] En la prueba del cajón anterior se coloca la rodilla a 90°, el examinador se sienta sobre los pies del paciente y con suavidad tracciona de la tibia hacia si.[26] La prueba de Lachman se realiza colocando una mano en el muslo del paciente y la otra en la tibia y tirando de ésta hacia delante.[27] El objetivo de estas pruebas es evaluar la integridad del LCA y su capacidad para limitar el desplazamiento anterior de la tibia. Según la mayoría de los profesionales, la prueba de Lachman se considera la más fiable y sensible de las tres.[28]
Pruebas de imagen[editar]

Aunque la exploración física llevada a cabo por un profesional experimentado puede ser diagnóstica, es habitual hacer una resonancia magnética de confirmación, que además proporciona imágenes de los tejidos blandos adyacentes, como los ligamentos o los cartílagos de la rodilla.[1] Además, permite valorar otras estructuras que pueden haber resultado dañadas, como los meniscos o los ligamentos colaterales. También se puede hacer una radiografía para evaluar si alguno de los huesos de la articulación de la rodilla se ha roto durante la lesión.[9]
Aunque la resonancia magnética es probablemente la prueba de imagen más utilizada para evaluar el estado del LCA, no siempre resulta la más fiable ya que la imagen puede estar distorsionada por el hematoma que se forma en la articulación tras la lesión.[29]
Otra manera de valorar la rodilla cuando el examen físico y la resonancia magnética no son concluyentes son las pruebas para medir la laxitud ligamentosa (artrometría y radiografías de estrés), que consisten en aplicar una fuerza a la pierna y medir el desplazamiento de la rodilla.[29]
Clasificación[editar]
La lesión de un ligamento se llama esguince. La Academia Estadounidense de Cirujanos Ortopédicos define las lesiones del LCA en función de la gravedad y las clasifica como esguinces de grado 1, 2 y 3.[1] Se considera que es un esguince de grado 1 cuando el ligamento se distiende ligeramente, pero la estabilidad de la articulación de la rodilla no se ve afectada. Se considera que es un esguince de grado 2 o desgarro parcial cuando el ligamento se distiende hasta elongarse. Por último, el esguince de grado 3 se produce cuando el ligamento se secciona por completo y la articulación de la rodilla ya no es estable. El tipo más común de lesión del LCA es el esguince de grado 3.
Aproximadamente la mitad de las lesiones del LCA ocurren junto a lesiones en otras estructuras de la rodilla, entre las que se incluyen otros ligamentos, los meniscos o los cartílagos situados en la superficie de los huesos. Un patrón específico de lesión es la llamada «Tríada de O'Donoghue» (también conocida como «tríada triste» o simplemente «la tríada») que implica lesiones en el LCA, el ligamento colateral medial y el menisco medial, y ocurre cuando se aplica una fuerza lateral a la rodilla mientras el pie está fijo en el suelo.[30]
Prevención[editar]
Se ha puesto especial esfuerzo en disminuir la incidencia de las lesiones del LCA causadas por un mecanismo diferente al impacto directo. Tras una revisión exhaustiva de las estrategias preventivas, el Comité Olímpico Internacional ha llegado a la conclusión de que los programas de prevención de lesiones tienen un efecto medible en la disminución de la incidencia de lesiones.[31] Estos programas son especialmente importantes en las deportistas, pues presentan una mayor incidencia de lesión del LCA que los deportistas varones; así como en niños y adolescentes ya que tienen un alto riesgo de volver a sufrir una rotura del LCA.[32][33]
Los investigadores han comprobado que es frecuente que las deportistas aterricen de un salto con las rodillas relativamente rectas e inclinadas hacia dentro, con la mayor parte del peso corporal en un pie y la parte superior del cuerpo inclinada hacia un lado. Estos cuatro factores ejercen una tensión excesiva en los ligamentos, lo que incrementa la probabilidad de lesión del LCA.[34][17] Se ha demostrado que el entrenamiento neuromuscular (NMT), cuyo objetivo es fortalecer los músculos isquiotibiales, mejorar el equilibrio y la estabilidad general; ayuda a reducir el riesgo de lesiones al mejorar los patrones de movimiento durante los movimientos de mayor riesgo. Dichos programas son beneficiosos para todos los deportistas, pero especialmente para las adolescentes que practican deporte.[35][19]
Tratamiento[editar]
El tratamiento de la lesión del LCA está orientado a:[36]
- Reducir los movimientos anómalos de la rodilla y mejorar su función
- Generar confianza para volver a usar la rodilla con normalidad
- Prevenir otras lesiones en la rodilla y reducir el riesgo de osteoartritis
- Mejorar la calidad de vida a largo plazo tras la lesión
No quirúrgico[editar]
El tratamiento no quirúrgico para la ruptura del LCA conlleva una rehabilitación progresiva y estructurada cuyos objetivos son recuperar la fuerza muscular, el control dinámico de la rodilla y la confianza. En algunos casos, el LCA puede curarse durante el proceso de rehabilitación sin necesidad de cirugía (las partes desgarradas se vuelven a unir y forman un ligamento funcional).[37]
La finalidad del tratamiento con ejercicios es recuperar el funcionamiento normal del sistema muscular y de equilibrio alrededor de la rodilla. Se ha demostrado que entrenando los músculos de la rodilla con ejercicios el cuerpo puede «aprender» a controlarla de nuevo y, a pesar del movimiento anómalo dentro de la articulación, la rodilla puede recuperar la sensación de estabilidad y la fuerza.
En estos casos, es necesario visitar a un fisioterapeuta o a un especialista en medicina deportiva poco después de la lesión que pueda supervisar un programa de ejercicios intensivo y estructurado. Inicialmente, se pueden usar otros tratamientos, como la terapia manual con el fin de reducir el dolor. El fisioterapeuta actuará como entrenador durante la rehabilitación al establecer objetivos para la recuperación y aportar sus impresiones sobre el progreso.
El tiempo de recuperación estimado con tratamiento conservador es tres a seis meses y depende de la gravedad de la lesión, el estado físico previo y el compromiso con la rehabilitación y los objetivos deportivos. En algunos casos, si los resultados con tratamiento conservador no son los esperados, el paciente puede ser intervenido más adelante.
Tratamiento quirúrgico[editar]
En la cirugía de reconstrucción del LCA se sustituye el ligamento desgarrado con un injerto, que es un tendón obtenido de otra parte. Los injertos se pueden obtener del tendón rotuliano, del tendón de los isquiotibiales o del tendón del cuádriceps de la persona que se somete al procedimiento («autoinjerto») o de un cadáver («aloinjerto»). El injerto funciona como una estructura sobre la cual crecerá el nuevo tejido ligamentoso.[1] A fecha de 2021, no existe suficiente evidencia científica de calidad para este procedimiento.[38]
La intervención quirúrgica se lleva a cabo con un artroscopio, una cámara de reducido tamaño que se introduce en la articulación y con pequeñas incisiones adicionales alrededor de la rodilla para meter los instrumentos quirúrgicos. Este método es menos invasivo que la intervención «abierta» (en la que se hace una incisión en la parte anterior de la rodilla y la articulación queda expuesta) y se ha comprobado que provoca menos dolor postoperatorio, menor estancia hospitalaria y tiempos de recuperación más rápidos.[1]
No existe unanimidad en cuanto al momento más adecuado para la reconstrucción quirúrgica. Diversos estudios muestran peores resultados cuando se interviene inmediatamente después de la lesión, mientras que en otros no se han observado diferencias en los resultados si se interviene inmediatamente tras la lesión o se demora la operación.[39][40] Según la Academia Estadounidense de Cirujanos Ortopédicos hay evidencia moderada que respalda la indicación de reconstruir el LCA dentro de los cinco meses posteriores a la lesión para mejorar la funcionalidad y proteger la rodilla de una lesión más grave. Sin embargo, es necesario llevar a cabo más estudios para determinar el mejor momento para intervenir, así como discernir la importancia del momento quirúrgico en los resultados.[41]
Los deportistas jóvenes que se someten a una reconstrucción quirúrgica temprana tienen más probabilidades de volver al nivel deportivo en el que se encontraban previamente, en comparación con aquellos que se sometieron a una reconstrucción tardía o a un tratamiento no quirúrgico. Además, tienen menos probabilidades de experimentar inestabilidad en la rodilla si se someten a una cirugía temprana.[42][43] En Estados Unidos se practican más de 100 000 cirugías de reconstrucción de LCA al año y más del 95 % de las reconstrucciones de LCA se realizan de forma ambulatoria. Los procedimientos más comunes realizados durante la reconstrucción del LCA son la meniscectomía parcial y la condroplastia.[44]
Rehabilitación[editar]
Los objetivos de la rehabilitación tras una lesión del LCA son recuperar la fuerza y el movimiento de la rodilla. Si una persona con una lesión del LCA se somete a una intervención quirúrgica, el proceso de rehabilitación se centrará, en primer lugar, en aumentar lentamente el rango de movimiento de la articulación y, a continuación, en fortalecer los músculos circundantes para proteger el nuevo ligamento y estabilizar la rodilla. Por último, se inicia el entrenamiento funcional específico con ejercicios adaptados según el deporte. El deportista tardará al menos seis meses en poder volver a practicar deporte tras la intervención quirúrgica, pues es imprescindible recuperar el sentido del equilibrio y el control sobre la rodilla para evitar una segunda lesión.[6]
Pronóstico[editar]
El pronóstico de la lesión del LCA es, por lo general, bueno y la mayoría recupera la función de la pierna lesionada en unos meses.[6] En el pasado, la lesión del LCA suponía, en muchos casos, el final de la carrera deportiva de un deportista de élite. Sin embargo, en la actualidad, gracias a la cirugía de reconstrucción del LCA seguida de rehabilitación física muchos deportistas vuelven a competir al nivel previo a la lesión.[45]
Entre las complicaciones a largo plazo de la lesión del LCA se encuentran la aparición temprana de artritis de la rodilla y el desgarro recurrente del ligamento. Los factores que incrementan el riesgo de artritis son: la gravedad de la lesión inicial, la lesión de otras estructuras de la rodilla y el nivel de actividad posterior al tratamiento.[9] En ocasiones, no reparar el LCA puede causar daños en el cartílago dentro de la rodilla porque con el LCA desgarrado, aumentan las probabilidades de rozamiento entre la tibia y el fémur.[1]
Por desgracia, las deportistas jóvenes corren un riesgo importante de rotura del injerto o de lesionarse el LCA de la otra rodilla tras la recuperación. Este riesgo se ha registrado en casi una de cada cuatro deportistas jóvenes.[46] Por lo tanto, es importante hacer una evaluación de estas deportistas ante la posibilidad de presentar algún déficit neuromuscular (por ejemplo, mayor debilidad en una pierna que en otra o una incorrecta caída tras el salto) antes de reiniciar la actividad deportiva.[16]
Epidemiología[editar]
En Estados Unidos se producen alrededor de 200 000 lesiones del LCA al año. La incidencia de primeras lesiones es de aproximadamente 69 por 100 000 al año, siendo en hombres de 82 por 100 000 y en mujeres de 59 por 100 000.[47] Al desglosar por edad y sexo, las mujeres entre 14 y 18 años tienen las tasas más altas de lesiones con 227,6 por 100 000; mientras que los hombres entre 19 y 24 años tienen las tasas más altas, con 241 por 100 000.
En el deporte[editar]
La tasa de segundas roturas entre los deportistas universitarios fue más alta en los jugadores de fútbol americano con 15 por 10 000, seguida de las gimnastas con 8 por 10 000 y las jugadoras de fútbol con 5,2 por 10 000.[48]
Los deportistas de secundaria tienen un riesgo mayor de sufrir desgarros del LCA en comparación con aquellos que no practican deporte. En Estados Unidos, el deporte con mayor riesgo de lesión del LCA entre las estudiantes de secundaria fue el fútbol, seguido del baloncesto y el lacrosse. Además, el baloncesto y el fútbol femeninos son los deportes que concentran la mayor cantidad de lesiones del LCA.[49] Entre los estudiantes de secundaria varones, el deporte con mayor riesgo fue el baloncesto, seguido del lacrosse y del fútbol.[50] En el baloncesto, las mujeres tienen entre cinco y ocho veces más probabilidades de sufrir un desgarro del LCA que los hombres.[49]
Referencias[editar]
- ↑ a b c d e f g h i j k l m n ñ o p q r s t u v w «Anterior Cruciate Ligament (ACL) Injuries-OrthoInfo - AAOS». orthoinfo.aaos.org. marzo de 2014. Archivado desde el original el 5 de julio de 2017. Consultado el 30 de junio de 2017.
- ↑ a b c d «ACL Injury: Does It Require Surgery?-OrthoInfo - AAOS». orthoinfo.aaos.org. septiembre de 2009. Archivado desde el original el 22 de junio de 2017. Consultado el 30 de junio de 2017.
- ↑ a b Hewett TE, Ford KR, Myer GD (marzo de 2006). «Anterior cruciate ligament injuries in female athletes: Part 2, a meta-analysis of neuromuscular interventions aimed at injury prevention». The American Journal of Sports Medicine 34 (3): 490-8. PMID 16382007. doi:10.1177/0363546505282619.
- ↑ a b Sugimoto D, Myer GD, Foss KD, Hewett TE (marzo de 2015). «Specific exercise effects of preventive neuromuscular training intervention on anterior cruciate ligament injury risk reduction in young females: meta-analysis and subgroup analysis». British Journal of Sports Medicine 49 (5): 282-9. PMID 25452612. doi:10.1136/bjsports-2014-093461.
- ↑ a b «A meta-analysis of the incidence of anterior cruciate ligament tears as a function of gender, sport, and a knee injury-reduction regimen». Arthroscopy 23 (12): 1320-25. diciembre de 2007. PMID 18063176. doi:10.1016/j.arthro.2007.07.003.
- ↑ a b c d e f «ACL Injury: Does It Require Surgery? - OrthoInfo - AAOS». Archivado desde el original el 22 de marzo de 2019. Consultado el 22 de marzo de 2018.
- ↑ Montalvo, Alicia M; Schneider, Daniel K; Yut, Laura; Webster, Kate E; Beynnon, Bruce; Kocher, Mininder S; Myer, Gregory D (agosto de 2019). «'What's my risk of sustaining an ACL injury while playing sports?' A systematic review with meta-analysis». British Journal of Sports Medicine 53 (16): 1003-1012. PMC 6561829. PMID 29514822. doi:10.1136/bjsports-2016-096274.
- ↑ Monk, A Paul; Davies, Loretta J; Hopewell, Sally; Harris, Kristina; Beard, David J; Price, Andrew J (3 de abril de 2016). «Surgical versus conservative interventions for treating anterior cruciate ligament injuries». Cochrane Database of Systematic Reviews 4: CD011166. PMC 6464826. PMID 27039329. doi:10.1002/14651858.CD011166.pub2.
- ↑ a b c «ACL injury - Symptoms and causes». Mayo Clinic (en inglés). Archivado desde el original el 23 de enero de 2018. Consultado el 22 de marzo de 2018.
- ↑ Rachel, Dedinsky; Baker, Lindsey; Imbus, Samuel; Bowman, Melissa; Murray, Leigh (2017). «Exercises That Facilitate Optimal Hamstring and Quadriceps Co-Activation to Help Decrease Acl Injury Risk in Healthy Females: A Systematic Review of the Literature». International Journal of Sports Physical Therapy 12 (1): 3-15. PMC 5294945. PMID 28217412.
- ↑ «ACL injury - Symptoms and causes». Mayo Clinic (en inglés). Archivado desde el original el 23 de enero de 2018. Consultado el 15 de noviembre de 2019.
- ↑ a b c Faryniarz, Deborah A. et al. (2006). «Quantitation of Estrogen Receptors and Relaxin Binding in Human Anterior Cruciate Ligament Fibroblasts». In Vitro Cellular & Developmental Biology – Animal 42 (7): 176-181. PMID 16948498. doi:10.1290/0512089.1.
- ↑ «Epidemiology of collegiate injuries for 15 sports: summary and recommendations for injury prevention initiatives». Journal of Athletic Training 42 (2): 311-9. April–June 2007. PMC 1941297. PMID 17710181.
- ↑ «Gender differences in muscular protection of the knee in torsion in size-matched athletes». The Journal of Bone and Joint Surgery. American Volume. 85-A (5): 782-9. mayo de 2003. PMID 12728025. doi:10.2106/00004623-200305000-00002.
- ↑ Samuelson, Kathleen; Balk, Ethan M.; Sevetson, Erika L.; Fleming, Braden C. (10 de octubre de 2017). «Limited Evidence Suggests a Protective Association Between Oral Contraceptive Pill Use and Anterior Cruciate Ligament Injuries in Females: A Systematic Review». Sports Health: A Multidisciplinary Approach 9 (6): 498-510. PMC 5665118. PMID 29016234. doi:10.1177/1941738117734164.
- ↑ a b Hewett, Timothy E.; Myer, Gregory D.; Ford, Kevin R.; Heidt, Robert S.; Colosimo, Angelo J.; McLean, Scott G.; van den Bogert, Antonie J.; Paterno, Mark V. et al. (30 de agosto de 2017). «Biomechanical Measures of Neuromuscular Control and Valgus Loading of the Knee Predict Anterior Cruciate Ligament Injury Risk in Female Athletes: A Prospective Study». The American Journal of Sports Medicine 33 (4): 492-501. PMID 15722287. doi:10.1177/0363546504269591.
- ↑ a b c d «Understanding and preventing acl injuries: current biomechanical and epidemiologic considerations - update 2010». North American Journal of Sports Physical Therapy 5 (4): 234-51. diciembre de 2010. PMC 3096145. PMID 21655382.
- ↑ «Lower extremity kinematic asymmetry in male and female athletes performing jump-landing tasks». Journal of Science and Medicine in Sport 15 (1): 87-92. enero de 2012. PMID 21925949. doi:10.1016/j.jsams.2011.07.008.
- ↑ a b Emery, Carolyn A; Roy, Thierry-Olivier; Whittaker, Jackie L; Nettel-Aguirre, Alberto; van Mechelen, Willem (17 de junio de 2015). «Neuromuscular training injury prevention strategies in youth sport: a systematic review and meta-analysis». British Journal of Sports Medicine 49 (13): 865-870. PMID 26084526. doi:10.1136/bjsports-2015-094639.
- ↑ Dragoo, Jason; Castillo, Tiffany; Braun, Hillary; Ridley, Bethany; Kennedy, Ashleigh; Golish, Raymond (7 de julio de 2011). «Prospective Correlation Between Serum Relaxin Concentration and Anterior Cruciate Ligament Tears Among Elite Collegiate Female Athletes». Journal of Sports Medicine 39 (10): 2175-80. PMID 21737831. doi:10.1177/0363546511413378.
- ↑ McLean, Scott G.; Huang, Xuemei; van den Bogert, Antonie J. (ctubre de 2005). «Association between lower extremity posture at contact and peak knee valgus moment during sidestepping: Implications for ACL injury». Clinical Biomechanics 20 (8): 863-870. PMID 16005555. doi:10.1016/j.clinbiomech.2005.05.007.
- ↑ Griffin, Letha (2008). «Risk and Gender Factors for Noncontact Anterior Cruciate Ligament Injury». The anterior cruciate ligament : reconstruction and basic science. Saunders/Elsevier. pp. 18-27. ISBN 978-1-4160-3834-4.
- ↑ «Anterior cruciate ligament biology and its relationship to injury forces». The Orthopedic Clinics of North America 37 (4): 585-91. ctubre de 2006. PMID 17141016. doi:10.1016/j.ocl.2006.09.001.
- ↑ «Anterior cruciate ligament injuries in female athletes». Connecticut Medicine 63 (11): 657-60. noviembre de 1999. PMID 10589146.
- ↑ «Pivot Shift Test - Orthopedic Examination of the Knee - PHYSICAL THERAPY WEB». PHYSICAL THERAPY WEB (en inglés estadounidense). Archivado desde el original el 22 de marzo de 2018. Consultado el 22 de marzo de 2018.
- ↑ «Anterior Drawer Test - Orthopedic Examination of the Knee - PHYSICAL THERAPY WEB». PHYSICAL THERAPY WEB (en inglés estadounidense). Archivado desde el original el 22 de marzo de 2018. Consultado el 22 de marzo de 2018.
- ↑ «Lachman Test». Physiopedia (en inglés). Archivado desde el original el 22 de marzo de 2018. Consultado el 22 de marzo de 2018.
- ↑ van Eck CF, van den Bekerom MP, Fu FH, Poolman RW, Kerkhoffs GM (agosto de 2013). «Methods to diagnose acute anterior cruciate ligament rupture: a meta-analysis of physical examinations with and without anaesthesia». Knee Surgery, Sports Traumatology, Arthroscopy 21 (8): 1895-903. PMID 23085822. doi:10.1007/s00167-012-2250-9.
- ↑ a b Rohman, Eric M.; Macalena, Jeffrey A. (16 de marzo de 2016). «Anterior cruciate ligament assessment using arthrometry and stress imaging». Current Reviews in Musculoskeletal Medicine 9 (2): 130-138. PMC 4896874. PMID 26984335. doi:10.1007/s12178-016-9331-1.
- ↑ «Surgical treatment of fresh injuries to the major ligaments of the knee». The Journal of Bone and Joint Surgery. American Volume. 32 A (4): 721-38. ctubre de 1950. PMID 14784482. doi:10.2106/00004623-195032040-00001.
- ↑ Ardern, Clare L; Ekås, Guri Ranum; Grindem, Hege; Moksnes, Håvard; Anderson, Allen F; Chotel, Franck; Cohen, Moises; Forssblad, Magnus et al. (abril de 2018). «2018 International Olympic Committee consensus statement on prevention, diagnosis and management of paediatric anterior cruciate ligament (ACL) injuries». British Journal of Sports Medicine 52 (7): 422-438. PMC 5867447. PMID 29478021. doi:10.1136/bjsports-2018-099060.
- ↑ Lang, Pamela J; Sugimoto, Dai; Micheli, Lyle J (junio de 2017). «Prevention, treatment, and rehabilitation of anterior cruciate ligament injuries in children». Open Access Journal of Sports Medicine 8: 133-141. PMC 5476725. PMID 28652828. doi:10.2147/OAJSM.S133940.
- ↑ Dekker, Travis J.; Godin, Jonathan A.; Dale, Kevin M.; Garrett, William E.; Taylor, Dean C.; Riboh, Jonathan C. (junio de 2017). «Return to Sport After Pediatric Anterior Cruciate Ligament Reconstruction and Its Effect on Subsequent Anterior Cruciate Ligament Injury». The Journal of Bone and Joint Surgery 99 (11): 897-904. PMID 28590374. doi:10.2106/JBJS.16.00758.
- ↑ Boden, Barry P.; Sheehan, Frances T.; Torg, Joseph S.; Hewett, Timothy E. (septiembre de 2010). «Noncontact Anterior Cruciate Ligament Injuries: Mechanisms and Risk Factors». Journal of the American Academy of Orthopaedic Surgeon 18 (9): 520-527. PMC 3625971. PMID 20810933. doi:10.5435/00124635-201009000-00003.
- ↑ «The influence of age on the effectiveness of neuromuscular training to reduce anterior cruciate ligament injury in female athletes: a meta-analysis». The American Journal of Sports Medicine 41 (1): 203-15. enero de 2013. PMC 4160039. PMID 23048042. doi:10.1177/0363546512460637.
- ↑ Filbay, Stephanie R.; Grindem, Hege (febrero de 2019). «Evidence-based recommendations for the management of anterior cruciate ligament (ACL) rupture». Best Practice & Research Clinical Rheumatology 33 (1): 33-47. PMC 6723618. PMID 31431274. doi:10.1016/j.berh.2019.01.018.
- ↑ Ihara, Hidetoshi; Kawano, Tsutomu (2017). «Influence of Age on Healing Capacity of Acute Tears of the Anterior Cruciate Ligament Based on Magnetic Resonance Imaging Assessment». Journal of Computer Assisted Tomography 41 (2): 206-211. PMC 5359784. PMID 28045756. doi:10.1097/RCT.0000000000000515.
- ↑ Blom, Ashley W; Donovan, Richard L; Beswick, Andrew D; Whitehouse, Michael R; Kunutsor, Setor K (7 de julio de 2021). «Common elective orthopaedic procedures and their clinical effectiveness: umbrella review of level 1 evidence». BMJ: n1511. doi:10.1136/bmj.n1511.
- ↑ Jarvela, Timo (febrero de 2008). «Double-bundle anterior cruciate ligament reconstruction using hamstring autografts and bioabsorbable interference screw fixation: prospective, randomized, clinical study with 2-year results». The American Journal of Sports Medicine 36 (2): 290-297. PMID 17940145. doi:10.1177/0363546507308360.
- ↑ Bottoni, Craig R. (abril de 2008). «Postoperative range of motion following anterior cruciate ligament reconstruction using autograft hamstrings: a prospective, randomized clinical trial of early versus delayed reconstructions». American Journal of Sports Medicine 36 (4): 656-662. PMID 18212347. doi:10.1177/0363546507312164.
- ↑ «OrthoGuidelines». Archivado desde el original el 24 de marzo de 2018. Consultado el 23 de marzo de 2018.
- ↑ «Anterior cruciate ligament tears in children and adolescents: a meta-analysis of nonoperative versus operative treatment». The American Journal of Sports Medicine 42 (11): 2769-76. noviembre de 2014. PMID 24305648. doi:10.1177/0363546513510889.
- ↑ Dunn, KL; Lam, KC; Valovich McLeod, TC (mayo de 2016). «Early Operative Versus Delayed or Nonoperative Treatment of Anterior Cruciate Ligament Injuries in Pediatric Patients.». Journal of Athletic Training 51 (5): 425-7. PMC 5013703. PMID 27244126. doi:10.4085/1062-6050.51.5.11.
- ↑ «Incidence and trends of anterior cruciate ligament reconstruction in the United States». The American Journal of Sports Medicine 42 (10): 2363-70. ctubre de 2014. PMID 25086064. doi:10.1177/0363546514542796.
- ↑ «Anterior Cruciate Ligament Injury». Archivado desde el original el 24 de marzo de 2018. Consultado el 23 de marzo de 2018.
- ↑ Paterno, MV (ctubre de 2010). «Biomechanical measures during landing and postural stability predict second anterior cruciate ligament injury after anterior cruciate ligament reconstruction and return to sport.». American Journal of Sports Medicine 38 (10): 1968-1978. PMC 4920967. PMID 20702858. doi:10.1177/0363546510376053.
- ↑ Sanders, Thomas L.; Kremers, Hilal Maradit; Bryan, Andrew J.; Larson, Dirk R.; Dahm, Diane L.; Levy, Bruce A.; Stuart, Michael J.; Krych, Aaron J. (26 de febrero de 2016). «Incidence of Anterior Cruciate Ligament Tears and Reconstruction: A 21-Year Population-Based Study». The American Journal of Sports Medicine (en inglés) 44 (6): 1502-7. PMID 26920430. doi:10.1177/0363546516629944.
- ↑ Gans, Itai; Retzky, Julia S.; Jones, Lynne C.; Tanaka, Miho J. (13 de junio de 2018). «Epidemiology of Recurrent Anterior Cruciate Ligament Injuries in National Collegiate Athletic Association Sports: The Injury Surveillance Program, 2004-2014». Orthopaedic Journal of Sports Medicine 6 (6): 232596711877782. PMC 6024527. PMID 29977938. doi:10.1177/2325967118777823.
- ↑ a b Ireland, Mary Lloyd; Gaudette, Michael; Crook, Scott (mayo de 1997). «ACL Injuries in the Female Athlete». Journal of Sport Rehabilitation 6 (2): 97-110. doi:10.1123/jsr.6.2.97.
- ↑ «Sport-Specific Yearly Risk and Incidence of Anterior Cruciate Ligament Tears in High School Athletes: A Systematic Review and Meta-analysis». The American Journal of Sports Medicine 44 (10): 2716-2723. ctubre de 2016. PMID 26657853. doi:10.1177/0363546515617742.
Enlaces externos[editar]
- Esta obra contiene una traducción derivada de «User:Mr. Ibrahem/Anterior cruciate ligament injury» de Wikipedia en inglés, concretamente de esta versión del 23 de noviembre de 2022, publicada por sus editores bajo la Licencia de documentación libre de GNU y la Licencia Creative Commons Atribución-CompartirIgual 4.0 Internacional.
