Imagen de contraste dependiente del nivel de oxígeno en la sangre
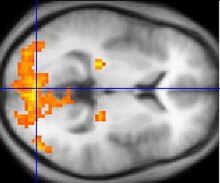
La imagen de contraste dependiente del nivel de oxígeno en la sangre (en inglés Blood-oxygen-level dependent contrast imaging o abreviado BOLD-contrast imaging), es una técnica usada en la imagen por resonancia magnética nuclear funcional (IRMf) para medir niveles locales y transitorios de oxígeno en la sangre. Estas cantidades locales de oxígeno son transportadas por la hemoglobina en función del flujo sanguíneo en los vasos cerebrales, el cual está relacionado con la actividad neuronal. Por tanto, a partir de estos niveles de oxígeno esta técnica obtiene imágenes que reflejan la activación de distintas zonas del cerebro. Esta técnica es la más utilizada para obtener imágenes por resonancia magnética funcional de forma no invasiva. [1]
Principio de funcionamiento[editar]

Las neuronas no cuentan con reservas internas de energía en forma de glucosa y oxígeno, por lo tanto cuando se activan y aumenta su actividad metabólica el organismo realiza un aumento correlativo del flujo sanguíneo local a través de la respuesta hemodinámica. Esta respuesta permite que las neuronas se abastezcan rápidamente de glucosa y oxígeno cuando lo necesitan, dándose, por tanto, un acoplamiento neurovascular. Este aumento del flujo sanguíneo cerebral causa un aumento local de la glucosa en la sangre en una cantidad similar a la requerida por las neuronas activadas. Sin embargo, el aumento transitorio de oxígeno es mucho mayor al consumido (mediante la glucólisis). Este suministro en exceso de oxígeno implica un decremento relativo de la desoxihemoglobina (hemoglobina desoxigenada) con respecto a la oxihemoglobina (hemoglobina oxigenada) en sangre. La hemoglobina desoxigenada es paramagnética (débilmente atraída por los campos magnéticos), mientras que la hemoglobina oxigenada es diamagnética (débilmente repelida por los campos magnéticos). Debido a que la hemoglobina desoxigenada es paramagnética, ésta provoca una alteración del campo magnético a su alrededor, resultando en que los protones del tejido cercano son sometidos a diferentes intensidades del campo magnético por lo que desarrollan diferentes velocidades de precesión. Esta heterogeneidad en las velocidades de precesión lleva al escáner de IRMf a medir una menor señal ponderada en T2* (y en T2) cuando la sangre no está oxigenada (y un mayor nivel de esta señal cuando la sangre altamente oxigenada, esto es, más diamagnética). [3] Estas diferencias de señal se hacen más evidentes cuanto mayor es el campo magnético generado por el escáner. Por tanto, gracias a este método es posible obtener una imagen 3D (compuesta por vóxeles), donde aproximadamente cada vóxel refleja el nivel de activación de las neuronas incluidas en el volumen de dicho vóxel. El valor que toman estos vóxeles durante y después de una corta activación neuronal sigue una respuesta la cual consta de varias fases: un breve valle inicial (que no siempre está presente), un pico (unos 5 segundos después del inicio del estímulo desencadenante de la actividad) y una sobreoscilación negativa. Si la activación neuronal se prolonga más tiempo, se observa una meseta entre el pico y la sobreoscilación negativa.
Activación neuronal detectada[editar]
Se podría pensar que el nivel de activación neuronal medido por este método de IRMf viene determinado principalmente por los potenciales de acción neuronales, ya que son procesos costosos energéticamente, y por tanto, podrían provocar un considerable aumento del flujo sanguíneo. Sin embargo, este nivel de activación neuronal medido (desencadenante del acoplamiento neurovascular) parece estar mejor representado por la activación de las sinapsis excitadoras, en concreto por la liberación del neurotransmisor glutamato. El glutamato es detectado por los astrocitos, cuyas prolongaciones contactan el músculo liso vascular, dilatando los vasos sanguíneos y aumentando el flujo sanguíneo, mediando así el acoplamiento neurovascular. [4] Este acoplamiento neurovascular (conjuntamente con otros mecanismos) regula el flujo y volumen de sangre, que junto a la cantidad de oxígeno consumida por las neuronas, determinan el nivel de desoxihemoglobina, y por tanto, la imagen obtenida por el escáner (resonador).
Historia[editar]
A principio de la década de los 80 Keith R. Thulborn y otros colegas de la Universidad de Oxford observaron que la constante de tiempo de relajación transversal espín-espín (T2) de los protones del agua en la sangre (obtenida mediante resonancia magnética nuclear (RMN)) proporciona información sobre el estado de oxigenación de la hemoglobina en la sangre. Por tanto, determinaron que la RMN permite monitorizar el oxígeno consumido por los tejidos y órganos continuamente. [5]
Al final de la misma década Seiji Ogawa, un investigador de los laboratorios Bell, estaba estudiando la posibilidad de usar la RMN para obtener imágenes de la fisiología del cerebro. En un estudio publicado en 1990 Ogawa y otros colegas utilizaron la desoxihemoglobina como un agente de contraste natural para obtener imágenes in vivo del cerebro de las ratas. [6] En este estudio demostraron que las imágenes obtenidas reflejaban el nivel de oxigenación de la sangre, obteniendo por tanto mediciones locales indicativas de la actividad neuronal. Para hacer esta demostración hicieron a una rata respirar gas compuesto de 90% O2 y 10% CO2, y observaron que la imagen obtenida era uniforme, no mostrando los vasos sanguíneos. Sin embargo, cuando la rata respiraba oxígeno puro los vasos sanguíneos aparecían representados como líneas oscuras (menores niveles de señal). Este resultado lo explicaron argumentando que cuando se incrementa la proporción de CO2 en la sangre (como hicieron en el primer caso) aumenta el flujo sanguíneo. Este incremento de flujo aumenta el suministro de oxígeno al cerebro, y en ausencia de un aumento de la tasa metabólica cerebral la sangre se encuentra más oxigenada. Esta sangre oxigenada no provoca una disminución en la señal registrada y por tanto no aparece en la imagen. En cambio cuando la rata respiraba oxígeno puro la velocidad del flujo sanguíneo era un 76% menor, explicando la disminución de la oxigenación sanguínea observada en la imagen del cerebro en el segundo caso. De esta forma demostraron que es posible obtener imágenes in vivo del cerebro las cuales codifican niveles locales de oxígeno en la sangre, los cuales pueden ser utilizados como medidas del nivel de actividad neuronal.
Referencias[editar]
- ↑ Caicedo Martínez, O. H.; Aldana Ramírez, C. A.; Hernández Suarez, C. A. (2009). «Resonancia magnética funcional: evolución y avances en clínica». Tecnura 13 (25): 88-103.
- ↑ Janz, C.; Schmitt, C.; Speck, O.; Hennig, J. (2000). «Comparison of the hemodynamic response to different visual stimuli in single‐event and block stimulation fMRI experiments». Journal of Magnetic Resonance Imaging 12 (5): 708-714.
- ↑ Costa Subias, Joaquín; Soria Jerez, Juan Alfonso (2015). Resonancia magnética dirigida a técnicos superiores en imagen para el diagnóstico. Barcelona, España: Elsevier España, S.L.U. p. 261. ISBN 9788490227459.
- ↑ Rodríguez-Rojas, R.; Machado C., Carballo M., Estévez M., Chinchilla M. (2013). Springer, ed. Cambios en el Acople Neurovascular Inducidos por el Zolpidem en el Estado Vegetativo Persistente: Estudio de RMN funcional. V Latin American Congress on Biomedical Engineering CLAIB 2011. Habana, Cuba. pp. 539-542.
- ↑ Thulborn, K. R.; Waterton, J. C.; Matthews, P. M.; Radda, G. K. (1982). «Oxygenation dependence of the transverse relaxation time of water protons in whole blood at high field». Biochimica et Biophysica Acta (BBA)-General Subjects 714 (2): 265-270.
- ↑ Ogawa, S.; Lee, T. M.; Kay, A. R.; Tank, D. W. (1990). «Brain magnetic resonance imaging with contrast dependent on blood oxygenation». Proceedings of the National Academy of Sciences 87 (24): 9868-9872.
