Diferencia entre revisiones de «Organismo genéticamente modificado»
Revertidos los cambios de 187.153.47.156 a la última edición de 187.153.47.156 usando monobook-suite |
|||
| Línea 3: | Línea 3: | ||
Comúnmente se los denomina transgénicos y son creados artificialmente en laboratorios por ingenieros genéticos. |
Comúnmente se los denomina transgénicos y son creados artificialmente en laboratorios por ingenieros genéticos. |
||
Las técnicas de [[ingeniería genética]] que se usan consisten en aislar segmentos del [[ADN]] (material genético) para introducirlos en el [[genoma]] (material hereditario) de otro, ya sea utilizando como vector otro ser vivo capaz de inocular fragmentos de ADN (''Agrobacterium tumefaciens'', virus), ya sea bombardeando las células con micropartículas recubiertas del adn que se pretenda introducir, u otros métodos fisicos como descargas eléctricas que permitan penetrar los fragmentos de ADN hasta el interior del núcleo, a través de las membranas celulares. |
|||
Al ser la manipulación en el material genético, este es hereditario, puede transferirse a la siguiente generación salvo que la modificación esterilice al organismo transgénico. |
Al ser la manipulación en el material genético, este es hereditario, puede transferirse a la siguiente generación salvo que la modificación esterilice al organismo transgénico. |
||
Revisión del 16:22 11 nov 2009
Un organismo modificado genéticamente (abreviado OMG, OGM o GMO, este último del inglés Genetically Modified Organism) es aquél cuyo material genético es manipulado en laboratorios donde ha sido diseñado o alterado deliberadamente con el fin de otorgarle alguna característica específica. Comúnmente se los denomina transgénicos y son creados artificialmente en laboratorios por ingenieros genéticos.
Las técnicas de ingeniería genética que se usan consisten en aislar segmentos del ADN (material genético) para introducirlos en el genoma (material hereditario) de otro, ya sea utilizando como vector otro ser vivo capaz de inocular fragmentos de ADN (Agrobacterium tumefaciens, virus), ya sea bombardeando las células con micropartículas recubiertas del adn que se pretenda introducir, u otros métodos fisicos como descargas eléctricas que permitan penetrar los fragmentos de ADN hasta el interior del núcleo, a través de las membranas celulares.
Al ser la manipulación en el material genético, este es hereditario, puede transferirse a la siguiente generación salvo que la modificación esterilice al organismo transgénico.
La modificación genética de organismos es objeto de una fuerte controversia:
- Por una parte, organizaciones ecologistas en todo el mundo como Greenpeace y WWF entre otras, advierten de los problemas encontrados en los OGM, que pueden descontrolarse a medida que estos organismos se expanden por acción de los vientos y las aves, contaminando cultivos naturales.
- Existe una fuerte oposición por las posibles consecuencias de la extensión de este tipo de cultivos, que ha llevado a algunos países a establecer moratorias o prohibirlos, y ha llevado en algunos casos a disturbios, como la quema de campos de OGM en algunas zonas de Europa.
- A menudo sus defensores apuntan que este tipo de tecnología puede servir para mitigar el hambre en el mundo, y para reducir la acción de una serie de enfermedades (por ejemplo, es posible preparar arroz que resulte más rico en ciertos nutrientes, previniendo la aparición de enfermedades carenciales, o vacas que den leche con vacunas o antibióticos).
- Por otra parte, las grandes multinacionales tienen una serie de patentes que pueden limitar los beneficios de esta tecnología a los intereses de sus accionistas.
- Estas tecnologías requieren una fuerte inversión, y al ser las empresas que los desarrollan las que financian la practica totalidad de los estudios realizados,[cita requerida] se crea un conflicto de intereses puede dar lugar a desconfianza sobre los estudios.
Ventajas
- Mejoras en el proceso industrial
En cuanto a las aplicaciones en agronomía y mejora vegetal en sentido amplio, poseen cuatro ventajas esenciales:
- Una gran versatilidad en la ingeniería, puesto que los genes que se incorporan al organismo huésped pueden provenir de cualquier especie, incluyendo bacterias.[1]
- Se puede introducir un solo gen en el organismo sin que esto interfiera con el resto de los genes; de este modo, es ideal para mejorar los caracteres monogénicos, es decir, codificados por un sólo gen, como algunos tipos de resistencias a herbicidas.[2]
- El proceso de modificación genética demora mucho menos que las técnicas tradicionales de mejoramiento por cruzamiento; la diferencia es de años, en frutales, a meses.
- Ventajas para los consumidores
Que fundamentalmente afectan a la calidad del producto final; es decir, a la modificación de sus características.
- Producción de nuevos alimentos
- Posibilidad de incorporar características nutricionales distintas en los alimentos
- Vacunas indiscriminadas comestibles, por ejemplo: tomates con la vacuna de la hepatitis B.[3]
- Ventajas para los agricultores
Mejoras agronómicas relativas a la metodología de producción y su rendimiento.
- Aumento de la productividad y la calidad aparente de los cultivos
- Resistencia a plagas y enfermedades conocidas; por ejemplo, por inclusión de toxinas bacterianas, como las de Bacillus thuringiensis específicas contra determinadas familias de insectos.[4]
- Tolerancia a herbicidas (como el glifosato o el glufosinato), salinidad, fitoextracción en suelos metalíferos contaminados con metales pesados,[5] sequías y temperaturas extremas.
- Rapidez. El proceso de modificación genética demora mucho menos que las técnicas tradicionales de mejora por cruzamiento, que requiere varias generaciones para eliminar otros genes que se introdujeron en el mismo cruzamiento.[cita requerida]
- Ventajas para el ambiente
- Algunos alimentos transgénicos han permitido una simplificación en el uso de productos químicos, como en el caso del maíz Bt, donde el combate de plagas ya no requiere el uso de insecticidas químicos de mayor espectro y menor biodegradabilidad.[6]
- Nuevos materiales
Además de la innovación en materia alimentaria, la ingeniería genética permite obtener cualidades novedosas fuera de este ámbito; por ejemplo, por producción de plásticos biodegradables y biocombustibles.[7]

Inconvenientes
- Resistencia a los antibióticos
Para localizar las células en que se ha incorporado y activado el gen introducido, un método común es la introducción de genes que determinan cierta resistencia a unos antibióticos, de modo que al añadir el antibiótico sobreviven solo las células resistentes, con el gen de resistencia incorporado y activo, y probablemente también con el gen que se desea introducir. Dicho método se utiliza con el fin de verificar que el gen de interés haya sido efectivamente incorporado en el genoma del organismo huésped. Estos genes acompañantes son denominados marcadores, y no son necesarios para el resultado final, solo simplifican el proceso para lograrlo. Existen otros marcadores que no tienen relación con la resistencia a quimioterápicos, como los de auxotrofía. Se teme que la inclusión de estos elementos en los alimentos transgénicos podría originar la transmisión de la resistencia a antibioticos las bacterias de la microbiota intestinal, [8] y de estas a organismos patogenos.No obstante, por orden de la FAO los alimentos transgénicos comercializados deberian carecer de los mencionados genes de resistencia;[9]
- Mayor nivel de residuos tóxicos en los alimentos
- Es un problema colateral al empleo de transgénicos. Algunos autores[cita requerida] suponen que en las especies resistentes a herbicidas los agricultores los emplean en cantidades mayores a las que se podía usar anteriormente.
- La posibilidad de usar intensivamente insecticidas a los que son resistentes los transgénicos hace que se vean afectadas y dañadas las especies colindantes (no resistentes). No obstante, existen evidencias científicas de que los cultivos de transgénicos resistentes a insecticidas permiten un menor uso de éstos en los campos, lo que redunda en un menor impacto en el ecosistema que alberga al cultivo.[10]
- Posibilidad de generación de nuevas alergias
- Un estudio científico de de 1999 mostró la posibilidad de que los alimentos transgénicos produjeran algún tipo de daño. En él se indicaba que el intestino de ratas alimentadas con patatas genéticamente modificadas (expresando una aglutinina de Galanthus nivalis, que es una lectina) resultaba dañado severamente.[11] No obstante, este estudio fue criticado debido a la existencia de errores en el diseño experimental y en el manejo de los datos. Por ejemplo, se incluyeron pocos animales en cada grupo experimental (lo que da lugar a una gran incertidumbre estadística), ni se analizó la composición química con precisión de las distintas variedades de patata empleadas, ni se incluyeron controles en los experimentos y finalmente, el análisis estadístico de los resultados era incorrecto.[12]
- Dependencia de la técnica empleada
- La precisión en la obtención de recombinantes, por ejemplo en su localización genómica, es muy dependiente de la técnica empleada: vectores, biobalística, etc.
- Contaminación de variedades tradicionales
- El polen de las especies transgéncias puede fecundar a cultivos convencionales, obteniéndose híbridos y transformando a estos cultivos en transgénicos. Este fenómeno ya ocurre con las variedades no transgénicas hoy en día. Además, la transferencia horizontal a bacterias de la rizosfera es posible[cita requerida].
- Muerte de insectos no objeto
- Aunque el empleo de recombinantes para toxinas de Bacillus thuringiensis es, por definición, un método específico, a diferencia de los plaguicidas convencionales, existe una demanda comercial que provoca el desarrollo de cepas que actúan conjuntamente contra lepidópteros, coleópteros y dípteros. Este hecho podría afectar a la fauna accesoria del cultivo. [cita requerida]
- Impacto ecológico de los cultivos
El posible riesgo sanitario ha sido desmentido para algunos GMOs, como el maíz resistente a glifosato.[13]
- Obligatoriedad del consumo
- La decisión de introducir alimentos transgénicos en la industria alimentaria ha sido totalmente contraria a todo proceso democrático, ocultando incluso la composición de los alimentos. La industria de los OMG sigue estando consciente de que no cuenta con el apoyo de la población de ningún país del mundo, y ello se demuestra con el hecho de que no se revela la información en el envasado de alimentos transgénicos.
- Monopolización del mercado, control del agricultor
- El hecho de que la misma empresa de OMG provee al agricultor de la planta y de insecticidas/herbicidas ha hecho que las plantas estén adaptadas a dichos productos químicos y viceversa, por lo que el agricultor pasa a depender en exclusiva de una sola empresa proveedora. El monopolio en el suministro conlleva a la imposición de precios y a condiciones de explotación.
Política y legislación
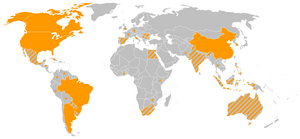
Los cinco países que producen más del 95% de GMO
 :Otros países con GMOs comercializados Puntos naranja: sólo cultivos experimentales.
:Otros países con GMOs comercializados Puntos naranja: sólo cultivos experimentales.La Organización Mundial de la Salud dice al respecto:
Los diferentes organismos OGM incluyen genes diferentes insertados en formas diferentes. Esto significa que cada alimento GM y su inocuidad deben ser evaluados individualmente, y que no es posible hacer afirmaciones generales sobre la inocuidad de todos los alimentos GM. Los alimentos GM actualmente disponibles en el mercado internacional han pasado las evaluaciones de riesgo y no es probable que presenten riesgos para la salud humana. Además, no se han demostrado efectos sobre la salud humana como resultado del consumo de dichos alimentos por la población general en los países donde fueron aprobados. El uso continuo de evaluaciones de riesgo en base a los principios del Codex y, donde corresponda, incluyendo el monitoreo post comercialización, debe formar la base para evaluar la inocuidad de los alimentos GM.[14]
La Administración de Fármacos y Alimentos estadounidense (FDA) aprobó en febrero de 2009 por primera vez el uso clínico de un primer medicamento obtenido usando animales genéticamente modificados. Se trata de ATryn, una forma recombinante de la hormona humana antitrombina, que se obtiene de la leche de cabras (Capra aegagrus hircus) modificadas genéticamente.[15][16] La droga, que previene la formación de coágulos sanguíneos en personas víctimas de deficiencia congénita de la hormona, ya había sido aprobada por la Unión Europea en 2006.[17]
Etiquetado de alimentos transgénicos
Debido a la sensibilización del público en este campo y para honrar el derecho que tenemos los consumidores a saber lo que consumimos, las legislaciones de muchos países empiezan a tener en cuenta este tema, obligando, por ejemplo, a rotular explícitamente los alimentos en cuya composición se incluyen los transgénicos. En Estados Unidos y Canadá no es necesario este etiquetado,[18] pero sí en la Unión Europea, Japón, Malasia y Australia.[19][20] Este etiquetado requiere la separación de los componentes transgénicos y no transgénicos durante su producción pero también durante el procesado subsiguiente, lo que exige un cuidadoso seguimiento de su trazabilidad.[19][20]
Véase también
Referencias
- ↑ Griffiths, J .F. A. et al. (2002). Genética. McGraw-Hill Interamericana. ISBN 84-486-0368-0.
- ↑ Agrios, G.N. (2005). Plant Pathology (5ta. ed. edición). Elsevier Academic Press. ISBN 0-12-044564-6.
- ↑ Xiao-Ming Lou (Abril 2007). «Expression of the human hepatitis B virus large surface antigen gene in transgenic tomato plants» (pdf). Clinical and Vaccine Immunology. 14 (4): 464-469. 1556-6811. Consultado el 11-08-2007.
- ↑ E. Schnepfm et al. (1998). «Bacillus thuringiensis and its pesticidal crystal proteins». Microbiology and Molecular Biology Reviews. 32 (3). ISSN 1098-5557.
- ↑ Mitch M. Lasat (1998). «Phytoextraction of toxic metals». Journal of Environmental Quality. 31. ISSN 1537-2537.
- ↑ E. Schnepfm et al. (1998). «Bacillus thuringiensis and its pesticidal crystal proteins». Microbiology and Molecular Biology Reviews. 32 (3). ISSN 1098-5557.
- ↑ E. S. Lipinsky (1978). «Fuels from biomass: Integration with food and materials systems». Science. 199 (4329). ISSN 0036-8075.
- ↑ Eede, G.; Aarts, H.; Buhk, H.J.; Corthier, G.; Flint, H.J.; Hammes, W.; Jacobsen, B.; Midtvedt, T.; Vossen, J.; Wright, A.; Others (2004), «The relevance of gene transfer to the safety of food and feed derived from genetically modified (GM)», Food and Chemical Toxicology 42 (7): 1127-1156, consultado el 6 de mayo de 2009.
- ↑ FDA, Estados Unidos (1998), Guidance for industry: use of antibiotic resistance marker genes in transgenic plants. 1-26.
- ↑ Morse, S.; Bennett, R.; Ismael, Y. (2004), «Why Bt cotton pays for small-scale producers in South Africa», Nature Biotechnology 22 (4): 379-380, consultado el 6 de mayo de 2009.
- ↑ Ewen, S.W.B.; Pusztai, A. (1999), «Effect of diets containing genetically modified potatoes expressing Galanthus nivalis lectin on rat», Lancet 354 (9187): 1353-1354.
- ↑ Kuiper, H.A.; Noteborn, H.; Peijnenburg, A. (1999), «Adequacy of methods for testing the safety of genetically modified foods», Lancet-London-: 1315-1315.
- ↑ Antonio L. Cerdeiraa et Stephen O. Dukeb (2006). «The current status and environmental impacts of glyphosate-resistant crops». J Environ Qual. 35 (1633-1658). ISSN 1537-2537.
- ↑ «20 preguntas sobre los alimentos genéticamente modificados». Consultado el 11-08-2007. Parámetro desconocido
|último=ignorado (se sugiere|apellido=) (ayuda) - ↑ Environmental Assessment for tbe Bc6 rDNA Construct in GTC 155-92 Goats Expressing Recombinant Human Antitbrombin III (rbAT or ATRYN). Presentado por ante el Centro de Medicina veterinaria de FDA. 29 de enero de 2009. Revisado el 11 de febrero de 2009.
- ↑ FDA Approves Orphan Drug ATryn to Treat Rare Clotting Disorder. FDA News. U.S. Food and Drug Administration. Revisado el 6 de febrero de 2009.
- ↑ Informe público europeo de evaluación (EPAR): ATRYN. Resumen para el público general European Medicines Agency. EMEA/H/C/587.
- ↑ Trade barriers seen in EU label for bio-engineered ingredients. (Regulatory and Policy Trends). Business and the Environment 13.11 (Nov 2002): p14(1).
- ↑ a b northwestern.edu Northwestern Journal of Technology and Intellectual Property Paper on: "Consumer Protection" Consumer Strategies and the European Market in Genetically Modified Foods Quote: The recent Trans Atlantic Consumer Dialogue (TACD) Statement on the WTO decision makes this clear: "clearly consumers' preference for non-GM food is the true engine of the market collapse for American crops." and For instance, Evenson notes that the politicization of GMOs is not merely a question of labeling as information, but unlabeled GM products as catalysts in the "globalization backlash."
- ↑ a b CBC Identifying genetically modified products. Quote: Yet as seen in this report from CBC's Marketplace, no such labeling law exists in Canada despite numerous surveys indicating up to 90 per cent of Canadians want mandatory labeling of GM food. Canada's leading national consumer group does not support mandatory labeling. It appeared to reverse its stance on December 3, 2003: http://www.consumer.ca/1626
Bibliografía
- Pratley, J. et at. 1996. Glyphosate resistance in annual ryegrass. Proc. Eleventh Ann. Conf. Grassld. Soc, NSW.
- Bergel, Salvador. 2001. "El principio precautorio y la transgénesis de las variedades vegetales" en: Bergel, Salvador, Alberto Díaz (org.). Biotecnología y Sociedad. Buenos Aires. Ciudad Argentina.
- Smith, J., Seeds of deception: exposing industry and government lies about the safety of the genetically engineered foods you're eating. 2nd. ed., Fairfield, Yes! Books, 2003. 290p.
Enlaces externos
- Glosario de biotecnología para la agricultura y la alimentación de la FAO
- FAO-BiotechNews-Esp — Boletín de noticias de biotecnología de la FAO
- La Biotecnología Agrícola - informe de la FAO (2004).
- Cultivos Modificados Genéticamente - resumen realizado por GreenFacts del informe de la FAO.
- Polinización cruzada entre cultivos GM y cultivos tradicionales
- Agroinformación de Cádiz
- Organizaciones por la biodiversidad en América Latina
- Los transgénicos son insostenibles
- ¿Si como tomates transgénicos me saldrán escamas? Los Transgénicos en el Museo Virtual Leyendo el Libro de la Vida
