Dispositivo intrauterino de cobre
| Dispositivo Intrauterino de Cobre | ||
|---|---|---|
 Foto de un modelo común
de DIU con cobre (Paragard T 380A) | ||
| Antecedentes | ||
| Tipo de anticonceptivo | Control de natalidad reversible de larga duración | |
| Primer uso | Década de 1970 | |
| Tasa de embarazo (primer año) | ||
| Uso perfecto | 0.6 | |
| Uso típico | 0.8 | |
| Uso | ||
| Reversibilidad | Rápida | |
| Recordatorios al usuario | Notar expulsión si hay dolor | |
| Revisión clínica | No requiere seguimiento | |
| Ventajas y desventajas | ||
| Protección contra ETS | No | |
| Períodos |
Puede ocasionar períodos abundantes o dolorosos | |
| Beneficios |
| |
| Riesgos |
| |
Un dispositivo intrauterino (DIU) con cobre, también conocido como bobina intrauterina o T de Cobre, es un tipo de dispositivo intrauterino que contiene cobre.[1] Se utiliza para el control de la natalidad y como contraceptivo de emergencia dentro de los cinco días posteriores a una relación sexual sin protección.[1] Es una de las formas más eficaces de control de la natalidad con una tasa de fracaso dentro del año de colocación de alrededor del 0,7 %.[2] El dispositivo se coloca en el útero y puede utilizarse hasta hasta doce años seguidos.[1][3][4] Puede ser utilizado por mujeres de todas las edades independientemente de si han tenido hijos o no.[5] Después de su remoción, la fertilidad regresa rápidamente.[3]
Entre los efectos secundarios, pueden presentarse períodos menstruales abundantes, dolorosos o que el dispositivo se salga.[1] Es menos recomendable en personas con alto riesgo de infecciones de transmisión sexual, ya que puede aumentar el riesgo de enfermedad pélvica inflamatoria en las primeras tres semanas después de la inserción.[5] Si una mujer queda embarazada con un DIU colocado, se recomienda retirarlo.[5] En raras ocasiones, puede ocurrir una perforación de la pared uterina durante la inserción.[3] El DIU de cobre es un tipo de método anticonceptivo reversible de acción prolongada.[2] Su principal mecanismo de acción es la liberación de iones cobre que resultan tóxicos para el esperma.[3]
El DIU de cobre entró en uso médico en la década de 1970.[3] Se encuentra en la Lista de Medicamentos Esenciales de la Organización Mundial de la Salud.[6] El costo mayorista en el mundo en desarrollo es de aproximadamente US$0,40 a US$3,00 por DIU.[7] En el Reino Unido le cuestan al NHS unas 10 libras esterlinas.[5] En Canadá costaban alrededor de 80 CAD en el año 2021.[8] En Estados Unidos cada DIU con cobre cuesta alrededor de $750.[9] Son utilizados por más de 170 millones de mujeres en todo el mundo.[10][11]
Usos médicos
[editar]Los DIU de cobre son una forma de anticoncepción reversible de acción prolongada y uno de los métodos anticonceptivos más eficaces.[12] El tipo de armazón y la cantidad de cobre pueden afectar a la eficacia de los distintos modelos de DIU de cobre.[13] Las tasas de fracaso de los distintos modelos varían entre el 0,1 y el 2,2% tras 1 año de uso. Los modelos en forma de T con una superficie de 380 mm² de cobre presentan los índices de fallo más bajos. El TCu 380A (ParaGard) tiene una tasa de fallos de un año del 0,8% y una tasa de fallos acumulada de 12 años del 2,2%.[13] Durante 12 años de uso, los modelos con menos superficie de cobre tienen tasas de fallos más elevadas. El TCu 220A tiene una tasa de fallos de 12 años del 5,8%. El GyneFix sin marco tiene una tasa de fallo inferior al 1% anual.[14] En todo el mundo se han dejado de fabricar modelos de DIU antiguos con tasas de eficacia más bajas.[15] A diferencia de otras formas de anticoncepción reversible, la tasa de fallo de uso típico y la tasa de fallo de uso perfecto para los DIU de cobre son las mismas porque el DIU no depende de la acción del usuario.[12] Una revisión de 2008 de los DIU de cobre en forma de T disponibles recomendó que el TCu 380A y el TCu 280S se utilizaran como primera opción para los DIU de cobre porque esos dos modelos tienen las tasas de fallo más bajas y las vidas útiles más largas.[13] La eficacia del DIU de cobre (tasa de fallo del 0,8%) es comparable a la esterilización tubárica (tasa de fallo del 0,5%) durante el primer año.[16][17][18]
Anticoncepción de emergencia
[editar]En 1976 se descubrió por primera vez que el DIU de cobre podía utilizarse como método anticonceptivo de emergencia (AE).[19] Es más eficaz que las píldoras anticonceptivas hormonales disponibles en la actualidad.[20] La tasa de embarazo entre las mujeres que utilizan el DIU de cobre como método anticonceptivo de urgencia es del 0,09%. Puede utilizarse como AE hasta cinco días después de haber mantenido relaciones sexuales sin protección y su eficacia no disminuye durante esos cinco días.[21] Otra ventaja de utilizar el DIU de cobre como anticonceptivo de emergencia es que puede utilizarse como método anticonceptivo durante 10-12 años después de su inserción.[21]
Extracción y vuelta a la fertilidad
[editar]La extracción del DIU de cobre también debe realizarla un médico cualificado. Se ha demostrado que la fertilidad vuelve a los niveles anteriores rápidamente tras la extracción del dispositivo.[22] Un estudio reveló que la mediana de tiempo transcurrido desde la extracción hasta el embarazo planificado fue de tres meses para las mujeres que utilizaban el TCu 380Ag.[23]
Efectos secundarios
[editar]Expulsión: A veces, el DIU de cobre puede expulsarse espontáneamente del útero.[22] Las tasas de expulsión pueden oscilar entre el 2,2% y el 11,4% de las usuarias entre el primer y el décimo año. El TCu380A puede tener menores tasas de expulsión que otros modelos.[24] Un flujo vaginal inusual, calambres o dolor, manchado entre periodos, manchado postcoital (después del sexo), dispareunia, o la ausencia o alargamiento de los hilos pueden ser signos de una posible expulsión.[22] Si se produce la expulsión, la mujer no está protegida contra el embarazo. Si se inserta un DIU con cobre después de que se haya producido una expulsión, el riesgo de reexpulsión se ha estimado en un estudio en aproximadamente un tercio de los casos al cabo de un año.[25] La resonancia magnética (RM) puede provocar la dislocación de un DIU con cobre, por lo que se recomienda comprobar la ubicación del DIU tanto antes como después de la RM.[26]

Perforación: En muy raras ocasiones, el DIU puede atravesar la pared del útero.[22] El riesgo de perforación viene determinado principalmente por la habilidad del profesional que realiza la inserción. Para los médicos experimentados, el riesgo de perforación es de 1 por 1.000 inserciones o menos.[27]
Infección: La inserción de un DIU de cobre plantea un riesgo transitorio de enfermedad inflamatoria pélvica (EIP) en los primeros 21 días tras la inserción. Sin embargo, se trata de un riesgo pequeño y es atribuible a una infección preexistente por gonorrea o clamidia en el momento de la inserción, y no al DIU en sí.[28][29] Los procedimientos adecuados de prevención de infecciones tienen poco o ningún efecto sobre el curso de las infecciones por gonorrea o clamidia, pero son importantes para ayudar a proteger tanto a las usuarias como a los proveedores de las infecciones en general.[29] Estas prácticas de prevención de infecciones incluyen lavarse las manos y luego ponerse guantes, limpiar el cuello uterino y la vagina, tener un contacto mínimo con superficies no estériles (utilizando una técnica de inserción sin contacto) y, después del procedimiento, lavarse las manos de nuevo y luego procesar los instrumentos.[15] El dispositivo en sí no conlleva un mayor riesgo de EPI más allá del momento de la inserción.[22]
Calambres: Algunas mujeres pueden sentir calambres durante el proceso de inserción del DIU e inmediatamente después como resultado de la dilatación del cuello uterino durante la inserción.[15] Tomar AINE antes del procedimiento suele reducir las molestias,[30] al igual que el uso de anestesia local. El misoprostol 6 a 12 horas antes de la inserción puede ayudar con la dilatación cervical.[30] Algunas mujeres pueden tener calambres durante 1 a 2 semanas después de la inserción.
Menstruaciones más abundantes: El DIU de cobre puede aumentar la cantidad de flujo sanguíneo durante los periodos menstruales de la mujer.[15] Por término medio, la pérdida de sangre menstrual puede aumentar entre un 20 y un 50% tras la inserción de un DIU T de cobre; este síntoma puede desaparecer en algunas mujeres después de 3 a 6 meses.[31]
Sangrado irregular y manchado: En algunas mujeres, el DIU de cobre puede provocar manchados entre las menstruaciones durante los primeros 3 a 6 meses tras la inserción.[22]
Embarazo: Aunque es poco frecuente, si se produce un embarazo con el DIU de cobre colocado puede haber efectos secundarios. El riesgo de embarazo ectópico para una mujer que utiliza un DIU es menor que el riesgo de embarazo ectópico para una mujer que no utiliza ningún método anticonceptivo. Sin embargo, de los embarazos que se producen durante el uso del DIU, un porcentaje mayor de lo esperado (3-4%) son ectópicos.[15] Si se produce un embarazo con el DIU colocado, existe un mayor riesgo de aborto espontáneo o parto prematuro. Si esto ocurre y los hilos del DIU son visibles, éste debe ser extraído inmediatamente por un médico.[22] Aunque el DIU Dalkon Shield se asoció a abortos sépticos (infecciones asociadas a abortos espontáneos), otras marcas de DIU no lo están. Los DIU tampoco se asocian a defectos de nacimiento.[15]
Algunos anticonceptivos de barrera protegen contra las ITS. Los anticonceptivos hormonales reducen el riesgo de desarrollar enfermedad inflamatoria pélvica (EIP), una complicación grave de ciertas ITS. En cambio, los DIU no protegen contra las ITS ni la EPI.[32][22]
Toxicidad por cobre: Existen pruebas anecdóticas que relacionan los DIU de cobre con casos de toxicidad por cobre.[33]
Contraindicaciones
[editar]Una afección de categoría 3 indica condiciones en las que los riesgos teóricos o probados suelen superar las ventajas de insertar un DIU de cobre. Una condición de categoría 4 indica condiciones que representan un riesgo inaceptable para la salud si se inserta un DIU de cobre.
Las mujeres no deben utilizar un DIU de cobre si:
(Categoría 4)
- Están embarazadas o creen que pueden estarlo
- Padecen ciertas anomalías uterinas
- Padecen una enfermedad trofoblástica gestacional maligna
- Tiene o puede tener una ITS
- Ha tenido o puede haber tenido una infección pélvica en los últimos tres meses
- Tiene tuberculosis pélvica
- Tiene hemorragias vaginales anormales inexplicables
- Tener cáncer de cuello uterino no tratado
- Tiene cáncer de útero
- Haber tenido un embarazo séptico o un aborto
(Categoría 3)
- Son puérperas entre 48 horas y 4 semanas (mayor tasa de expulsión del DIU con inserción posparto retrasada). Los criterios de los CDC y la OMS difieren en su recomendación para las mujeres que han dado a luz entre 48 horas y 4 semanas. Los CDC no lo consideran una contraindicación.
- Tienen SIDA (a menos que estén clínicamente bien con terapia antirretroviral)
- Tienen una enfermedad trofoblástica gestacional benigna
- Tiene cáncer de ovario
- Tienen una probabilidad individual muy alta de exposición a gonorrea o ITS por clamidia
Se puede encontrar una lista completa de contraindicaciones en los Criterios médicos de elegibilidad para el uso de anticonceptivos de la Organización Mundial de la Salud (OMS)[31] y en los Criterios médicos de elegibilidad para el uso de anticonceptivos de los Centros para el Control y la Prevención de Enfermedades (CDC) de Estados Unidos.[34]
Ser nulípara (mujer que nunca ha dado a luz) no es una contraindicación para el uso del DIU. Los DIU son seguros y aceptables incluso en mujeres nulíparas jóvenes.[35][36]
Descripción del dispositivo
[editar]Hay varios modelos de DIU de cobre disponibles en todo el mundo. La mayoría de los dispositivos de cobre consisten en un núcleo de plástico envuelto en un alambre de cobre.[13] Muchos de los dispositivos tienen forma de T, similar al DIU hormonal. Sin embargo, también existen DIU de cobre "sin marco". ParaGard es el único modelo disponible actualmente en Estados Unidos. En Canadá existen al menos tres modelos de DIU de cobre, dos de los cuales son versiones en forma de T más finas que se utilizan en mujeres que no han tenido hijos. Los primeros DIU de cobre sólo tenían cobre alrededor del vástago vertical, pero los modelos más recientes también tienen manguitos de cobre alrededor de los brazos horizontales, lo que aumenta su eficacia.[37]
Algunos modelos más nuevos también contienen un núcleo de plata en lugar de un núcleo de plástico para retrasar la fragmentación del cobre y aumentar la vida útil del dispositivo. La vida útil de los dispositivos oscila entre 3 y 10 años; sin embargo, algunos estudios han demostrado que el TCu 380A puede ser eficaz hasta los 12 años.[27]
Su código Sistema de Clasificación Anatómica Terapéutica Química (ATC) es G02BA (OMS).
Inserción
[editar]Un DIU de cobre puede insertarse en cualquier fase del ciclo menstrual, pero el momento óptimo es justo después del periodo menstrual, cuando el cuello uterino está más blando y la mujer tiene menos probabilidades de quedarse embarazada.[38] El proceso de inserción suele durar cinco minutos o menos. El procedimiento puede provocar calambres o ser doloroso para algunas mujeres. Antes de la colocación de un DIU, es útil que un profesional médico realice una historia clínica y un examen físico para comprobar si existe alguna contraindicación o preocupación.[38] Algunos médicos también recomiendan que las pacientes se sometan a pruebas de gonorrea y clamidia, ya que estas dos infecciones aumentan el riesgo de contraer enfermedad inflamatoria pélvica poco después de la inserción.[28]
Inmediatamente antes de la inserción, el clínico realizará un examen pélvico para determinar la posición del útero.[22] Tras el examen pélvico, se mantiene abierta la vagina con un espéculo.[38] Se utiliza un tenáculo para estabilizar el cuello uterino y el útero.[38] Se puede utilizar un sonda uterina para medir la longitud y la dirección del canal cervical y el útero con el fin de disminuir el riesgo de perforación uterina. El DIU se coloca utilizando un tubo estrecho, que se introduce a través del cuello uterino hasta el útero. Unos hilos cortos de monofilamento de plástico/nylon cuelgan del útero hacia la vagina. El clínico recortará los hilos para que sólo sobresalgan 3 o 4 cm del cuello uterino y permanezcan en la parte superior de la vagina. Los hilos permiten a la paciente o al clínico comprobar periódicamente que el DIU sigue en su sitio y facilitan la extracción del dispositivo.[22]
El DIU de cobre puede insertarse en cualquier momento del ciclo menstrual, siempre que la mujer no esté embarazada.[27] El DIU también puede insertarse inmediatamente después del parto y después de un aborto, siempre que no se haya producido una infección.[34] La lactancia no es una contraindicación para el uso del DIU de cobre. El DIU puede insertarse en mujeres con VIH o SIDA, ya que no aumenta el riesgo de transmisión.[31] Aunque anteriormente no se recomendaba para mujeres nulíparas (mujeres que no han tenido hijos), el DIU se recomienda ahora para la mayoría de las mujeres que ya han pasado la menarquia (su primer periodo), incluidas las adolescentes.[39]
Tipos
[editar]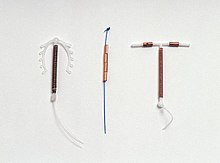
Actualmente se fabrican muchos tipos diferentes de DIU de cobre en todo el mundo, pero la disponibilidad varía según el país. En Estados Unidos, sólo está aprobado el uso de un tipo de DIU de cobre, mientras que en el Reino Unido existen más de diez variedades.[40] Una empresa, Mona Lisa N.V., ofrece versiones genéricas de muchos de los DIU existentes.[41]
| DIU | Tipo | Ancho (mm) | Largo (mm) | Cobre (mm2) | Vida útil (años) | Fabricante | Características distintivas |
|---|---|---|---|---|---|---|---|
| Gyneplus Cu 380 | Forma de T | 380 | 5 | Dispo.Cont. | |||
| Multiload Cu375 | Forma de U | 20.5[42] | 35 | 375 | 5 | Multilan | |
| Multiload Cu375 | Forma de U | 250 | 3 | Multilan | |||
| Multi-Safe 375 | Forma de U | 19.5[43] | 32.5 | 375 | 5 | Williams Medical Supplies | |
| Multi-Safe 375 bucle corto | Forma de U | 375 | 5 | Williams Medical Supplies | |||
| Load 375 | Forma de U | 19.5[43] | 32.5 | 375 | 5 | 7-MED Industrie | |
| Nova-T 380 | Forma de T (lisa) | 32[44] | 32 | 380 | 5 | Bayer | |
| Neo-Safe T 380 | Forma de T (lisa) | 32[43] | 32 | 380 | 5 | Durbin | |
| Neo-Safe T 380 Mini | Forma de T (lisa) | 24[45] | 30 | 380 | 5 | Durbin | |
| UT 380 | Forma de T (lisa) | 32[43] | 32 | 380 | 5 | Laboratoire CCD | |
| UT 380 corto | Forma de T (lisa) | 32[43] | 28.4 | 380 | 5 | Laboratoire CCD | |
| Flexi-T 300 | Forma de T (lisa) | 23[46] | 29 | 300 | 5 | Prosan | |
| Flexi-T + 300 | Forma de T (lisa) | 28[46] | 32 | 300 | 5 | Prosan | Brazos más anchos que Flexi-T 300 |
| T-safe CU 380A | En forma de T (en banda) | 31.8[43] | 35.8 | 380 | 8 | Durbin | |
| Flexi-T + 380 | En forma de T (en banda) | 28[46] | 32 | 380 | 5 | Prosan | |
| TT 380 Slimline | En forma de T (en banda) | 31.8[43] | 35.8 | 380 | 10 | 7-MED Industrie | |
| TT 380 Mini | En forma de T (en banda) | 23.2[46] | 29.5 | 380 | 5 | 7-MED Industrie | |
| Paragard | En forma de T (en banda) | 32[47] | 36 | 380 | 10 | Duramed | Único DIU de cobre aprobado por la FDA |
| Gynefix 330 (estándar) | Sin marco | 2.2[43] | 30 | 330 | 5 o 10 | Contrel | Única marca de DIU sin marco disponible |
| Gynefix 200 (mini) | Sin marco | 200 | 5 | Contrel | Única marca de DIU sin marco disponible | ||
| IUB SCu300A/B | Esférico (3D) | 300 | 5 | OCON | Montura con núcleo de aleación de nitinol. La marca es Ballerine | ||
| SMB TCu 380A | En forma de T (en banda) | 32[48] | 36 | 380 | 10 | SMB corp | OMS UNFPA Fabricante de DIU precalificado |
| Protect TCu 380A | En forma de T (en banda) | 380 | 12 | SMB corp | OMS UNFPA Fabricante de DIU precalificado | ||
| Protect Multibrazo Cu 375 estándar | Forma de U | 375 | 5 | SMB corp | OMS UNFPA Fabricante de DIU precalificado | ||
| Protección Multibrazo Cu 375 corto | Forma de U | 375 | 5 | SMB corp | OMS UNFPA Fabricante de DIU precalificado |
DIU sin marco
[editar]El DIU sin marco elimina el uso del marco que da a los DIU convencionales su característica forma de T. Este cambio en el diseño se hizo para reducir las molestias y la expulsión asociadas a los DIU anteriores; sin un marco sólido, el DIU sin marco debería amoldarse a la forma del útero. Puede reducir las tasas de expulsión e interrupción en comparación con los DIU de cobre con marco.[49]
Gynefix es la única marca de DIU sin marco disponible actualmente. Consta de tubos huecos de cobre sobre un hilo de polipropileno. Se introduce a través del cuello uterino con un aplicador especial que ancla el dispositvo al fondo (parte superior) del útero; a continuación, el hilo se corta con una cola que cuelga fuera del cuello uterino, de forma similar a los DIU con marco. Cuando se tira de esta cola, el nudo es liberado del fondo y puede extraerse el dispositivo. Esto puede requerir más fuerza que la extracción de un DIU en forma de T y puede provocar molestias comparables durante la extracción.[50]
Mecanismo de acción
[editar]El principal mecanismo de acción del DIU de cobre es impedir la fecundación.[22][51][52][53] El cobre actúa como espermicida dentro del útero. La presencia de cobre aumenta los niveles de iones de cobre, prostaglandinas y glóbulos blancos dentro de los fluidos uterinos y tubáricos.[22][51]
Aunque no se trata de un mecanismo de acción primario, algunos expertos en reproducción humana creen que hay pruebas suficientes para sugerir que los DIU con cobre pueden interrumpir la implantación,[54] especialmente cuando se utilizan como anticonceptivos de emergencia.[55][56] A pesar de ello, no ha habido pruebas definitivas de que las usuarias de DIU tengan mayores tasas de pérdida embrionaria que las mujeres que no utilizan anticonceptivos.[51] Por lo tanto, se considera que el DIU de cobre es un verdadero anticonceptivo y no un abortivo.[22]
Uso
[editar]A nivel mundial, el DIU es el método anticonceptivo reversible más utilizado.[57] Los datos más recientes indican que hay 169 millones de usuarias de DIU en todo el mundo. Esto incluye tanto los DIU no hormonales como los hormonales. Los DIU son más populares en Asia, donde la prevalencia es de casi el 30%. En África y Europa, la prevalencia se sitúa en torno al 20%.[57] En 2009, se estimaba que el uso del DIU en Estados Unidos era del 5,5%.[16] Los datos de Estados Unidos no distinguen entre DIU hormonal y no hormonal. En Europa, la prevalencia del DIU de cobre oscila entre menos del 5% en el Reino Unido y más del 10% en Dinamarca en 2006.[58]
Historia
[editar]Según la leyenda popular, los comerciantes árabes introducían pequeñas piedras en el útero de sus camellas para evitar embarazos durante las largas travesías por el desierto. La historia fue originalmente un cuento chino para entretener a los delegados de una conferencia científica sobre planificación familiar; aunque posteriormente se repitió como verdad, no tiene base histórica conocida.[59]
Los precursores de los DIU se comercializaron por primera vez en 1902. Desarrollados a partir de los pesarios con vástago (en los que el vástago mantenía el pesario en su sitio sobre el cuello uterino), el "vástago" de estos dispositivos se extendía en realidad hasta el propio útero. Como ocupaban tanto la vagina como el útero, este tipo de pesario de tallo también se conocía como dispositivo intrauterino. El uso de dispositivos intrauterinos se asoció a altas tasas de infección; por este motivo, fueron condenados por la comunidad médica.[60]
El primer dispositivo intrauterino (contenido íntegramente en el útero) se describió en una publicación alemana en 1909, aunque parece que el autor nunca comercializó su producto.[61]
En 1929, el alemán Ernst Gräfenberg publicó un informe sobre un DIU fabricado con suturas de seda. Había encontrado una tasa de embarazo del 3% entre 1.100 mujeres que utilizaban su anillo. En 1930, Gräfenberg comunicó una tasa de embarazo inferior, del 1,6%, entre 600 mujeres que utilizaban un anillo mejorado envuelto en alambre de plata. Gräfenberg desconocía que el alambre de plata estaba contaminado con un 26% de cobre. El papel del cobre en el aumento de la eficacia del DIU no se reconocería hasta casi 40 años después.
En 1934, el médico japonés Tenrei Ota desarrolló una variación del anillo de Gräfenberg que contenía una estructura de soporte en el centro. La adición de este disco central redujo la tasa de expulsión del DIU. Estos dispositivos seguían presentando altas tasas de infección, y su uso y desarrollo se vieron aún más obstaculizados por la política de la Segunda Guerra Mundial: la anticoncepción estaba prohibida tanto en la Alemania nazi como en el Japón aliado del Eje. Los Aliados no conocieron los trabajos de Gräfenberg y Ota hasta mucho después de que acabara la guerra.[61]
El primer DIU de plástico, la espiral de Margulies, se introdujo en 1958. Este dispositivo era algo grande, lo que causaba molestias a gran parte de las mujeres usuarias, y tenía una cola de plástico duro, lo que causaba molestias a sus parejas masculinas. El coloquialismo moderno "espiral" se basa en el diseño en forma de espiral de los primeros DIU.
El Lippes loop, un dispositivo ligeramente más pequeño con una cola de monofilamento, se introdujo en 1962 y ganó popularidad frente al dispositivo de Margulies.[60]
El DIU de anillo único de acero inoxidable se desarrolló en la década de 1970[62] y se utilizó ampliamente en China debido a los bajos costes de fabricación. El gobierno chino prohibió la producción de DIU de acero en 1993 debido a las elevadas tasas de fracaso (hasta un 10% al año).[15][63]
Howard Tatum, en EE. UU., concibió el DIU de plástico en forma de T en 1968. Poco después, Jaime Zipper, en Chile, introdujo la idea de añadir cobre a los dispositivos para mejorar su eficacia anticonceptiva.[60][64] Se descubrió que los dispositivos que contenían cobre podían fabricarse en tamaños más pequeños sin comprometer su eficacia, lo que se traducía en menos efectos secundarios como dolor y hemorragias.[15] Los dispositivos en forma de T presentaban menores tasas de expulsión debido a su mayor similitud con la forma del útero.[61]
El DIU de plástico Dalkon Shield (que tenía una cola multifilamento), mal diseñado, fue fabricado por A. H. Robins Company y vendido por Robins en los Estados Unidos durante tres años y medio, desde enero de 1971 hasta junio de 1974, antes de que Robins suspendiera las ventas el 28 de junio de 1974, a petición de la FDA debido a problemas de seguridad tras los informes de 110 abortos espontáneos sépticos en mujeres con el Dalkon Shield colocado, siete de las cuales habían muerto.[65][66] Robins interrumpió las ventas internacionales del Dalkon Shield en abril de 1975.[67]
Tatum desarrolló muchos modelos diferentes del DIU de cobre. Creó el TCu220 C, que tenía collares de cobre en lugar de un filamento de cobre, lo que evitaba la pérdida de metal y aumentaba la vida útil del dispositivo. En los años setenta también se introdujo la segunda generación de DIU T de cobre. Estos dispositivos tenían una mayor superficie de cobre y, por primera vez, alcanzaron tasas de eficacia superiores al 99%.[15] El último modelo desarrollado por Tatum fue el TCu380A, el más recomendado en la actualidad.[13]
Véase también
[editar]Referencias
[editar]- ↑ a b c d WHO Model Formulary 2008. World Health Organization. 2009. pp. 370-2. ISBN 9789241547659.
- ↑ a b Wipf, Joyce (2015). Women's Health, An Issue of Medical Clinics of North America (en inglés). Elsevier Health Sciences. p. 507. ISBN 978-0-323-37608-2.
- ↑ a b c d e Goodwin, T. Murphy; Montoro, Martin N.; Muderspach, Laila; Paulson, Richard; Roy, Subir (2010). Management of Common Problems in Obstetrics and Gynecology (en inglés) (5 edición). John Wiley & Sons. pp. 494-496. ISBN 978-1-4443-9034-6.
- ↑ «IUD Birth Control Info About Mirena & ParaGard IUDs». www.plannedparenthood.org (en inglés). Archivado desde el original el 4 de enero de 2021. Consultado el 22 de marzo de 2018.
- ↑ a b c d British national formulary : BNF 69 (69 edición). British Medical Association. 2015. pp. 557-559. ISBN 978-0-85711-156-2.
- ↑ World Health Organization model list of essential medicines: 21st list 2019. Geneva: World Health Organization. 2019. WHO/MVP/EMP/IAU/2019.06. License: CC BY-NC-SA 3.0 IGO.
- ↑ «Iud (Copper)». International Drug Price Indicator Guide. Archivado desde el original el 12 de julio de 2020. Consultado el 8 de diciembre de 2016.
- ↑ Ton, Joey (6 de febrero de 2022). «#308 Can It Stay or Must It Go? Extended Use of Intrauterine Devices». CFPCLearn. Archivado desde el original el 28 de marzo de 2023. Consultado el 14 de junio de 2023.
- ↑ Zieman, Mimi (2012). Managing Contraception 2012–2014 (en inglés). Managing Contraception. p. Chapter 27. ISBN 978-1-4675-3640-0.
- ↑ Speroff, Leon; Darney, Philip D. (2011). A Clinical Guide for Contraception (en inglés). Lippincott Williams & Wilkins. p. 243. ISBN 978-1-60831-610-6.
- ↑ Schäfer-Korting, Monika (2010). Drug Delivery (en inglés). Springer Science & Business Media. p. 290. ISBN 978-3-642-00477-3.
- ↑ a b Winner, Brooke; Peipert, Jeffrey; Zhao, Quihong; Buckel, Christina; Madden, Tessa; Allsworth, Jenifer; Secura, Gina (1 de enero de 2012). «Effectiveness of long-acting reversible contraception». The New England Journal of Medicine 366 (21). doi:10.1056/NEJMoa1110855. Consultado el 26 de agosto de 2023.
- ↑ a b c d e Kulier R, O'Brien P, Helmerhorst FM, Usher-Patel M, d'Arcangues C (2008). «Copper containing, framed intra-uterine devices for contraception (Review)». Cochrane Database of Systematic Reviews. PMID 17943851. doi:10.1002/14651858.CD005347.PUB3.
- ↑ O'Brien, P. A.; Marfleet, C. (2005). «Frameless versus classical intrauterine device for contraception». The Cochrane Database of Systematic Reviews. ISSN 1469-493X. PMID 15674904. doi:10.1002/14651858.CD003282.
- ↑ a b c d e f g h i Treiman, Katherine; Liskin, Laurie; Kols, Adrienne; Rinehart, Ward (1995). «IUDs—an update. Population Reports. Series B, Intrauterine Devices.». Johns Hopkins School of Public Health, Population Information Program: 1-35. PMID 8724322. Archivado desde el original el 29 de octubre de 2013. Consultado el 30 de agosto de 2023.
- ↑ a b «Contraceptive Use in the United States». The Guttmacher Institute. 2012.
- ↑ Bartz, Deborah; Greenberg, James A (2008). «Sterilization in the United States». Reviews in Obstetrics and Gynecology 1 (1): 23-32. ISSN 1941-2797. PMC 2492586. PMID 18701927. Consultado el 26 de agosto de 2023.
- ↑ Committee On Practice Bulletins-Gynecology, Long-Acting Reversible Contraception Work Group (2017). «Practice Bulletin No. 186». Obstetrics & Gynecology: e251-e269. PMID 29064972. doi:10.1097/AOG.0000000000002400.
- ↑ Lippes, J; Malik, T; Tatum, HJ (1976). «The postcoital copper-T». Adv Plan Parent: 24-9. PMID 976578.
- ↑ Cheng, L; Gulmezoglu, AM; Piaggio, G; Ezcurra, E; Van Look, PF (2008). «Interventions for emergency contraception». Cochrane Database of Systematic Reviews. PMID 18425871. doi:10.1002/14651858.cd001324.pub3.
- ↑ a b Cleland, Kelly; Zhu, Haoping; Goldstuck, Norman; Cheng, Linan; Trussell, James (2012-7). «The efficacy of intrauterine devices for emergency contraception: a systematic review of 35 years of experience». Human Reproduction (Oxford, England) 27 (7): 1994-2000. ISSN 0268-1161. PMC 3619968. PMID 22570193. doi:10.1093/humrep/des140. Consultado el 26 de agosto de 2023.
- ↑ a b c d e f g h i j k l m Dean, Gillian; Schwarz, Eleanor Bimla (2011). «Intrauterine contraceptives (IUCs)». Contraceptive technology, New York: Ardent Media: 147-191. ISBN 978-1-59708-004-0. ISSN 0091-9721. «Mecanismo de acción Aunque se desconoce el mecanismo de acción exacto, los dispositivos intrauterinos actualmente disponibles actúan principalmente impidiendo que los espermatozoides fecunden los óvulos.26 Los dispositivos intrauterinos no son abortivos: no interrumpen un embarazo implantado.27 El embarazo se impide por una combinación del "efecto de cuerpo extraño" del armazón de plástico o metal y la acción específica de la medicación (cobre o levonorgestrel) que se libera. La exposición a un cuerpo extraño provoca una reacción inflamatoria estéril en el entorno intrauterino que es tóxica para los espermatozoides y los óvulos y dificulta la implantación.28,29 La producción de péptidos citotóxicos y la activación de enzimas provocan la inhibición de la motilidad espermática, la reducción de la capacitación y la supervivencia de los espermatozoides y el aumento de la fagocitosis de los espermatozoides.30,31 El TCu380A provoca un aumento de los iones de cobre, las enzimas, las prostaglandinas y los glóbulos blancos (macrófagos) en los fluidos uterinos y tubáricos, lo que perjudica la función espermática e impide la fecundación. p. 162: Tabla 7-1. Mitos y conceptos erróneos sobre las AIU Mito: Las AIU son abortivas. Realidad: Las AIU impiden la fecundación y son verdaderos anticonceptivos.»
- ↑ Belhadj, H; et al. (1986). «Recovery of fertility after use of the Levonorgestrel 20 mcg/d or copper T 380 Ag intrauterine device». Contraception: 261-267. PMID 3098498. doi:10.1016/0010-7824(86)90007-7.
- ↑ Kaneshiro, Bliss; Aeby, Tod (9 de agosto de 2010). «Long-term safety, efficacy, and patient acceptability of the intrauterine Copper T-380A contraceptive device». International Journal of Women's Health 2: 211-220. ISSN 1179-1411. PMC 2971735. PMID 21072313. Consultado el 28 de agosto de 2023.
- ↑ Bahamondes L, Díaz J, Marchi NM, Petta CA, Cristofoletti ML, Gomez G (1995). «Performance of copper intrauterine devices when inserted after an expulsion». Hum. Reprod.: 2917-8. PMID 8747044. doi:10.1093/oxfordjournals.humrep.a135819.
- ↑ Berger-Kulemann, Vanessa; Einspieler, Henrik; Hachemian, Nilouparak; Prayer, Daniela; Trattnig, Siegfried; Weber, Michael; Ba-Ssalamah, Ahmed (2013). «Magnetic Field Interactions of Copper-Containing Intrauterine Devices in 3.0-Tesla Magnetic Resonance Imaging: In Vivo Study». Korean Journal of Radiology: 416-22. ISSN 1229-6929. PMC 3655294. PMID 23690707. doi:10.3348/kjr.2013.14.3.416.
- ↑ a b c «WHO Scientific Group on the Mechanism of Action Safety and Efficacy of Intrauterine Devices, World Health Organization». Mechanism of action, safety and efficacy of intrauterine devices. 1987. ISBN 9241207531.
- ↑ a b Mohllajee, Anshu P.; Curtis, Kathryn M.; Peterson, Herbert B. (1 de febrero de 2006). Does insertion and use of an intrauterine device increase the risk of pelvic inflammatory disease among women with sexually transmitted infection? A systematic review. doi:10.1016/j.contraception.2005.08.007. Consultado el 28 de agosto de 2023.
- ↑ a b «Infection Prevention Practices for IUD Insertion and Removal». web.archive.org. 1 de enero de 2010. Archivado desde el original el 1 de enero de 2010. Consultado el 28 de agosto de 2023.
- ↑ a b Hutten-Czapski P, Goertzen J (2008). «The occasional intrauterine contraceptive device insertion». web.archive.org. Can J Rural Med. pp. 31-5. Archivado desde el original el 14 de agosto de 2016. Consultado el 28 de agosto de 2023.
- ↑ a b c World Health Organization (2015). «Medical eligibility criteria for contraceptive use (5th ed.)». Geneva: World Health Organization. ISBN 9789241549158.
- ↑ Farley TM, Rosenberg MJ, Rowe PJ, Chen JH, Meirik O (1992). «Intrauterine devices and pelvic inflammatory disease: an international perspective». Lancet: 785-8. PMID 1347812. doi:10.1016/0140-6736(92)91904-M.
- ↑ «The hidden danger of the copper IUD». swlondoner.shorthandstories.com (en inglés). Consultado el 28 de agosto de 2023.
- ↑ a b Curtis KM, Tepper NK, Jatlaoui TC, et al. (2016). «U.S. Medical Eligibility Criteria for Contraceptive Use, 2016». MWR Recomm Rep.: 1-103. PMID 27467196. doi:10.15585/mmwr.rr6503a1.
- ↑ Forthofer KV (2009). «Una revisión clínica del dispositivo intrauterino como método anticonceptivo eficaz». J Obstet Gynecol Neonatal Nurs: 693-8. PMID 19930283. doi:10.1111/j.1552-6909.2009.01067.x.
- ↑ Lohr, Patricia A.; Lyus, Richard; Prager, Sarah (2017). «Uso de dispositivos intrauterinos en mujeres nulíparas». Contraception: 529-537. ISSN 0010-7824. PMID 27591814. doi:10.1016/j.contraception.2016.08.011.
- ↑ Sivin I, Stern J (1979). «DIU de cobre T de acción prolongada y mayor eficacia: resumen de la experiencia en EE.UU., 1970-1975». Studies in Family Planning: 263-281. PMID 516121. doi:10.2307/1965507.
- ↑ a b c d «Birth Control Intrauterine Devices (IUDs)». web.archive.org. 10 de agosto de 2010. Archivado desde el original el 10 de agosto de 2010. Consultado el 28 de agosto de 2023.
- ↑ «ACOG - Increasing Use of Contraceptive Implants and Intrauterine Devices To Reduce Unintended Pregnancy». web.archive.org. 2 de mayo de 2012. Archivado desde el original el 2 de mayo de 2012. Consultado el 28 de agosto de 2023.
- ↑ Ghelani, Rita (11 de abril de 2019). «Is the IUD the right contraceptive method for you?». Netdoctor (en inglés británico). Consultado el 28 de agosto de 2023.
- ↑ Mona Lisa N.V.. 2011. Archivado desde el original el 14 de julio de 2011. Consultado el 30 de agosto de 2023.
- ↑ «Data». www.broadwaymed.co.nz. 2020. Archivado desde el original el 17 de enero de 2020. Consultado el 30 de agosto de 2023.
- ↑ a b c d e f g h «Guidance». www.nhstaysideadtc.scot.nhs.uk. 2021.
- ↑ «Nova-T 380 IUD (Intrauterine Device)». www.mistrymedical.com. 2020. Archivado desde el original el 30 de marzo de 2020. Consultado el 30 de agosto de 2023.
- ↑ «Neo-Safe T CU 380 Mini IUD». MidMeds Ltd (en inglés). Consultado el 29 de agosto de 2023.
- ↑ a b c d «Product information». Prosan (en nl-NL). Consultado el 29 de agosto de 2023.
- ↑ «How big is the Paragard IUD?». Paragard® IUD (en inglés estadounidense). Consultado el 29 de agosto de 2023.
- ↑ «Leading Medical Contraceptive Devices and IUD Manufacturer». www.smbcorpn.com. Consultado el 29 de agosto de 2023.
- ↑ Wu S, Hu J, Wildemeersch D (2000). «Performance of the frameless GyneFix and the TCu380A IUDs in a 3-year multicenter, randomized, comparative trial in parous women». Contraception: 91-8. PMID 10802273. doi:10.1016/s0010-7824(00)00087-1.
- ↑ D'Souza, Rachel E.; Bounds, Walli; Guillebaud, John (1 de abril de 2003). «Comparative trial of the force required for, and pain of, removing GyneFix® versus Gyne-T380S® following randomised insertion». BMJ Sexual & Reproductive Health (en inglés) 29 (2): 29-31. ISSN 2515-1991. PMID 12681034. doi:10.1783/147118903101197494. Consultado el 29 de agosto de 2023.
- ↑ a b c Ortiz, María Elena; Croxatto, Horacio B. (2007). «Dispositivo intrauterino de cobre-T y sistema intrauterino de levonorgestrel: bases biológicas de su mecanismo de acción». Contraception: S16‒S30. PMID 17531610. doi:10.1016/j.contraception.2007.01.020. «Conclusiones Las sustancias activas liberadas por el DIU o el SIU, junto con los productos derivados de la reacción inflamatoria presentes en los fluidos luminales del tracto genital, son tóxicas para los espermatozoides y los ovocitos, impidiendo el encuentro de gametos sanos y la formación de embriones viables. Los datos actuales no indican que se formen embriones en las usuarias de DIU a un ritmo comparable al de las no usuarias. La creencia común de que el mecanismo de acción habitual de los DIU en las mujeres es la destrucción de embriones en el útero no está respaldada por pruebas empíricas. La mayor parte de los datos indican que la interferencia con el proceso reproductivo después de que se haya producido la fecundación es excepcional en presencia de un DIU T-Cu o LNG y que el mecanismo habitual por el que evitan el embarazo en las mujeres es impidiendo la fecundación.»
- ↑ Speroff, Leon; Darney, Philip D. (2011). «Intrauterine contraception. A clinical guide for contraception». Philadelphia: Lippincott Williams & Wilkins: 239-280. ISBN 978-1-60831-610-6. «Mecanismo de acción La acción anticonceptiva de todos los DIU se produce principalmente en la cavidad intrauterina. La ovulación no se ve afectada y el DIU no es abortivo.58-60 Actualmente se cree que el mecanismo de acción de los DIU es la producción de un ambiente intrauterino espermicida. Los DIU no medicados dependen para su anticoncepción de la reacción general del útero ante un cuerpo extraño. Se cree que esta reacción, una respuesta inflamatoria estéril, produce una lesión tisular de grado menor pero suficiente para ser espermicida. Muy pocos espermatozoides, si es que alguno, alcanzan el óvulo en la trompa de Falopio... En las mujeres que utilizan DIU de cobre, los ensayos sensibles de gonadotropina coriónica humana no encuentran pruebas de fecundación.62,63 Esto concuerda con el hecho de que el DIU de cobre protege contra los embarazos intrauterinos y ectópicos. El DIU de cobre libera cobre libre y sales de cobre que tienen un impacto tanto bioquímico como morfológico en el endometrio y también producen alteraciones en el moco cervical y en las secreciones endometriales.... Es probable que se produzca un efecto espermicida adicional en el moco cervical.»
- ↑ Jensen, Jeffrey T.; Mishell, Daniel R. Jr. (2012). «Family planning: contraception, sterilization, and pregnancy termination». Comprehensive gynecology. Philadelphia: Mosby Elsevier: 215-272. ISBN 978-0-323-06986-1. «Dispositivos intrauterinos Mecanismos de acción La creencia común de que el mecanismo de acción habitual de los DIU en las mujeres es la destrucción de embriones en el útero no está respaldada por pruebas empíricas... Debido a que la preocupación sobre el mecanismo de acción representa una barrera para la aceptación de este importante y altamente efectivo método para algunas mujeres y algunos clínicos, es importante señalar que no hay evidencia que sugiera que el mecanismo de acción de los DIU sea abortivo... el principal mecanismo de acción del DIU de cobre T 380A es interferir con la acción de los espermatozoides, impidiendo la fecundación del óvulo.»
- ↑ ESHRE Capri Workshop Group (2008). «Intrauterine devices and intrauterine systems». Human Reproduction Update: 197‒208. PMID 18400840. doi:10.1093/humupd/dmn003. «Mecanismos de acción Así pues, tanto las pruebas clínicas como las experimentales sugieren que los DIU pueden impedir e interrumpir la implantación. Sin embargo, es poco probable que éste sea el principal modo de acción de los DIU, ... Las mejores pruebas indican que en las usuarias de DIU es inusual que los embriones lleguen al útero. En conclusión, los DIU pueden ejercer su acción anticonceptiva a diferentes niveles. Potencialmente, interfieren en la función y el transporte de los espermatozoides dentro del útero y las trompas. Es difícil determinar si la fecundación del ovocito se ve alterada por estos espermatozoides comprometidos. Existen pruebas suficientes que sugieren que los DIU pueden impedir e interrumpir la implantación. Se desconoce en qué medida esta interferencia contribuye a su acción anticonceptiva. Los datos son escasos y las consecuencias políticas de resolver esta cuestión interfieren en una investigación exhaustiva. p. 205: Resumen Los DIU que liberan cobre o levonorgestrel son anticonceptivos extremadamente eficaces... Tanto los DIU de cobre como los que liberan levonorgestrel pueden interferir en la implantación, aunque puede que éste no sea el principal mecanismo de acción. Los dispositivos también crean barreras para el transporte de espermatozoides y la fertilización, y ensayos sensibles detectan hCG en menos del 1% de los ciclos, lo que indica que la prevención significativa debe ocurrir antes de la etapa de implantación.»
- ↑ Speroff, Leon; Darney, Philip D. (2011). «Special uses of oral contraception: emergency contraception, the progestin-only minipill". A clinical guide for contraception». A clinical guide for contraception (5th ed.). Philadelphia: Lippincott Williams & Wilkins.: 153-166. ISBN 978-1-60831-610-6. «Anticoncepción postcoital de emergencia Otros métodos Otro método de anticoncepción de emergencia es la inserción de un DIU de cobre, en cualquier momento durante la fase preovulatoria del ciclo menstrual y hasta 5 días después de la ovulación. La tasa de fracaso (en un pequeño número de estudios) es muy baja, 0,1%.34,35 Este método impide definitivamente la implantación, pero no es adecuado para mujeres que no son candidatas a la anticoncepción intrauterina, por ejemplo, múltiples parejas sexuales o una víctima de violación. El uso de un DIU de cobre para la anticoncepción de emergencia es caro, pero no si se mantiene como método anticonceptivo continuado.»
- ↑ Trussell, James; Schwarz, Eleanor Bimla (2011). «Emergency contraception». Contraceptive technology (20th revised ed.). New York: Ardent Media: 113-145. ISBN 978-1-59708-004-0. ISSN 0091-9721. «Mecanismo de acción SIU liberadoras de cobre Cuando se utilizan como método anticonceptivo regular o de emergencia, los dispositivos intrauterinos liberadores de cobre actúan principalmente impidiendo la fecundación. La inserción de emergencia de una AIU de cobre es significativamente más eficaz que el uso de PAE, reduciendo el riesgo de embarazo tras una relación sexual sin protección en más de un 99%.2,3 Este alto nivel de eficacia implica que la inserción de emergencia de una AIU de cobre debe prevenir algunos embarazos tras la fecundación. El embarazo comienza con la implantación, según autoridades médicas como la FDA estadounidense, los Institutos Nacionales de Salud y el Colegio Americano de Obstetras y Ginecólogos (ACOG).»
- ↑ a b «Data Highlights - 26: Growth in World Contraceptive Use Stalling; 215 Million Women’s Needs Still Unmet | EPI». www.earth-policy.org. Consultado el 29 de agosto de 2023.
- ↑ Sonfield, Adam (2012). «"Popularity Disparity: Attitudes About the IUD in Europe and the United States». The Guttmacher Institute.
- ↑ «A History of Birth Control Methods». Planned Parenthood. 2002. Archivado desde el original el 17 de mayo de 2008. Consultado el 30 de agosto de 2023. «que cita:
- Thomas, Patricia (1988-03-14). "Contraceptives". Medical World News. 29 (5): 48.
- Bullough, Vern L.; Bullough, Bonnie (1990). Contraception: A Guide to Birth Control Methods. Buffalo, NY: Prometheus Books.»
- ↑ a b c Lynch, Catherine M. «La historia del DIU». Contraception Online. Baylor College of Medicine. Archivado desde el original el 27 de enero de 2006. Consultado el 30 de agosto de 2023.
- ↑ a b c «Evolution and Revolution: The Past, Present, and Future of Contraception». Contraception Online (Baylor College of Medicine). 2000. Archivado desde el original el 26 de septiembre de 2006. Consultado el 30 de agosto de 2023.
- ↑ «OBGYN.net - OBGYN.net - Ultrasound Section: 'Chinese Ring'». web.archive.org. 17 de enero de 2006. Archivado desde el original el 17 de enero de 2006. Consultado el 29 de agosto de 2023.
- ↑ Kaufman, J. (1993). «The cost of IUD failure in China». Studies in Family Planning.: 194-6. PMID 8351700. doi:10.2307/2939234.
- ↑ Van Kets, H.E. (1997). C. Coll Capdevila; L. Iglesias Cortit; G. Creatsas (eds.). (1997). «Importance of intrauterine contraception». Contraception Today, Proceedings of the 4th Congress of the European Society of Contraception. The Parthenon Publishing Group: 112-116. Archivado desde el original el 10 de agosto de 2006. Consultado el 30 de agosto de 2023.
- ↑ Sivin I (1993). «Another look at the Dalkon Shield: meta-analysis underscores its problems». Contraception. PMID 8403900. doi:10.1016/0010-7824(93)90060-K.
- ↑ «A Crime Against Women». multinationalmonitor.org. Consultado el 29 de agosto de 2023.
- ↑ «6 Commonly Used Scuba Delving Myths | Info For Health & Garcinia Cambogia» (en inglés estadounidense). Consultado el 29 de agosto de 2023.
