Fosfaalquino
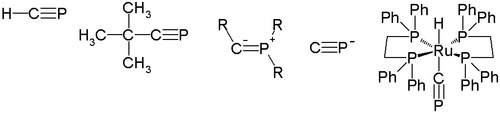
En química, un fosfaalquino s una molécula que tiene el grupo funcional enlace triple fósforo-carbono.[1] Este tipo de compuesto es ampliamente estudiado en química orgánica, pero no existe fuera del laboratorio.
Hay dos tipos de fosfaalquinos. Un tipo de fosfaalquino es un análogo pesado de los nitrilos (R-C≡N). Otro tipo de fosfaalquino tiene un átomo de fósforo pentavalente tricoordinado. Esta molécula también puede ser descrita como un iluro o un fosfinocarbeno. El análogo de fósforo de los isonitrilos, R-P+≡C-, denominado isofosfaalquino jamás ha sido observado.
En 1950, H. Albers reportó la primera evidencia de la existencia del compuesto padre de los fosfaalquinos (tipo A), H-C≡P. Este compuesto fue identificado por espectroscopia infrarroja y su síntesis fue mejorada por Manfred Regitz en 1987. La síntesis del primer fosfaalquino cinéticamente estable, que tenía un grupo tert-butilo como sustituyente R, fue reportada en 1981. Estos fosfaalquinos exhiben reacciones de adición 1,2 y cicloadiciones en su reactividad.
En el 2000, Guy Bertrand reportó la primera estructura de fosfaalquino del tipo B. Su ángulo de enlace P-C-R es de 152,6°, así que este tipo de fosfaalquino puede ser descrito mejor por una estructura de iluro de fósforo vinilo (B2).
El ion ciafuro P≡C− como análogo de fósforo del anión cianuro no es conocido como una sal, y sólo ha sido observado en la fase gaseosa. Las mediciones in silico revelan que la carga negativa en este ion reside principalmente en el carbono (0,65). Por otra parte, la molécula existe como un ligando terminal en cierto complejo de metal de transición de rutenio, el trans-[(dppe)2Ru-(H)(C≡P)], estabilizado por dppe.[2]
Referencias
[editar]- ↑ Cyaphide (C≡P-): The Phosphorus Analogue of Cyanide (C≡N-)Robert J. Angelici Angew. Chem. Int. Ed. 2007, 46, 330 – 332 doi 10.1002/anie.200603724
- ↑ Making the True "CP" Ligand. Cordaro et al. Angew. Chem. Int. Ed. 2006, 45, 6159 - 6162 doi 10.1002/anie.200602499
