Coenzima Q
Historia
La coenzima Q fue descubierta por el profesor Fred L. Crane y colegas del Instituto Enzimático de la Universidad de Wisconsin-Madison. Su estructura química fue dilucidada en 1958 por el Dr. D. E. Wolf y un grupo de investigación de los Laboratorios Merck conducido por el Dr. Karl Folkers.
Propiedades químicas
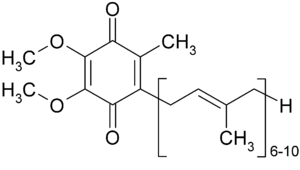
Los diversos tipos de coenzimas Q pueden diferenciarse por el número de isoprenos que posee su cadena lateral. En la naturaleza se encuentran organismos con 6 unidades de isopreno (Saccharomyces cerevisiae), 8 (Escherichia coli) o 9 (Caenorhabditis elegans), o una combinación de 9 y 10 (Mus musculus). La forma de CoQ más común en humanos es la CoQ10, aunque también se pueden encontrar pequeñas trazas de Q9. Esta molécula se denomina también ubiquinona ya que es producida por prácticamente todos los organismos con metabolismo respiratorio. En las células, al ser un lípido, se encuentra distribuido en todas las membranas celulares llevando a cabo diversas funciones relacionadas con su capacidad redox, es decir, la capacidad de alternar una forma oxidada (quinona) con una forma reducida (quinol).
Entre sus funciones podemos destacar un papel como transportador de electrones de la cadena de transporte electrónico ya que transporta en la membrana interna mitocondrial electrones desde el complejo I (NADH-reductasa) o el complejo II (succinato deshidrogenasa) hasta el complejo III (coenzima Q - citocromo c reductasa). Además también participa como aceptor de electrones de la acetil-coenzima A deshidrogenasa implicada en la (beta-oxidación de ácidos grasos) y de la dihidro-orotato deshidrogenasa, enzima implicada en la (síntesis de nucleótidos). También se ha demostrado su implicación en la actividad de enzimas desacoplantes y en la apertura del poro mitocondrial y, por tanto, la regulación de la apoptosis. En otras membranas muestra una función antioxidante, ya sea de forma directa contra la formación de lipoperóxidos o de forma indirecta a través del reciclado de otros antioxidantes lipídicos como la vitamina E, o hidrosolubles como la vitamina C o ácido ascórbico.
Inhibición por estatinas y beta bloqueantes
La inhibición de la CoQ10 por las estatinas y beta bloqueantes comparte un camino biosintético con el colesterol. La síntesis de un precursor intermediario de CoQ10, el mevalonato, es inhibido por algunos beta bloqueantes [1], medicación hipotensora, y estatinas [2], medicación reductora del colesterol. Las estatinas pueden reducir los niveles séricos de CoQ10 hasta en un 40%.
Véase también
Referencias
[1] Kishi, T; Watanabe, T; Folkers, K (1977). "Bioenergetics in clinical medicine XV. Inhibition of coenzyme Q10-enzymes by clinically used adrenergic blockers of beta-receptors". Research communications in chemical pathology and pharmacology 17 (1): 157–64. PMID 17892.
[2] Ghirlanda, G; Oradei, A; Manto, A; Lippa, S; Uccioli, L; Caputo, S; Greco, AV; Littarru, GP (1993). "Evidence of plasma CoQ10-lowering effect by HMG-CoA reductase inhibitors: a double-blind, placebo-controlled study". Journal of Clinical Pharmacology 33 (3): 226–9. doi:10.1002/j.1552-4604.1993.tb03948.x. PMID 8463436.
Enlaces externos
- Coenzima Q10 (Ubiquinona), artículo en Coenzima.com
- http://www.dsalud.com/index.php?pagina=articulo&c=737
- http://www.nlm.nih.gov/medlineplus/spanish/druginfo/natural/938.html
- Coenzima Q10 (Ubiquinol), artículo en ubiquinol.es
