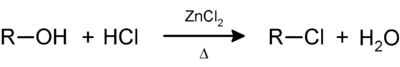
Reactivo de Lucas
El reactivo de Lucas es una solución de ZnCl2 disuelto en HCl concentrado que se usa en química orgánica. Esta disolución es usada para clasificar alcoholes de bajo peso molecular. La reacción es una sustitución en el cual el cloruro reemplaza el grupo hidroxilo. Un ensayo positivo es indicado por un cambio desde una solución limpia y sin color a una turbidez, que se trata de la formación de un cloroalcano.[1]
Cuando se agrega el reactivo de Lucas al alcohol, el H+ del HCl protonará el grupo -OH del alcohol, tal que el grupo saliente H2O, siendo un nucleófilo más débil que el OH-, pueda ser sustituido por el nucleófilo Cl-.
El reactivo de Lucas ofrece un medio polar en el que el mecanismo SN1 está favorecido. En la sustitución nucleofílica unimolecular, la velocidad de reacción es más rápida cuando el carbocatión intermediario está más estabilizado por un mayor número de grupos alquilo (R-) donantes de electrones, unidos al átomo de carbono cargado positivamente. Los alcoholes terciarios reaccionan inmediatamente con el reactivo de Lucas para producir turbidez, mientras que los alcoholes secundarios lo hacen en cinco minutos. Los alcoholes primarios no reaccionan significativamente con el reactivo de Lucas a temperatura ambiente.
De ahí que, el tiempo que toma la turbidez en aparecer es una medida de la reactividad del tipo de alcohol con el reactivo de Lucas, y esto es utilizado para diferenciar entre las tres clases de alcoholes:
- no hay reacción visible: alcohol primario
- la solución se turbia en 3-5 minutos: alcohol secundario
- la solución se vuelve turbia inmediatamente, y/o las fases se separan: alcohol terciario, bencílico o alílico
La prueba es llevada a cabo generalmente a temperatura ambiente.
Referencias[editar]
Bibliografía[editar]
• GUERRERO,C.A Principios de química orgánica. Guía de laboratorio. Universidad Nacional de Colombia. Departamento de Química. 2013.
Enlaces externos[editar]
- «Lucas Test for Primary, Secondary, and Tertiary Alcohols (video)». Journal of Chemical Education. 2001. Archivado desde el original el 5 de enero de 2010. Consultado el 13 de septiembre de 2009.