Dorisporfina
Apariencia
(Redirigido desde «Iseluxina»)
| Dorifornina | ||
|---|---|---|
 | ||
| Nombre IUPAC | ||
| 7-Hidroxi-6-metoxi-2-metil-1(2H)-isoquinolinona | ||
| General | ||
| Fórmula estructural |
 | |
| Fórmula molecular | C11H11NO3 | |
| Identificadores | ||
| Número CAS | 54302-47-5[1] | |
| Propiedades físicas | ||
| Apariencia | Agujas (Cloroformo) | |
| Masa molar | 205,213 g/mol | |
| Punto de fusión | 216 °C (489 K) | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
La dorifornina es un alcaloide quinolínico aislado de la corteza de Doryphora sassafras (Atherospermataceae).[2]

Derivados
[editar]En la naturaleza se han encontrado varios compuestos relacionados con la 1-isoquinolinona presentes en plantas del orden Laurales.
| Nombre | Estructura | Fórmula molecular | CAS | Masa molecular (g/mol) | Estado | Fuente natural | Otras propiedades |
|---|---|---|---|---|---|---|---|
| N-Metil-6,7-dimetoxiisoquinolona |  |
C12H13NO3 | 20323-75-5 | 219.240 | Sólido. Forma agujas PF = 112 - 113 °C (98-100 °C) | Aislado de Hernandia ovigera (Hernandiaceae), Stephania sasakii (Menispermaceae), y de las raíces de Thalictrum alpinum y Thalictrum isopyroides (Ranunculaceae)[3] | UV: [neutro]λmax245 (log ε3.8) ;270 (log ε3.11) ;280 (log ε3.18) ;290 (log ε3.18) ;335 (log ε2.9) ( MeOH) |
| Dorianina (6-Metil-1,3-dioxolo[4,5-g]isoquinolin-5(6H)-ona) |  |
C11H9NO3 | 24880-42-0 | 203.197 | Agujas (Acetona/éter de petróleo) PF = 162 - 163 °C | Aislado de Doryphora sassafras[4] | UV: [neutro]λmax230 (log ε4.45) ;250 (log ε4.51) ;255 (log ε3.85) ;295 (log ε3.91) ;325 (log ε3.67) ( MeOH) |
| N-(2-Acetil-5,6-metilenedioxibencil)-6,7-metilenedioxi-1(2H)-isoquinolinona |  |
C20H15NO6 | 813466-13-6 | Sólido cristalino (MeOH) | Aislado de Corydalis bungeana[5] | ||
| Pericampilinona A |  |
C9H9NO3 | 330847-76-2 | 179.175 | Agujas amarillo pálido 229 - 230 °C | Aislado de Aristolochia elegans y de Iseia luxurians[6] | UV: [neutro]λmax220 (log ε4.23) ;267 (log ε3.75) ;304 (log ε3.69) ( MeOH) |
| Talifolina |  |
C11H13NO3 | 21796-15-6 | 207.229 | Sólido. Forma prismas (MeOH.)PF 210 - 211 °C | Aislado de Thalictrum minus var. adiantifolium (Ranunculaceae), y de las hojas, tallos y frutos de Cryptocarya longifolia (Lauraceae)[7][8] | |
| Nortalifolina | 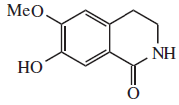 |
C10H11NO3 | 157669-72-2 | 193.202 | Sólido en barras. (Metanol/Acetona) PF = 222 - 224 °C | Aislado de los pedicelos de Lindera megaphylla[9] | |
| Coridaldina |  |
C11H13NO3 | 493-49-2 | 207.229 | Sólido. Forma agujas (butanona), prisma (benceno) 175 °C | Aislado de Berberis baluchistanica (Berberidaceae) y Enantia polycarpa , (Annonaceae)[10] | |
| N-Metilcoridaldina |  |
C12H15NO3 | 6514-05-2 | 221.255 | Sólido cristalino (MeOH, EtOH) PF = 125 - 126 °C (120.5 °C) | Aislado de Hernandia ovigera (Hernandiaceae), Papaver bracteatum, Papaver urbanianum[11] (Papaveraceae), y Thalictrum fendleri (Ranunculaceae).[12][13] También se ha obtenido por la degradación de Warifteína, Taliracebina y Adiantifolina. | |
| Oxihidrastinina |  |
C11H11NO3 | 552-29-4 | 205.213 | Sólido cristalino (éter de petróleo); PF = 98 °C | Aislado de Fumaria schleicheri, Argemone mexicana y Papaver dubium var. glabrum (Fumariaceae, Papaveraceae)[14][15]
Physical Description: Cryst. (petrol) |
UV: [neutro0]λmax207</samll> (log ε4.39) ;217 (log ε4.47) ;222 (log ε4.46) ;262 (log ε3.84) ;303 (log ε3.9) ( MeOH) |
| N-Desmetildorifornina (Nordorifornina) |  |
C10H9NO3 | 711006-89-2 | 191.186 | Barras (MeOH); PF = 257 - 259 °C | Aislado de las raíces de Menispermum dauricum[16] | UV: [neutro]λmax243 (log ε3.24) ;279 (log ε1.14) ;290 (log ε1.17) ;325 (log ε0.83) ( MeOH) |
| 7-Hidroxi-6-metoxi-1(2H)-isoquinolinona |  |
C10H9NO3 | 711006-89-2 | 191.186 | Columnas (MeoH) PF = 257 - 259 °C | Aislado de Menispermum dauricum | UV: [neutol]λmax243 (log ε3.24) ;279 (log ε1.14) ;290 (log ε1.17) ;325 (log ε0.83) ( MeOH) |
| 6,7-Dimetoxi-1(2H)-isoquinolinona |  |
C11H11NO3 | 16101-63-6 | 205.213 | Sólido cristalino (Cloroformo/Benceno) PF = 244 - 245° | UV: [neutro]λmax246 (log ε4.26) ;253 (log ε4) ;268 (log ε3.45) ;278 (log ε3.48) ;290 (log ε3.51) ;310 (log ε3.25) ;322 (log ε3.35) ;335 (log ε3.24) ( EtOH) | |
| 3,4-Deshidronoroxihidrastinina |  |
C10H7NO3 | 24188-76-9 | 189.170 | Sólido cristalino (Cloroformo o etanol); agujas (benceno/acetona) PF = 278 °C (268-270 °C) | Aislado de Corydalis bungeana y Thalictrum rugosum | |
| Iseluxina | 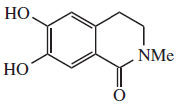 |
C9H9NO3 | 330847-76-2 | 179.175 | Agujas amarillo pálido PF = 229 - 230 °C | Aislado de from Aristolochia elegans e Iseia luxurians[17] | UV: [neutro]λmax220 (log ε4.23) ;267 (log ε3.75) ;304 (log ε3.69) ( MeOH) |
| Noroxihidrastinina |  |
C10H9NO3 | 21796-14-5 | 191.186 | Sólido cristalino (MeOH o benceno) | Aislado de Fumaria parviflora, Corydalis ophiocarpa, y de las raíces de Thalictrum alpinum, Thalictrum minus var. adianthifolium, Thalictrum rugosum y Thalictrum foliolosum (Ranunculaceae)[18][19] |
Referencias
[editar]- ↑ Número CAS
- ↑ Chen, C.R. et al., J. Nat. Prod., 1974, 37, 493
- ↑ Belgaonkar, V.H. et al., J. Het. Chem., 1978, 15, 257- 261
- ↑ Gharbo, S.A. et al., J. Nat. Prod., 1965, 28, 237- 244
- ↑ Xie, C. et al., Phytochemistry, 2004, 65, 3041- 3047
- ↑ Wu, T.-S. et al., J. Nat. Prod., 2002, 65, 1522- 1525
- ↑ Doskotch, R.W. et al., Tetrahedron, 1969, 25, 469- 475
- ↑ Bick, I.R.C. et al., Aust. J. Chem., 1981, 34, 195- 207
- ↑ Chou, C.-J. et al., J. Nat. Prod., 1994, 57, 689- 694
- ↑ Shamma, M. et al., JACS, 1974, 96, 7809- 7811
- ↑ Jackson, A.H. et al., JCS Perkin 1, 1974, 1911- 1920
- ↑ Theuns, H.G. et al., Phytochemistry, 1977, 16, 753- 755
- ↑ Cava, M.P. et al., Tet. Lett., 1966, 4279- 4282
- ↑ Markosyan, S.S. et al., Arm. Khim. Zh., 1976, 29, 1053- 1057
- ↑ Hussain, S.F. et al., Phytochemistry, 1983, 22, 319- 320
- ↑ Zhang, X. et al., Phytochemistry, 2004, 65, 929- 932
- ↑ Schimming, T. et al., Z. Naturforsch., C, 2000, 55, 1023- 1025
- ↑ Wu, W.-N. et al., J. Nat. Prod., 1980, 43, 372- 381
- ↑ Hanaoka, M. et al., Chem. Pharm. Bull., 1982, 30, 2793- 2796
