Diu hormonal
| Diu hormonal | ||
|---|---|---|
 Dispositivo intrauterino (DIU) con progestágeno | ||
El dispositivo intrauterino (DIU) o diu [1] con progestágeno es un dispositivo intrauterino que libera la hormona levonorgestrel. Se utiliza para el control de la natalidad, los períodos menstruales abundantes y para prevenir la acumulación excesiva del revestimiento del útero en aquellos que reciben terapia de reemplazo de estrógenos. Es una de las formas más efectivas de anticoncepción con una tasa de fracaso anual de alrededor del 0.2%. El dispositivo se coloca en el útero y dura de tres a cinco años. Después de la eliminación, la fertilidad vuelve rápidamente.
Los efectos secundarios incluyen períodos irregulares, quistes ováricos benignos, dolor pélvico y depresión. En raras ocasiones puede ocurrir una perforación uterina. No se recomienda su uso durante el embarazo, pero es seguro con la lactancia. El DIU con progestágeno es un tipo de anticoncepción reversible de acción prolongada. Funciona al esperar la mucosidad en la abertura del cuello uterino, deteniendo la acumulación del revestimiento del útero y, ocasionalmente, evitando la ovulación.
El DIU con levonorgestrel se aprobó por primera vez para uso médico en 1990 en Finlandia y en los Estados Unidos en 2000.[2] Está en la Lista de Medicamentos Esenciales de la Organización Mundial de la Salud, los medicamentos más efectivos y seguros que se necesitan en un sistema de salud. El costo mayorista en el mundo en desarrollo es de aproximadamente 122,46 dólares cada uno. En el Reino Unido cuestan al NHS alrededor de 88 libras. En los Estados Unidos cuestan alrededor de 844 dólares. Más de 120 países han aprobado el dispositivo y lo usan más de 10 millones de mujeres.[3]
Usos médicos
[editar]Además del control de la natalidad, el DIU hormonal se usa para la prevención y el tratamiento de:
- Períodos menstruales abundantes[4]
- Endometriosis y dolor pélvico crónico[4][5]
- Adenomiosis y dismenorrea
- Anemia[4][6]
- En algunos casos, el uso de un DIU hormonal puede evitar la necesidad de una histerectomía.
Ventajas Considerado una de las formas más efectivas de control de la natalidad reversible[7]
- Se puede usar durante la lactancia
- No se necesitan preparativos antes de tener relaciones sexuales,[8] aunque se recomienda la verificación rutinaria de las cuerdas del dispositivo por parte del paciente y del médico para garantizar que la colocación correcta permanezca intacta.[9]
- El 90% de las usuarias que desean quedar embarazadas lo hacen dentro de los 24 meses posteriores a la extracción.[10]
- Puede experimentar períodos más ligeros (algunas mujeres dejan de tener períodos por completo)[11]
- Efectivo de tres a cinco años (dependiendo del diu).[12]
Inconvenientes
- A menudo ocurren períodos irregulares y manchas entre períodos después de la inserción.
- Incomodidad leve a moderada durante el procedimiento de inserción, que incluye calambres o dolor de espalda.
- Otros posibles efectos adversos y riesgos.
Efectividad
[editar]Después de la inserción, oficialmente es efectivo hasta cinco años, aunque varios estudios han demostrado que sigue siendo efectivo durante siete años. Está aprobado para su uso hasta 7 años en Europa.
- El diu hormonal es un anticonceptivo reversible de acción prolongada y se considera una de las formas más efectivas de control de la natalidad. La tasa de fracaso del primer año para el diu hormonal es del 0,2% y la tasa de fracaso a cinco años es del 0,7%. Estas tasas son comparables a la esterilización tubárica, pero a diferencia de la esterilización, los efectos del diu hormonal son reversibles.
- El diu hormonal se considera más efectivo que otras formas comunes de anticoncepción reversible, como la píldora anticonceptiva, ya que requiere poca acción por parte de la usuaria después de la inserción.[7] La efectividad de otras formas de control de la natalidad disminuye debido a las propias usuarias. Si los regímenes de medicamentos para la anticoncepción no se siguen con precisión, el método se vuelve menos eficaz. Los dius no requieren un régimen diario, semanal o mensual, por lo que su tasa de falla de uso típico es, por lo tanto, la misma que su tasa de falla de uso perfecto.
En mujeres con útero bicorne y que necesitan anticoncepción, generalmente se aplican dos dius (uno en cada cuerno) debido a la falta de evidencia de eficacia con un solo diu. Faltan pruebas sobre el uso de diu progestágeno para la menorragia en útero bicorne, pero el informe de un caso mostró un buen efecto con un solo diu para este propósito.[13]
Contraindicaciones
[editar]Un diu hormonal no tendría que ser utilizado por mujeres que:
- Están embarazadas o piensan que pueden estarlo.
- Tiene sangrado vaginal anormal que no ha sido explicado
- Tengan cáncer cervical o uterino no tratado
- Tiene, o puede tener, cáncer de mama
- Tengan anomalías en el cuello uterino o el útero
- Ha tenido enfermedad inflamatoria pélvica en los últimos 3 meses
- Ha tenido una ITS como clamidia o gonorrea en los últimos 3 meses
- Tiene una enfermedad hepática o tumor
- Tiene alergia al levonorgestrel o a alguno de los ingredientes inactivos incluidos en el dispositivo
La inserción de un DIU no se recomienda en las mujeres que han tenido un aborto en las últimas cuatro semanas. Para reducir el riesgo de infección, no se recomienda la inserción de un diu en las mujeres que han tenido un aborto con medicación pero que aún no se han hecho una ecografía para confirmar que el aborto fue completo o que aún no han tenido su primera menstruación después del aborto con medicación.
Se puede encontrar una lista completa de contraindicaciones en los Criterios médicos de elegibilidad de la OMS para el uso de anticonceptivos y los Criterios médicos de elegibilidad para uso anticonceptivo de los Estados Unidos.[14]
Efectos secundarios
[editar]- Patrón menstrual irregular: sangrado irregular y manchado son comunes en los primeros 3 a 6 meses de uso. Después de eso, los períodos de tiempo se vuelven más cortos y el 20% de las mujeres dejan de tener períodos después de 1 año de uso.[15][16]
- Calambres y dolor: muchas mujeres sienten incomodidad o dolor durante e inmediatamente después de la inserción. Algunas mujeres pueden tener calambres durante las primeras 1-2 semanas después de la inserción.
- Expulsión: a veces el diu puede salirse del útero. Esto se denomina expulsión. Alrededor del 5% de las usuarias de diu experimentan la expulsión. Si esto sucede, la mujer no está ya protegida del embarazo. La expulsión es más común en mujeres jóvenes, mujeres que no han tenido hijos y cuando se inserta un diu inmediatamente después del parto o el aborto.[17][18][19]
- Perforación: muy rara vez, el diu se puede empujar a través de la pared del útero durante la inserción. El riesgo de perforación está determinado principalmente por la habilidad del médico que realiza la inserción. Para médicos experimentados, el riesgo de perforación es de 1 por 1000 inserciones o menos. Con las inserciones posparto, la perforación del útero es más probable que ocurra cuando la involución uterina es incompleta; La involución por lo general se completa entre 4 y 6 semanas después del parto. Se aplican consideraciones especiales a las mujeres que planean amamantar. Si se produce una perforación, puede dañar los órganos internos y, en algunos casos, se necesita cirugía para extraer el diu.
- Complicaciones del embarazo: aunque el riesgo de embarazo con un diu es muy pequeño, si ocurre uno, existe un mayor riesgo de problemas graves. Estos incluyen embarazo ectópico, infección, aborto espontáneo y parto prematuro. Hasta la mitad de los embarazos pueden ser ectópicos. La tasa de incidencia de embarazos ectópicos es de aproximadamente 1 por cada 1000 usuarios por año. Se recomienda la extracción inmediata del diu en caso de embarazo.
- Infección: la inserción del diu tiene un pequeño riesgo de enfermedad inflamatoria pélvica (EIP). La infección concurrente con gonorrea o clamidia en el momento de la inserción aumenta el riesgo de enfermedad inflamatoria pélvica. Si se produce EIP, lo más probable es que suceda dentro de los 21 días posteriores a la inserción. El dispositivo en sí no aumenta el riesgo de infección.[20] Quistes ováricos: los folículos agrandados (quistes ováricos) se han diagnosticado en aproximadamente el 12% de los sujetos que usan un diu hormonal. La mayoría de estos folículos son asintomáticos, aunque algunos pueden estar acompañados por dolor pélvico o dispareunia. En la mayoría de los casos, los folículos agrandados desaparecen espontáneamente después de dos o tres meses. No suele ser necesaria la intervención quirúrgica.[21]
- Cambios en la salud mental que incluyen: nerviosismo, estado de ánimo deprimido, cambios de humor[20]
- Aumento de peso[20]
- Dolor de cabeza, migraña[20]
- Náusea[20]
- Acnée
- Exceso de vello
- Dolor abdominal o lumbar
- Disminución de la libido
- Picazón, enrojecimiento o hinchazón de la vagina
- Secreción vaginal
- Dolor de pecho, sensibilidad
- Edema
- Distensión abdominal
- Cervicitis
- Puede afectar la tolerancia a la glucosa
- Puede experimentar un cambio en la visión o la tolerancia de lentes de contacto
- Puede agotar la vitamina B1 lo que puede afectar a la energía, el estado de ánimo y el funcionamiento del sistema nervioso
- Una "espiral perdida" ocurre cuando el hilo no puede ser sentido por una mujer en la revisión de rutina y no se ve en el examen con espéculo. Se pueden usar varios dispositivos colectores de hilo o pinzas simples para tratar de agarrar el dispositivo a través del cuello uterino. En los casos poco frecuentes en que esto no sea posible, se puede realizar una ecografía para verificar la posición de la espiral y excluir su perforación a través de la cavidad abdominal o su expulsión previa no reconocida.
Cáncer
[editar]Según una evaluación de 1999 de los estudios realizados sobre el control de la natalidad solo con progestina realizada por la Agencia Internacional para la Investigación del Cáncer, existen algunas pruebas de que el control de la natalidad solo con progestina reduce el riesgo de cáncer de endometrio. La IARC concluyó que no hay evidencia de que el control de la natalidad solo con progestina aumente el riesgo de cáncer, aunque los estudios disponibles eran demasiado pequeños para ser definitivamente concluyentes.[22]
La progesterona es una hormona en el endometrio que contrarresta el crecimiento impulsado por el estrógeno. Los niveles muy bajos de progesterona harán que los estrógenos actúen más, lo que provocará hiperplasia endometrial y adenocarcinoma. Estos efectos se pueden minimizar si se tratan con progestina, pero no en muchos casos.
El estrógeno y la progesterona tienen una relación antagónica. El estrógeno promueve el crecimiento del revestimiento endometrial, mientras que la progesterona lo limita. En el caso del cáncer de endometrio, la progesterona puede regular negativamente el crecimiento impulsado por el estrógeno. Los tumores formados se correlacionan con la insufiencia de progesterona y el exceso de estrógeno. En pacientes con cáncer de endometrio que usa progestina, la liberación de los dius dio resultados mixtos.
Densidad ósea
[editar]No se han identificado pruebas para sugerir que el diu hormonal afecte la densidad mineral ósea (DMO). Dos estudios pequeños, limitados al estudio de la DMO en el antebrazo, no muestran disminución en la DMO. Uno de los estudios mostró a los 7 años de uso una DMO similar en la parte media del cúbito y en el radio distal a la de usuariosde igual edad e IMC. Además, las mediciones de DMO fueron similares a los valores esperados para las mujeres en el mismo grupo de edad que las participantes. Los autores del estudio dijeron que sus resultados eran predecibles, ya que está bien establecido que el principal factor responsable de la pérdida ósea en las mujeres es el hipoestrogenismo y, de acuerdo con informes anteriores, encontraron que los niveles de estradiol en los usuarios del diu eran normales.
Composición y liberación hormonal
[editar]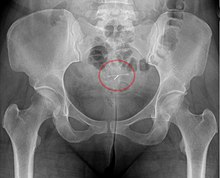
El diu hormonal es una pequeña pieza de plástico en forma de "T" que contiene levonorgestrel, un tipo de progestina.[23] El cilindro del dispositivo está recubierto con una membrana que regula la liberación de la droga.[24] El diu libera el medicamento a una tasa inicial de ente 6 y 20 microgramos por día, según el modelo.En comparación, los anticonceptivos orales pueden contener 150 microgramos de levonorgestrel. El diu hormonal libera el levonorgestrel directamente en el útero, por lo que sus efectos son en su mayoría paracrinos más que sistémicos. La mayor parte del medicamento permanece dentro del útero, y solo una pequeña cantidad se absorbe en el resto del cuerpo. Los niveles sanguíneos de levonorgestrel son una décima parte de los que se encuentran en usuarios de pastillas de levonorgestrel solo.</ref>
Inserción y extracción
[editar]

El diu hormonal se inserta en un procedimiento similar al diu de cobre no hormonal, y solo puede ser insertado por un médico calificado. Antes de la inserción, se realiza un examen pélvico para examinar la forma y la posición del útero. También se recomienda que los pacientes sean examinados para detectar gonorrea y clamidia antes de la inserción, ya que una ITS en el momento de la inserción puede aumentar el riesgo de infección pélvica. Sin embargo, si una persona ha sido examinada previamente y no hay evidencia de infección en el examen, no es necesario retrasar la inserción del diu.[25]
Durante la inserción, la vagina se mantiene abierta con un espéculo, el mismo dispositivo que se usa durante la prueba de Papanicolaou. Se usa un instrumento de agarre para estabilizar el cuello uterino, se mide la longitud del útero para una inserción adecuada y se coloca el diu con un tubo angosto a través de la abertura del cuello uterino hacia el útero. Un tramo corto de monofilamento de plástico/nylon cuelga del cuello uterino hacia la vagina. La cuerda permite que los médicos y los pacientes verifiquen que el diu esté todavía en su lugar y permite una fácil extracción del dispositivo. Pueden ocurrir durante el procedimiento calambres de leves a moderados, que generalmente duran cinco minutos o menos. La inserción se puede realizar inmediatamente después del parto y después del aborto si no se ha producido una infección. El misoprostol no es efectivo para reducir el dolor en la inserción del diu.[26]
La extracción del dispositivo también debe ser realizada por un médico calificado. Después de la eliminación, la fertilidad volverá a niveles previos de manera relativamente rápida. Un estudio encontró que la mayoría de las participantes volvió a la fertilidad dentro de los tres meses.[27]
Mecanismos de acción
[editar]Levonorgestrel es un progestágeno, es decir, agonista del receptor de progesterona. El principal mecanismo de acción del diu hormonal es prevenir la fertilización.[28][29][30][31] El sistema intrauterino de levonorgestrel tiene varios efectos anticonceptivos:
- El interior del útero se vuelve mortal para los espermatozoides[32]
- El moco cervical se espesa
- La ovulación no está inhibida[33]
- También pueden adelgazar el revestimiento endometrial y potencialmente afectar la implantación, pero esta no es la función habitual.[34]
Numerosos estudios han demostrado que los dius evitan principalmente la fertilización, no la implantación. En un experimento que involucró el lavado tubárico, se encontraron óvulos fertilizados en la mitad de las mujeres que no usaban anticonceptivos, pero no se encontraron óvulos fertilizados en mujeres que usaban el diu. Los dius también disminuyen el riesgo de embarazo ectópico, lo que implica además que los dius impiden la fertilización
Historia
[editar]Los dius hormonales se desarrollaron en la década de 1970, después del desarrollo del diu de cobre en los años sesenta y setenta. El Dr. Antonio Scommenga, que trabaja en el Hospital Michael Reese en Chicago, descubrió que la administración de progesterona dentro del útero podría tener beneficios anticonceptivos. Con conocimiento del trabajo de Scommegna, un médico finlandés, Jouni Valtteri Tapani Luukkainen, creó el diu en forma de "T" que liberaba progesterona, comercializado como el Sistema Progestasert en 1976. Este diu tenía una vida útil corta, de 1 año y nunca alcanzó popularidad generalizada. Después de esta relativa falta de éxito, el Dr. Luukkainen reemplazó la progesterona con la hormona levonorgestrel para ser liberada durante un período de 5 años, creando el actual DIU.
El diu se estudió por seguridad y eficacia en dos ensayos clínicos en Finlandia y Suecia en los que participaron 1.169 mujeres que tenían entre 18 y 35 años de edad al comienzo de los ensayos. Los ensayos incluyeron mujeres predominantemente caucásicas que habían estado embarazadas previamente sin antecedentes de embarazo ectópico o enfermedad inflamatoria pélvica durante el año anterior. Más del 70% de los participantes habían usado diu previamente.[35]
Controversias
[editar]En 2009, Bayer, el fabricante de uno de estos dispositivos, recibió una advertencia de la FDA de la Administración de Drogas y Alimentos de los Estados Unidos por exagerar la eficacia, minimizar los riesgos de uso y realizar "presentaciones falsas o engañosas" sobre el dispositivo. De 2000 a 2013, la agencia federal recibió más de 70,072 quejas sobre el dispositivo y los efectos adversos relacionados. A partir de abril de 2014, se han presentado más de 1,200 demandas en los Estados Unidos[36][37][38][39]
Véase también
[editar]Referencias
[editar]- ↑ ASALE, RAE-. «diu | Diccionario de la lengua española». «Diccionario de la lengua española» - Edición del Tricentenario. Consultado el 11 de octubre de 2021.
- ↑ Bradley, Linda D.; Falcone, Tommaso (2008). Hysteroscopy: Office Evaluation and Management of the Uterine Cavity. Elsevier Health Sciences. p. 171. ISBN 0323041019.
- ↑ Schäfer-Korting, Monika (2010). Drug Delivery. Springer Science & Business Media. p. 290. ISBN 9783642004773.
- ↑ a b c «Levonorgestrel-releasing intrauterine system: uses and controversies.». Expert Review of Medical Devices 5 (4): 437-45. 2008. PMID 18573044. doi:10.1586/17434440.5.4.437.
- ↑ «Randomized clinical trial of a levonorgestrel-releasing intrauterine system and a depot GnRH analogue for the treatment of chronic pelvic pain in women with endometriosis.». Hum Reprod 20 (7): 1993-8. 2005. PMID 15790607. doi:10.1093/humrep/deh869.
- ↑ «The LNG-IUS study on adenomyosis: a 3-year follow-up on the efficacy and side effects of the use of levonorgestrel intrauterine system for the treatment of dysmenorrheal associated with adenomyosis». Contraception 79 (3): 189-193. 2009. PMID 19185671. doi:10.1016/j.contraception.2008.11.004.
- ↑ a b «Effectiveness of Long-Acting Reversible Contraception». New England Journal of Medicine 366 (21): 1998-2007. 2012. PMID 22621627. doi:10.1056/NEJMoa1110855. Archivado desde el original el 18 de febrero de 2013.
- ↑ «IUD». Planned Parenthood. Archivado desde el original el 18 de junio de 2015. Consultado el 18 de junio de 2015.
- ↑ «Convenience». Bayer. Archivado desde el original el 18 de junio de 2015. Consultado el 18 de junio de 2015.
- ↑ «Mirena». MediResource Inc. Archivado desde el original el 3 de julio de 2015. Consultado el 18 de junio de 2015.
- ↑ «Bleeding patterns and clinical performance of the levonorgestrel-releasing intrauterine system (Mirena) up to two years.». Contraception 65 (2): 129-132. February 2002. PMID 11927115. doi:10.1016/s0010-7824(01)00302-x.
- ↑ «Mirena (hormonal IUD)». Mayo Clinic. 10 de enero de 2015. Archivado desde el original el 9 de julio de 2015. Consultado el 18 de junio de 2015.
- ↑ «Successful management of intractable menorrhagia with a levonorgestrel-releasing intrauterine device, in a woman with a bicornuate uterus». J Obstet Gynaecol 18 (4): 392-3. July 1998. PMID 15512123. doi:10.1080/01443619867263.
- ↑ WHO (2010). «Intrauterine devices (IUDs)». Medical Eligibility Criteria for Contraceptive Use (4th edición). Geneva: Reproductive Health and Research, WHO. ISBN 978 92 4 1563888.
- ↑ McCarthy L (2006). «Levonorgestrel-Releasing Intrauterine System (Mirena) for Contraception». Am Fam Physician 73 (10): 1799-. Archivado desde el original el 26 de septiembre de 2007. Consultado el 4 de mayo de 2007.
- ↑ Rönnerdag M, Odlind V (1999). «Health effects of long-term use of the intrauterine levonorgestrel-releasing system. A follow-up study over 12 years of continuous use». Acta Obstet Gynecol Scand 78 (8): 716-21. PMID 10468065. doi:10.1034/j.1600-0412.1999.780810.x.
- ↑ IUDs—An Update. «Chapter 2.7:Expulsion». Archivado desde el original el 5 de septiembre de 2006.
- ↑ IUDs—An Update. «Chapter 3.3 Postpartum Insertion». Archivado desde el original el 29 de abril de 2006.
- ↑ IUDs—An Update. «Chapter 3.4 Postabortion Insertion». Archivado desde el original el 11 de agosto de 2006.
- ↑ a b c d e «Mirena: Consumer Medicine Information». Bayer. March 2014. Archivado desde el original el 27 de abril de 2014. Consultado el 27 de abril de 2014.
- ↑ Bahamondes L; Hidalgo M; Petta CA; Diaz J; Espejo-Arce X; Monteiro-Dantas C. (2003). «Enlarged ovarian follicles in users of a levonorgestrel-releasing intrauterine system and contraceptive implant». J. Reproduc. Med. 48 (8): 637-640. PMID 12971147.
- ↑ Hormonal Contraceptives, Progestogens Only. International Agency for Research on Cancer. 1999. Archivado desde el original el 28 de septiembre de 2006. Consultado el 8 de octubre de 2006.
- ↑ «Archived copy». Aust N Z J Obstet Gynaecol 50 (3): 273-9. 2010. PMID 20618247. doi:10.1111/j.1479-828X.2010.01152.x. Archivado desde el original el 31 de julio de 2012. Consultado el 19 de julio de 2012., Bayer Pharmaceuticals.
- ↑ Luukkainen, T. (1991). «Levonorgestrel-Releasing Intrauterine Device». Annals of the New York Academy of Sciences 626: 43-49. doi:10.1111/j.1749-6632.1991.tb37898.x.
- ↑ «CDC - Summary - US SPR - Reproductive Health». www.cdc.gov (en inglés estadounidense). 21 de junio de 2017. Archivado desde el original el 13 de septiembre de 2017. Consultado el 13 de septiembre de 2017.
- ↑ Lopez, LM; Bernholc, A; Zeng, Y; Allen, RH; Bartz, D; O'Brien, PA; Hubacher, D (29 de julio de 2015). «Interventions for pain with intrauterine device insertion.». The Cochrane Database of Systematic Reviews 7: CD007373. PMID 26222246. doi:10.1002/14651858.CD007373.pub3.
- ↑ «Return to fertility after IUD removal for planned pregnancy». Contraception 32 (3): 253-259. 1985. doi:10.1016/0010-7824(85)90048-4.
- ↑ Ortiz, María Elena; Croxatto, Horacio B. (June 2007). «Copper-T intrauterine device and levonorgestrel intrauterine system: biological bases of their mechanism of action». Contraception 75 (6 Suppl): S16‒S30. PMID 17531610. doi:10.1016/j.contraception.2007.01.020.Ortiz, María Elena; Croxatto, Horacio B. (June 2007). «Copper-T intrauterine device and levonorgestrel intrauterine system: biological bases of their mechanism of action». Contraception 75 (6 Suppl): S16‒S30. PMID 17531610. doi:10.1016/j.contraception.2007.01.020. p. S28:
- ↑ ESHRE Capri Workshop Group (May–June 2008). «Intrauterine devices and intrauterine systems». Human Reproduction Update 14 (3): 197‒208. PMID 18400840. doi:10.1093/humupd/dmn003.ESHRE Capri Workshop Group (May–June 2008). «Intrauterine devices and intrauterine systems». Human Reproduction Update 14 (3): 197‒208. PMID 18400840. doi:10.1093/humupd/dmn003. p. 199:
- ↑ Speroff, Leon; Darney, Philip D. (2011). «Intrauterine contraception». A clinical guide for contraception (5th edición). Philadelphia: Lippincott Williams & Wilkins. pp. 239-280. ISBN 978-1-60831-610-6.Speroff, Leon; Darney, Philip D. (2011). «Intrauterine contraception». A clinical guide for contraception (5th edición). Philadelphia: Lippincott Williams & Wilkins. pp. 239–280. ISBN 978-1-60831-610-6. pp. 246–247:
- ↑ Jensen, Jeffrey T.; Mishell, Daniel R. Jr. (2012). «Family planning: contraception, sterilization, and pregnancy termination». En Lentz, Gretchen M. Comprehensive gynecology. Philadelphia: Mosby Elsevier. pp. 215-272. ISBN 978-0-323-06986-1.Jensen, Jeffrey T.; Mishell, Daniel R. Jr. (2012). «Family planning: contraception, sterilization, and pregnancy termination». En Lentz, ed. Comprehensive gynecology. Philadelphia: Mosby Elsevier. pp. 215-272. ISBN 978-0-323-06986-1.
|editor=y|apellido-editor=redundantes (ayuda)Jensen, Jeffrey T.; Mishell, Daniel R. Jr. (2012). «Family planning: contraception, sterilization, and pregnancy termination». En Lentz, ed. Comprehensive gynecology. Philadelphia: Mosby Elsevier. pp. 215-272. ISBN 978-0-323-06986-1. p. 259: - ↑ «Endometrial effects of intrauterine levonorgestrel». Contraception 75 (6 Suppl.): S93-S98. 2007. PMID 17531624. doi:10.1016/j.contraception.2007.01.015.«Endometrial effects of intrauterine levonorgestrel». Contraception 75 (6 Suppl.): S93-S98. 2007. PMID 17531624. doi:10.1016/j.contraception.2007.01.015.
- ↑ Malik, S (January 2013). «Levonorgestrel-IUS system and endometrial manipulation.». Journal of mid-life health 4 (1): 6-7. PMC 3702070. PMID 23833526. doi:10.4103/0976-7800.109625.Malik, S (January 2013). «Levonorgestrel-IUS system and endometrial manipulation.». Journal of mid-life health 4 (1): 6-7. PMC 3702070. PMID 23833526. doi:10.4103/0976-7800.109625.
- ↑ ESHRE Capri Workshop, Group (2008). «Intrauterine devices and intrauterine systems.». Human Reproduction Update 14 (3): 197-208. PMID 18400840. doi:10.1093/humupd/dmn003. «Both copper IUDs and levonorgestrel releasing IUSs may interfere with implantation».ESHRE Capri Workshop, Group (2008). «Intrauterine devices and intrauterine systems.». Human Reproduction Update 14 (3): 197-208. PMID 18400840. doi:10.1093/humupd/dmn003. «Both copper IUDs and levonorgestrel releasing IUSs may interfere with implantation».
- ↑ «MIRENA - levonorgestrel intrauterine device». Bayer Health Pharmaceuticals. May 2009. Archivado desde el original el 18 de junio de 2015. Consultado el 18 de junio de 2015.
- ↑ Mosher, Steven (20 de noviembre de 2012). «The Mirena IUD is Becoming More Popular - and the Lawsuits are Piling Up». Population Research Institute. Archivado desde el original el 6 de julio de 2015. Consultado el 18 de junio de 2015.
- ↑ Bekiempis, Victoria (24 de abril de 2014). «The Courtroom Controversy Behind Popular Contraceptive Mirena». Journal of mid-life health (Newsweek) 4 (1): 6-7. PMC 3702070. PMID 23833526. doi:10.4103/0976-7800.109625. Archivado desde el original el 15 de noviembre de 2016. Consultado el 16 de noviembre de 2016.
- ↑ «Popular contraceptive device Mirena target of lawsuits in Canada, U.S». CTV. 21 de mayo de 2014. Archivado desde el original el 26 de octubre de 2016. Consultado el 16 de noviembre de 2016.
- ↑ Blackstone, Helena (31 de mayo de 2016). «When IUDs Go Terribly Wrong». Vice. Archivado desde el original el 17 de noviembre de 2016. Consultado el 16 de noviembre de 2016.
Enlaces externos
[editar]- FDA (2000). «Medical review» (PDF scanned image). " (PDF imagen escaneada)". - En Berlex Laboratorios' Mirena aplicación
- Physician Hoja de hecho (2008 versión de EE.UU.)
- Physician Hoja de hecho (2013 U.K. Versión)
- Mirena Efectos de lado/de descripción de fármaco
- El vídeo que muestra el procedimiento de inserción para un Mirena IUD
