Liriodenina
| Liriodenina | ||
|---|---|---|
 | ||
| Nombre IUPAC | ||
| 8H-Benzo[g]-1,3-benzodioxolo[6,5,4-de]quinolin-8-ona | ||
| General | ||
| Fórmula estructural |
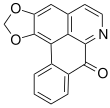 | |
| Fórmula molecular | C17H9NO3 | |
| Identificadores | ||
| Número CAS | 475-75-2[1] | |
| ChEBI | 70649 | |
| ChEMBL | CHEMBL37736 | |
| ChemSpider | 9738 | |
| PubChem | 10144 | |
| UNII | E134R7X4O9 | |
| KEGG | C09567 | |
| Propiedades físicas | ||
| Apariencia | Agujas amarillas (cloroformo) | |
| Masa molar | 275,263 g/mol | |
| Punto de fusión | 275 °C (548 K) | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
La liriodenina es un alcaloide dioxoloaporfínico aislado de una gran variedad de plantas de las familias Annonaceae (Annona, Asimina, Cananga, Cleistopholis, Enantia, Fusaea, Isolona, Guatteria, Melodorum, Pseuduvaria, Hexalobus, Mitrella, Monodora, Pachypodanthium, Polyalthia, Uvariopsis, Schefferomitra, Xylopia), Araceae (Lysichiton), Eupomatiaceae (Eupomatia), Lauraceae (Litsea, Neolitsea), Magnoliaceae (Liriodendron,Magnolia, Michelia, Elmerrillia, Talauma), Menispermaceae (Pycnarrhena, Stephania, Chasmanthera,Pachygone, Rhigiocarya), Monimiaceae (Dryadodaphne), Nelumbonaceae (Nelumbo), Papaveraceae (Roemeria, Papaver), Rhamnaceae (Colubrina), Rutaceae (Zanthoxylum), Atherospermataceae (Atherosperma, Doryphora, Laurelia) y Siparunaceae (Siparuna). Coeficiente de partición calculado Log P:2.94; UV: [ácido]λmax257 (ε21400) ;277 (ε18200) ;329 (ε4680) ;392 (ε4900) ;455 (ε3800) (EtOH/HCl) [neutro]λmax248 (ε16600) ;268 (ε13500) ;309 (ε4170) ;413 (ε6610) ( EtOH) [neutro]λmax247 (ε10960) ;267 (ε9550) ;310 (ε2884) ;413 (ε4680) ( MeOH) [neutro]λmax204;248;268;311;415 (EtOH).[2]
Actividad biológica
Este alcaloide presenta actividad contra Leishmania. La Liriodenina inhibe la proliferación de líneas celulares de hepatoma humano por bloqueo de la progresión del ciclo celular y de la activación del óxido nítrico de la expresión de p53.[3] También inhibe la topoisomerasa II.[4] La liriodenina presenta un efecto anticancerígeno en células SW480 de colon por inducción del inhibición en la fase G1/S.[5] También tiene citotoxicidad moderada contra las células de carcinoma nasofaríngeo humano. También tiene actividad contra Trichophyton mentagraphytes y Syncephalestrum racemosum. También es efectivo contra la mancha reticular de la cebada y la enfermedad de la mancha del grano de cacao. Tiene un espectro amplio como antimicrobiano y es activo contra bacterias gram-positivas, así como levaduras y hongos.[6] Es un antagonista de los receptores muscarínicos. Es un mutágeno.[7]
Síntesis
La irradiación de etil (Z)-l-(2-bromobenziliden)-6,7-metilenedioxi-1,2,3,4-tetrahidroisoquinolina- 2-carboxilato de etilo produjo 6,7-dihidro-5H-benzo[g]-1,3-benzodioxolo[6,5,4-de]quinolina-7-carboxilato de etilo, seguido de la reducción con hidruro de litio y alumino para dar el derivado 7-metilo. La oxidación posterior de este precursor da liriodenina con rendimiento moderado[8]

Referencias
- ↑ Número CAS
- ↑ Bick, I.R.C. et al., Tet. Lett., 1964, 1629
- ↑ Hsieh et al., Liriodenine inhibits the proliferation of human hepatoma cell lines by blocking cell cycle progression and nitric oxide-mediated activation of p53 expression. Food and Chemical Toxicology, (2005) 43(7):1117-1126
- ↑ Sung Ho Woo et al.,Inhibition of topoisomerase II by liriodenine. Biochemical Pharmacology (1997) 54(4): 467-473
- ↑ Chen et al., Process Biochemistry (2012) 47(10):1460-1468
- ↑ Hufford, C. D., Funderburk, M. J., Morgan, J. M., and Robertson, L. W., J. Pharnz. Sci., 1975,64,789
- ↑ Pharmacological characteristics of liriodenine, isolated from Fissistigma glaucescens, a novel muscarinic receptor antagonist in guinea-pigs. Lin CH et al.Br J Pharmacol. (1994) 113(1):275-81.
- ↑ Nimgirawath, S. et al., Aust. J. Chem., 1983, 36, 1061
