Diferencia entre revisiones de «Alcaloide»
m Revertidos los cambios de 200.120.53.149 a la última edición de Diegusjaimes |
|||
| Línea 20: | Línea 20: | ||
== Genalcaloides == |
== Genalcaloides == |
||
Los genalcaloides |
Los genalcaloides -u [[óxido]]s aminados de alcaloide- son derivados por oxidación de los alcaloides que contienen el grupo R=(NO)-R, donde el [[nitrógeno]] tiene [[valencia atómica|valencia]] V, en contraposición a los alcaloides normales, donde es trivalente (R=N-R). Su acción es la misma que la del alcaloide del cual provienen, pero es más pausada. Se nombran añadiendo el prefijo gen- al nombre del alcaloide. Algunos se encuentran en estado natural, como la gen[[eserina]] del [[Strychnos ignatii|haba de Calabar]]. |
||
Químicamente pueden ser considerados como -heterocíclicos nitrogenados- derivados de aminoácidos y de los triterpenos. se encuentran formando sales con el ácido acético, oxálico, láctico, málico, tartárico y cítrico. sus actividades biológicas son importantes por su mimetismo hormonal y su intervención en las reacciones principales del metabolismo celular. a pesar de ser sustancias poco similares entre ellas desde el punto de vista estructural, poseen propiedades fisiológicas análogas. Estos compuestos están ampliamente distribuidos en el reino vegetal (25% de las plantas contienen alcaloides) y en algunas especies su concentración puede alcanzar el 10% (flores). Muchos alcaloides son la causa de intoxicaciones en humanos y animales. la forma más común es la intoxicación por infusiones con hierbas con fines medicinales, siendo esta una causa importante de muerte sobre todo en niños. su presencia en vegetales hace posible su incorporación accidental en alimentos, creando una vía fácil de intoxicación. para entender el origen estructural de estos compuestos se les suele clasificar así: |
Químicamente pueden ser considerados como -heterocíclicos nitrogenados- derivados de aminoácidos y de los triterpenos. se encuentran formando sales con el ácido acético, oxálico, láctico, málico, tartárico y cítrico. sus actividades biológicas son importantes por su mimetismo hormonal y su intervención en las reacciones principales del metabolismo celular. a pesar de ser sustancias poco similares entre ellas desde el punto de vista estructural, poseen propiedades fisiológicas análogas. Estos compuestos están ampliamente distribuidos en el reino vegetal (25% de las plantas contienen alcaloides) y en algunas especies su concentración puede alcanzar el 10% (flores). Muchos alcaloides son la causa de intoxicaciones en humanos y animales. la forma más común es la intoxicación por infusiones con hierbas con fines medicinales, siendo esta una causa importante de muerte sobre todo en niños. su presencia en vegetales hace posible su incorporación accidental en alimentos, creando una vía fácil de intoxicación. para entender el origen estructural de estos compuestos se les suele clasificar así: |
||
Revisión del 20:51 9 jun 2010
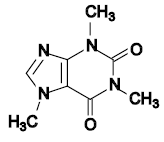
Se llaman alcaloides (de álcali, carbonatos de alcalinos, y -oide, parecido a, en forma de) a aquellos metabolitos secundarios de las plantas sintetizados, generalmente, a partir de aminoácidos. Los alcaloides verdaderos derivan de un aminoácido, son por lo tanto nitrogenados. Son básicos (excepto colchicina), y poseen acción fisiológica intensa en los animales aun a bajas dosis con efectos psicoactivos, por lo que son muy usados en medicina para tratar problemas de la mente y calmar el dolor. Ejemplos conocidos son la cocaína, la morfina, la atropina, la colchicina, la quinina, cafeína y la estricnina.
Sus estructuras químicas son variadas.[1] Se considera que un alcaloide es, por definición, un compuesto químico que posee un nitrógeno heterocíclico procedente del metabolismo de aminoácidos; de proceder de otra vía, se define como pseudoalcaloide.[2]
Generalmente actúan sobre el sistema nervioso central, si bien algunos afectan al sistema nervioso parasimpático y otras al sistema nervioso simpático, por ejemplo, la cocaína actúa impidiendo la recaptación de dopamina de la terminal sináptica, lo que produce un mayor efecto de los receptores dopaminérgicos.
La actividad biológica de los alcaloides es muy diversa, la más estudiada es la acción euforizante que presentan algunos como la cocaína, si bien también existen alcaloides con efectos depresores del sistema nervioso central como la morfina.
Los métodos de extracción son muy variados, pero últimamente está adquiriendo fuerza la purificación por medio de fluidos supercríticos, concretamente con dióxido de carbono. Para obtener los alcaloides de los vegetales, se extraen de las partes de la planta que los contienen, con agua si están en forma de sales (solubles) o con ácido clorhídrico diluido si están en forma insoluble.
En cuanto a su detección, existen multitud de métodos: procedimientos cromatográficos, reacciones coloreadas (reacción de Mayer, de Dragendorff, de Bouchardat... si bien no son específicas de los alcaloides: puede obtenerse un resultado positivo en presencia, por ejemplo, de péptidos).
Historia
El aislamiento de los primeros alcaloides en el siglo XIX coincidió más o menos con la introducción del proceso de percolación para la extraccióon de las drogas. El farmacéutico francés Charles Derosne probablemente aisló en 1803 el alcaloide denominado después narcotina, y el farmacéutico Friedrich Sertüner investigó sobre el opio y aisló la morfina. A ello siguió rápidamente el aislamiento de otros alcaloides como la estricnina, cafeína, entre otros.
La coniína es el alcaloide más antiguo en cuanto al establecimiento de su estructura y de su síntesis, pero otros, como la colchicina, necesitaron más de un siglo para que sus estructuras fuesen definidas.
Genalcaloides
Los genalcaloides -u óxidos aminados de alcaloide- son derivados por oxidación de los alcaloides que contienen el grupo R=(NO)-R, donde el nitrógeno tiene valencia V, en contraposición a los alcaloides normales, donde es trivalente (R=N-R). Su acción es la misma que la del alcaloide del cual provienen, pero es más pausada. Se nombran añadiendo el prefijo gen- al nombre del alcaloide. Algunos se encuentran en estado natural, como la geneserina del haba de Calabar.
Químicamente pueden ser considerados como -heterocíclicos nitrogenados- derivados de aminoácidos y de los triterpenos. se encuentran formando sales con el ácido acético, oxálico, láctico, málico, tartárico y cítrico. sus actividades biológicas son importantes por su mimetismo hormonal y su intervención en las reacciones principales del metabolismo celular. a pesar de ser sustancias poco similares entre ellas desde el punto de vista estructural, poseen propiedades fisiológicas análogas. Estos compuestos están ampliamente distribuidos en el reino vegetal (25% de las plantas contienen alcaloides) y en algunas especies su concentración puede alcanzar el 10% (flores). Muchos alcaloides son la causa de intoxicaciones en humanos y animales. la forma más común es la intoxicación por infusiones con hierbas con fines medicinales, siendo esta una causa importante de muerte sobre todo en niños. su presencia en vegetales hace posible su incorporación accidental en alimentos, creando una vía fácil de intoxicación. para entender el origen estructural de estos compuestos se les suele clasificar así:
Alcaloides de núcleo pirídico: a este grupo pertenecen la nicotina, la pilocarpina y la eparteína.
La nicotina se encuentra en el jugo del tabaco acompañada de otros alcaloides. es un liquido incoloro de olor semejante al tabaco y sabor ardiente y picante. Es muy tóxicas en dosis extremadas.
Alcaloides de núcleo isoquinoleico: se encuentran en las plantas papaveráceas y ranunculáceas. el más importante es la papaverina, que tiene propiedades hipnóticas (aunque no tan acentuadas como las de la morfina).
Alcaloides de núcleo fenantrénico: el más importante es la morfina. se encuentra en el opio en forma de sal. Se emplea en medicina en forma de clorhidrato y sulfato, como sedantes y calmantes.
Alcaloides de núcleo tropánico: pertenecen a este grupo la atropina y la cocaína. la atropina se encuentra en el jugo de varias plantas como la belladona y el estramonio. La cocaína se extrae de las hojas de coca, es de sabor amargo, insensibiliza la lengua, y se usa en medicina en forma de clorhidrato.
Alcaloides de núcleo indólico: los más importantes son la estricnina y la brucina. la estricnina es uno de los alcaloides más enérgicos, se extrae de diversas plantas del género strychnos, entre ellas el haba de San Ignacio y de la nuez vómica. Es de sabor amargo muy intenso y muy tóxica. su ingestión produce convulsiones tetánicas.
Alcaloides de núcleo no definido: son todos aquellos alcaloides cuya constitución no ha sido aún establecida con claridad. entre ellos se encuentra la aconitina (veneno muy violento, utilizado en terapéutica para combatir ciertas dolencias) y la ergotinina (uno de los principios activos del cornezuelo de centeno, que ejerce una acción específica sobre el útero.
Los alcaloides pirrolidininicos están asociados a estructuras de pirrolizidinas son metabolitos secundarios de una gran variedad de plantas, que incluye especies que se encuentran en todo el mundo. estas plantas son la causa de numerosos casos de envenenamiento de ganado, y ha causado grandes pérdidas económicas. También son causa de muerte en humanos, especialmente en países poco desarrollados, como consecuencia de la contaminación de cereales y semillas por lo que son de gran importancia en el campo de los alimentos. Se cree que la ingestión de hierbas y vegetales que contienen estos alcaloides, son causa de dolencias. La estructura de estos alcaloides esta basada en dos anillos de 5 átomos unidos que comparten un átomo de nitrógeno. en la naturaleza por lo general los anillos tienen como sustituyentes grupos hidroximetileno en la posición c-1 y grupos hidroxilos en c-7; esta estructura se conoce como necina. ejemplos típicos de esta base son la heliotridina y la retronecina.
Las pirrolizidinas se encuentran principalmente en las familias Compositae, Boraginacae, Leguminosae y Apocynacae. Los géneros productores de estos alcaloides están distribuidos en diferentes regiones y climas y podrían representar hasta el 3% de las plantas con flores. Algunas contienen una sola clase de pirrolizidina pero la mayoría contienen entre 5 y ocho clases. El contenido varía con cada especie, pero puede llegar a ser un porcentaje importante del peso seco. La mayor concentración se encuentra en raíces y es mayor en hojas jóvenes, inflorescencias y capullos que en hojas más viejas. En algunas especies se encontraron altas concentraciones en semillas, lo que implica un riesgo en los casos en que estas semillas sean utilizadas para la alimentación humana. Existen N-óxidos de estos alcaloides, que son más solubles en agua y son transportados más fácilmente dentro de la planta.
Referencias
- ↑ Robinson T. 1981. The biochemistry of alkaloids. 2ª ed. Springer, Nueva York.
- ↑ Azcón-Bieto,J y Talón, M. (2000). Fundamentos de Fisiología Vegetal. Mc Graw Hill Interamericana de España SAU. ISBN 84-486-0258-7.
Enlaces externos
 Wikimedia Commons alberga una galería multimedia sobre Alcaloide.
Wikimedia Commons alberga una galería multimedia sobre Alcaloide. Wikcionario tiene definiciones y otra información sobre alcaloide.
Wikcionario tiene definiciones y otra información sobre alcaloide.- Lista de alcaloides importantes en qbitácora (blog).
