Diferencia entre revisiones de «Propano»
m Revertidos los cambios de 148.202.152.114 a la última edición de Markoszarrate |
|||
| Línea 30: | Línea 30: | ||
== Generales == |
== Generales == |
||
Las mezclas de propano con el aire pueden ser explosivas con concentraciones del 1,7 - 9,3 % Vol de propano. La llama del propano al igual que la de los demás gases combustibles debe de ser completamente azul;cualquier parte amarillenta, anaranjada o rojiza de la misma denota una mala combustión. A temperatura ambiente es inerte frente a la mayor parte de los reactivos aunque reacciona por ejemplo con el bromo en presencia de luz. En elevadas concentraciones el propano tiene propiedades narcotizantes |
Las mezclas de propano con el aire pueden ser explosivas con concentraciones del 1,7 - 9,3 % Vol de propano. La llama del propano al igual que la de los demás gases combustibles debe de ser completamente azul;cualquier parte amarillenta, anaranjada o rojiza de la misma denota una mala combustión. A temperatura ambiente es inerte frente a la mayor parte de los reactivos aunque reacciona por ejemplo con el bromo en presencia de luz. En elevadas concentraciones el propano tiene propiedades narcotizantes. |
||
== Tensión de vapor == |
== Tensión de vapor == |
||
Revisión del 18:42 9 mar 2010
| Propano | ||
|---|---|---|
 | ||
| Nombre IUPAC | ||
| propano | ||
| General | ||
| Fórmula semidesarrollada | CH3CH2CH3 | |
| Fórmula estructural |
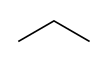 | |
| Fórmula molecular | C3H8 | |
| Identificadores | ||
| Número CAS | 74-98-6[1] | |
| Número RTECS | TX2275000 | |
| ChEBI | 32879 | |
| ChEMBL | CHEMBL135416 | |
| ChemSpider | 6094 | |
| PubChem | 6334 | |
| UNII | T75W9911L6 | |
| Propiedades físicas | ||
| Apariencia | Incoloro | |
| Densidad | 8 kg/m³; 0,008 g/cm³ | |
| Masa molar | 44 g/mol | |
| Punto de fusión | 85,5 K (−188 °C) | |
| Punto de ebullición | 231,05 K (−42 °C) | |
| Temperatura crítica | 367,15 K (94 °C) | |
| Propiedades químicas | ||
| Solubilidad en agua | 80 mg/l a 20 ºC | |
| Peligrosidad | ||
| Punto de inflamabilidad | 169,15 K (−104 °C) | |
| Temperatura de autoignición | 723,15 K (450 °C) | |
| Frases R | Plantilla:R12 | |
| Frases S | Plantilla:S2, Plantilla:S9, Plantilla:S16, | |
| Riesgos | ||
| Inhalación | Somnolencia y pérdida del conocimiento. Llevar al accidentado inmediatamente a un sitio al aire libre y mantenerlo en reposo. Respiración artificial si éste estuviese indicado. Proporcionar asistencia médica | |
| Piel | En contacto con líquido: congelación. En caso de congelación, aclarar con abundante agua. No se debe quitar la ropa. Proporcionar asistencia médica | |
| Ojos | En contacto con líquido: congelación. En caso de congelación, enjuagar con abundante agua por varios minutos. Proporcionar asistencia médica | |
| Compuestos relacionados | ||
| Alcanos | Butano, Pentano, Metilpropano | |
| Otros | Clorobutano | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
El propano ( de abreviación de propiónico mas el sufijo -ano) es un gas incoloro e inodoro. Pertenece a los hidrocarburos alifáticos (los alcanos). Su fórmula química C3H8:
Generales
Las mezclas de propano con el aire pueden ser explosivas con concentraciones del 1,7 - 9,3 % Vol de propano. La llama del propano al igual que la de los demás gases combustibles debe de ser completamente azul;cualquier parte amarillenta, anaranjada o rojiza de la misma denota una mala combustión. A temperatura ambiente es inerte frente a la mayor parte de los reactivos aunque reacciona por ejemplo con el bromo en presencia de luz. En elevadas concentraciones el propano tiene propiedades narcotizantes.
Tensión de vapor
Tensión de vapor del propano en función de la temperatura:
| Temperatura | Presión |
|---|---|
| 50 ºC | 18 kg/cm² |
| 40 ºC | 13,125 kg/cm2 |
| 30 ºC | 11,250 kg/cm2 |
| 15 ºC | 7,500 kg/cm2 |
| 0ºC | 5,000 kg/cm2 |
| -10 ºC | 3,800 kg/cm2 |
| -20 ºC | 2,750 kg/cm2 |
| -30 ºC | 1,880 kg/cm² |
| -40 ºC | 1,250 kg/cm2 |
Síntesis
El propano se suele obtener del gas natural o de los gases de los procesos de "cracking" producidos en las instalaciones petroquímicas.
Usos
El principal uso del propano es el aprovechamiento energético como combustible. Con base al punto de ebullición más bajo que el butano y el mayor valor energético por gramo, a veces se mezcla con éste o se utiliza propano en vez de butano. En la industria química es uno de los productos de partida en la síntesis del propeno. Además se utiliza como gas refrigerante (R290) o como gas propulsor en aerosoles.
Véase también
Enlaces externos
 Wikimedia Commons alberga una galería multimedia sobre Propano.
Wikimedia Commons alberga una galería multimedia sobre Propano.- Instituto nacional de Seguridad e Higiene en el Trabajo de España: Ficha internacional de seguridad química del propano.
