Hemoglobina glicada
La hemoglobina A glucada[1] (mal denominada también glucosilada) o HbA1 es una heteroproteína de la sangre que resulta de la unión de la hemoglobina (Hb) con glúcidos unidos a cadenas carbonadas con funciones ácidas en el carbono 3 y el 4.
Terminología[editar]
Se prefiere el término "hemoglobina glicada" en lugar de glucosilada para referirse al proceso correcto, que es no enzimático. Anteriormente, en la literatura se hacía referencia a la hemoglobina glucosilada de forma frecuente debido a que no estaba aún claro qué proceso era el involucrado hasta que se llevó a cabo mayor investigación. Los términos algunas veces se usan todavía indistintamente, pero el correcto es hemoglobina glicada.[2]
Es posible encontrar en la literatura, especialmente en otros idiomas, referencias a "HbA1c" que se derivan de la separación de la hemoglobina tipo A por Cromatografía de intercambio iónico. La primera fracción en separarse, probablemente considerada hemoglobina A pura, se designó HbA0, y las fracciones siguientes fueron HbA1a, HbA1b y HbA1c, en su orden de elución. Técnicas mejoradas de separación han llevado posteriormente al aislamiento de más subfracciones.[3]
Relación con la diabetes mellitus[editar]
La medición de la Hemoglobina (Hb) glicada es una prueba de laboratorio muy utilizada en la diabetes para saber si el control que realiza el paciente sobre la enfermedad ha sido buena durante los últimos tres o cuatro meses (aunque hay médicos que consideran sólo los dos últimos meses). De hecho, el 50 % del resultado depende sólo de entre las cuatro y seis últimas semanas.[4]
Se puede determinar dicho control gracias a que la glucosa forma una unión irreversible junto con la hemoglobina, presente en los glóbulos rojos de la sangre, que llegará a su fin a los 120 días de vida del glóbulo rojo. Lo mismo ocurre también en las personas sin diabetes. Por otra parte, el término "glucosilada" está mal empleado: sería más adecuado hablar de hemoglobina glicada, pues la glicosilación es un proceso altamente regulado, en tanto que la glicación es un proceso espontáneo y aleatorio.[5]
Mecanismos de daño[editar]
La hemoglobina glicada provoca un aumento de radicales libres altamente reactivos dentro de las células sanguíneas. Los radicales alteran las propiedades de la membrana de las células sanguíneas. Esto conduce a la agregación de células sanguíneas (eritrocitos) y al aumento de la viscosidad de la sangre, lo que da como resultado un flujo sanguíneo deteriorado.[6]
Otra forma en que la Hb glicada causa daño es a través de la inflamación, que da como resultado la formación de placa aterosclerótica (ateroma). La acumulación de radicales libres promueve la excitación de Fe2+-Hb a través de Fe3+-Hb en el Hb ferril anormal (Fe4+-Hb). Fe4+ es inestable y reacciona con aminoácidos específicos en la Hb para recuperar su estado de oxidación de Fe3+. Las moléculas de Hb se agrupan mediante reacciones de reticulación (también denominadas de trans-enlaces), y estos grupos de Hb (multímeros) promueven el daño celular y la liberación de Fe 4+-Hb en la matriz de capas más internas (subendotelio) de arterias y venas. Esto da como resultado una mayor permeabilidad de la superficie interior (endotelio) de los vasos sanguíneos y la producción de proteínas de adhesión de monocitos proinflamatorias, que promueven la acumulación de macrófagos en las superficies de los vasos sanguíneos, lo que finalmente conduce a placas dañinas en estos vasos.[6]
Las altamente glicosadas Hb-AGE atraviesan la capa de músculo liso vascular e inactivan la relajación dependiente del endotelio inducida por acetilcolina, posiblemente mediante la unión al óxido nítrico (NO), impidiendo su funcionamiento normal. El NO es un potente vasodilatador y también inhibe la formación de la forma oxidizada de LDL promotoras de placas (p.e, "colesterol malo").[6]
Esta degradación general de las células sanguíneas también libera hemo de ellas. El hemo suelto puede causar la oxidación de las proteínas endoteliales y LDL, lo que resulta en placas.[6]
El impacto de las proteínas glicosiladas ha sido estudiado como causa de enfermedades como la diabetes y neurodegenerativas.[7]También se ha encontrado que la presencia de proteínas incorrectamente plegadas (como aquellas afectadas por la glicación) afectan la composición y funcionalidad de las proteínas de largo plazo en el organismo [8][9][10]
Enfermedades como el Parkinson y el Alzheimer se han relacionado con el plegamiento erróneo de proteínas y los procesos de acumulación y deposición de fibrillas del tipo amiloide.[11][12][13]
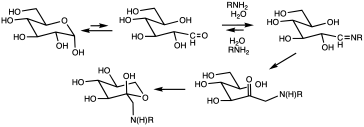
Tipos de hemoglobina glucosilada[editar]
Existen la hemoglobina glicosilada HbA1 y la HbA1c que es más estable, es decir, no influyen en esta los cambios bruscos en la glucemia. Sin embargo, alteraciones en la concentración de la hemoglobina total pueden variar el resultado[15] (hemoglobina alta, hemorragias agudas).
Hemoglobina glucosilada (HbA1c) y glucemia en sangre[editar]
Tabla para la hemoglobina HbA1c.[4]
Valores normales: 4,5-7 %. En individuos diabéticos puede alcanzar cifras de hasta el 20 %. Se consideran cifras de buena compensación las comprendidas entre 5 % y 8 %.| Media de glucemias (mg/dL) | Hemoglobina glucosilada (%) |
|---|---|
| 80-120 | 5-6 |
| 120-150 | 6-7 |
| 150-180 | 7-8 |
| 180-210 | 8-9 |
| 210-240 | 9-10 |
| 240-270 | 10-11 |
| 270-300 | 11-12 |
| 300-330 | 12-13 |
| etc. | etc. |
Hay estudios, como el DCCT Archivado el 18 de octubre de 2007 en Wayback Machine. y el UKPDS, que establecen que con una hemoglobina glicosilada menor del 7 %, se reduce considerablemente el riesgo de padecer enfermedades micro y macrovasculares.
Un estudio recientemente publicado en el New England Journal of Medicine denominado ACCORD demuestra que la disminución de la hemoglobina glucosilada mejora el pronóstico de las personas y disminuye el riesgo a sufrir enfermedades micro y macrovasculares con respecto al grupo de control. Buscar ACCORD en NEJM
Referencias[editar]
- ↑ OMS,OPS,BIREME (ed.). «Hemoglobina A Glucada». Descriptores en Ciencias de la Salud. Biblioteca Virtual en Salud.
- ↑ Oliwia Witczak, Trine B. Haugen (25 de noviembre de 2014). «Glycated or glycosylated?». Journal of the Norwegian Medical Association 134 (22): 2179. PMID 25423986. doi:10.4045/tidsskr.14.0172. Consultado el 5 de diciembre de 2018. «Hospitals should ensure that the correct term for HbA1c – glycated haemoglobin – is now to be found in laboratory manuals.»
- ↑ «What is hemoglobin A1c? An analysis of glycated hemoglobins by electrospray ionization mass spectrometry». Clinical Chemistry 44 (9): 1951-1958. 1998. PMID 9732983. doi:10.1093/clinchem/44.9.1951. Parámetro desconocido
|vauthors=ignorado (ayuda) - ↑ a b Antonio J. Arnal Meinhardt. Hemoglobina glicosilada (A1c), Control de Diabetes Revisado de TuDoctorOnline.blogspot.com
- ↑ Fourner, M; Bonté, F; Desmouliere, A (Oct 2018). «Glycation Damage: A Possible Hub for Major Pathophysiological Disorders and Aging». Aging and disease 9 (5): 880-900. PMC 6147582. PMID 30271665. doi:10.14336/AD.2017.1121.
- ↑ a b c d Saleh, Jumana (26 de agosto de 2015). «Glycated hemoglobin and its spinoffs: Cardiovascular disease markers or risk factors?». World Journal of Cardiology 7 (8): 449-53. ISSN 1949-8462. PMC 4549778. PMID 26322184. doi:10.4330/wjc.v7.i8.449.
- ↑ Thorpe SR, Baynes JW. (1996). «Role of the Maillard reaction in diabetes mellitus and diseases of aging.». Drugs Aging.
- ↑ Fan X, Zhang J, ThevesM, Strauch C, Nemet I, Liu S, Qian J, Giblin FJ, Monnier VM (2009). «Protein synthesis, post-translational modification, and degradation». J Biol Chem 284 ( 50): 34618- 34627.
- ↑ Maillard-Lefebvre H, Boulanger E, Daroux M, Gaxatte C, Hudson Bi, Lambert M. (2009). «Soluble receptor for advanced glycation end-products: a new biomarker in diagnosis and prognosis of chronic inflammatory disease». Rheumatology 48 ( 10): 1190-1196.
- ↑ Zhang Q, Monroe ME, Schepmoes AA, Clauss TRW, Gritsenko MA, Meng D, Petyuk VA, Smith RD, Metz TO. (2011). «Comprehensive identification of glycated peptides and their glycation motifs in plasma and erythrocytes of control diabetic subjects». J Proteome Res 10 ( 7): 3076-3088.
- ↑ Mimna R, Camus MS, Schmid A, Tuchscherer G, Lashuel Ha, Mutter M. (2007). «Disruption of amyloid-derived peptide assemblies through the controlled induction of a β-sheet to α-helix transformation: application of the switch concept». Angew Chem Int Ed 46 ( 15): 2681-2684.
- ↑ Xu Q, Park Y, Huang X, Hollenbeck A, Blair A, Schatzkin A, Chen H. (2011). «Diabetes and risk of Parkinson's disease. Diabetes Care 34 ( 4): 910- 915». Diabetes Care 34 ( 4): 910- 915.
- ↑ Caldés Melis C. (2012). «Formación de bases de Schiff de aminofosfolípidos con compuestos alicantes y efecto competitivo de Vitámeros B6». Disertación Grado Doctor en Ciencia y Tecnología Química - Palma de Mallorca: Universidad de las Islas Baleares, Programa de Doctorado de Ciencia y Tecnología Química, pp. 192.
- ↑ Yaylayan, Varoujan A.; Huyghues-Despointes, Alexis (1994). «Chemistry of Amadori Rearrangement Products: Analysis, Synthesis, Kinetics, Reactions, and Spectroscopic Properties». Critical Reviews in Food Science and Nutrition 34 (4): 321-69. PMID 7945894. doi:10.1080/10408399409527667.
- ↑ Antonio J. Arnal Meinhardt. ¿La Hemoglobina alta causa problemas? Archivado el 25 de abril de 2012 en Wayback Machine. Revisado en TuDoctorOnline.blogspot.com
