Tetrahidrometanopterina
| Tetrahidrometanopterina | ||
|---|---|---|
 | ||
| General | ||
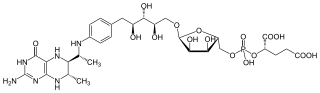
| Fórmula estructural |
| |
| Fórmula molecular |
C 30H 45N 6O 16P | |
| Identificadores | ||
| Número CAS | 92481-94-2[1] | |
| ChEBI | 17321 | |
| ChemSpider | 4573696 | |
| PubChem | 5462234 | |
| KEGG | C01217 | |
|
O=C2/N=C(/N)NC=1N[C@@H](C)C(NC=12)[C@H](Nc3ccc(cc3)C[C@H](O)[C@H](O)[C@H](O)CO[C@H]4O[C@@H]([C@@H](O)[C@H]4O)COP(=O)(O[C@H](C(=O)O)CCC(=O)O)O)C
| ||
|
InChI=1S/C30H45N6O16P/c1-12(21-13(2)33-26-22(34-21)27(44)36-30(31)35-26)32-15-5-3-14(4-6-15)9-16(37)23(41)17(38)10-49-29-25(43)24(42)19(51-29)11-50-53(47,48)52-18(28(45)46)7-8-20(39)40/h3-6,12-13,16-19,21,23-25,29,32,34,37-38,41-43H,7-11H2,1-2H3,(H,39,40)(H,45,46)(H,47,48)(H4,31,33,35,36,44)/t12-,13+,16+,17-,18+,19-,21?,23+,24-,25-,29+/m1/s1
Key: SCBIBGUJSMHIAI-FDLOOEGASA-N | ||
| Propiedades físicas | ||
| Masa molar | 776 682 661 g/mol | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
La tetrahidrometanopterina (THMPT, H
4MPT) es una coenzima en el proceso de metanogénesis. Funciona como transportador del grupo C1 mientras se reduce a nivel de metilo, antes de ser transferido a la coenzima M.[2]
La tetrahidrosarcinapterina (THSPT, H
4SPT) es una forma modificada de THMPT, en la cual hay un grupo glutamil enlazado al extremo 2-hidroxiglutárico.
THMPT es la principal plataforma para transformaciones C1
[editar]El N-formilmetanofurano dona su grupo C1 al sitio N5 de la pterina para producir el formil-THMPT.[3] El grupo formilo subsecuentemente se condensa intramolecularmente para producir metenil-THMPT+
, el cual luego es reducido a metileno-THMPT.[4] El metileno-MPT subsecuentemente se convierte (utilizando coenzima F420 como fuente de electrones), a metil-THMPT, reacción catalizada por la metileno-THMPT reductasa dependiente de F420. El metil-THMPT funciona como donante de metilo a la coenzima M, una conversión mediada por la metil-THMPT:coenzima M metil-transferasa.[2]
Comparación con el ácido tetrahidrofólico
[editar]El THMP se encuentra relacionado con el mejor conocido ácido tetrahidrofólico (THFA, H
4FA). La diferencia más importante entre THMPT y THFA es que THFA posee un grupo aceptor de electrones en el anillo fenilo. Como resultado, el metenil-THMPT es más difícil de reducir que el metenil-THFA. La reducción la efectúa una hidrogenasa llamada "libre de grupos hierro azufre".[4] Este abstruso nombre distingue entre esta hidrogenasa, aquella llamada hidrogenasa solo hierro, y de las hidrogenasas que contienen grupos Fe-S.
Referencias
[editar]- ↑ Número CAS
- ↑ a b Thauer RK (septiembre de 1998). «Biochemistry of methanogenesis: a tribute to Marjory Stephenson. 1998 Marjory Stephenson Prize Lecture». Microbiology 144 (Pt 9): 2377-406. PMID 9782487. doi:10.1099/00221287-144-9-2377. Archivado desde el original el 17 de mayo de 2020. Consultado el 22 de marzo de 2015.
- ↑ Acharya P, Warkentin E, Ermler U, Thauer RK, Shima S (marzo de 2006). «The structure of formylmethanofuran: tetrahydromethanopterin formyltransferase in complex with its coenzymes». J. Mol. Biol. 357 (3): 870-9. PMID 16466742. doi:10.1016/j.jmb.2006.01.015.
- ↑ a b Korbas M, Vogt S, Meyer-Klaucke W, et al. (octubre de 2006). «The iron-sulfur cluster-free hydrogenase (Hmd) is a metalloenzyme with a novel iron binding motif». J. Biol. Chem. 281 (41): 30804-13. PMID 16887798. doi:10.1074/jbc.M605306200.
