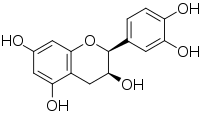
Catequina
| Catequina | ||
|---|---|---|
 | ||
 | ||
| Nombre IUPAC | ||
| (2R,3S)-2-(3,4-dihydroxifenil)-3,4-dihidro-2H-chromene-3,5,7-triol | ||
| General | ||
| Otros nombres |
Catecol Cianidanol Cyanidanol (+)-catequin D-Catequina Ácido catequínico Catechuic acid Cianidol Dexcianidanol (2R,3S)-Catequina 2,3-trans-catequina 3,3',4',5,7–flavanpentol | |
| Fórmula semidesarrollada | C15H14O6 | |
| Fórmula molecular | ? | |
| Identificadores | ||
| Número CAS | 7295-85-4[1] | |
| ChEBI | 15600 | |
| ChEMBL | CHEMBL311498 | |
| ChemSpider | 8711 | |
| DrugBank | 14086 | |
| PubChem | 9064 | |
| UNII | 8R1V1STN48 | |
| KEGG | C06562 | |
| Propiedades físicas | ||
| Apariencia | sólido incoloro | |
| Masa molar | 290,26 g/mol | |
| Punto de fusión | 448 K (175 °C) | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
La catequina es un antioxidante polifenólico que procede de las plantas en las cuales aparece como un metabolito secundario. El término catequina se emplea comúnmente para referirse a la familia de los flavonoides y al subgrupo de los flavan-3-oles (o simplemente flavanoles). El nombre de catequina proviene de la familia de plantas denominada catechu (Terra Japonica) y concretamente del jugo extraído de la Mimosa catechu (Acacia catechu L.f)[2]
Propiedades químicas[editar]
Descripción molecular[editar]

La molécula de catequina (en inglés "catechin") posee dos anillos bencénicos (denominados los anillos A- y B- ) y un heterociclo dihidropirano (el anillo C) con un grupo hidroxilo sobre el carbono 3. El anillo A es similar al grupo funcional del resorcinol mientras que el anillo B es similar al grupo funcional del catecol. Existen en la molécula dos centros de quiralidad, uno se encuentra en el carbono 2 y el otro sobre el 3. Por lo tanto la catechina posee cuatro diastereoisémeros. Dos son isómeros de configuración trans y se denominan catequina y los otros dos son de configuración cis y se denominan epiccatequina.
El isómero más común de la catequina es la (+)-catequina. Su otro estereoisómero es la (-)-catequina o ent-catequina. El isómero más común de la epicatequina es la (-)-epicatequina (conocido también con otras denominaciones como la L-epicatequina, epicatecol, (-)-epicatecol, l-acacatequina, l-epicatecol, epi-catequina, 2,3-cis-epicatequina o (2R,3R)-(-)-epicatequina). La diferencia entre los epímeros puede apreciarse mediante el empleo de cromatografía de columnas quirales.[3] Haciendo ninguna referencia a un isómero en particular, la molécula puede denominarse simplemente catequina. Las mezclas de diferentes enantiómeros puede ser denominado (+/-)-catequina o DL-catequina e incluso (+/-)-epicatequina o DL-epicatequina.
- Diastereoisomers gallery
-
(+)-catechin (2R-3S)
-
(-)-catechin (2S-3R)
-
(-)-Epicatechin (2R-3R)
-
(+)-epicatechin (2S-3S)

Además, la flexibilidad del anillo C permite dos isómeros conformacionales, ubicando el anillo B en una posición pseudoecuatorial (E conformer) o en una posición pseudoaxial (A conformer). algunos estudios han confirmado que la (+)-catechina adopta una mezcla de A- y E- conformers en soluciones acuosas y que su equilibrio conformacional se evalúa en la proporción 33:67.[4]
En relación con su actividad antioxidante, el (+)-catequina se ha podido encontrar en la mayoría de los más potentes 'eliminadores' ("scavengers") entre diferentes miembros de las clases de flavonoides. La habilidad para eliminar moléculas de oxígeno parece estar relacionada con la estructura química de la molécula de la catequina, que en presencia del grupo funcional del catecol en el anillo B y con la presencia del grupo hidroxilo activando el doble enlace del anillo C.[5]
Oxidación[editar]
Los experimentos electroquímicos muestran que los mecanismos de la oxidación de la (+)-catequina se producen en una secuencia de pasos bien definidos, todos ellos relacionados con la presencia de los grupos catecol y resorcinol siendo además la oxidación dependiente del pH. La oxidación que primero ocurre es la donación de electrones de la catecol 3′,4′-dihydroxilo, todo ello en una existencia de muy bajos potenciales positivos, siendo además una reacción reversible. El grupo hidroxilo del grupo funcional del resorcinol oxidado, tras este primer paso, deviene en una reacción irreversible de oxidación.[6]
Datos espectrales[editar]
| UV-Vis | |
|---|---|
| Retention time | 4.473 min (C18 RP, Acetonitrilo 80%)[7] |
| Lambda-max: | 276 nm |
| Extinction coefficient (log ε) | 4.01 |
| IR | |
| Bandas de absorción | 1600 cm−1(anillos de benceno) |
| NMR | |
| Proton NMR
|
δ : 2.49 (1H, dd, J = 16.0, 8.6 Hz, H-4a), |
| Carbon-13 NMR | |
| Other NMR data | |
| MS | |
| Masses of main fragments |
ESI-MS [M+H]+ m/z : 291.0
|
Fuentes[editar]
Tanto la (+)-catequina como la (-)-epicatequina se encuentran en las plantas de la medicina tradicional china como puede ser la Uncaria rhynchophylla,[9] en la Potentilla fragarioides ambas conocidas en la terapia china y que contienen D-catequina.[10] Una mezcla racémica de (+)-catequina y (-)-catequina se extrae de las raíces de malas hierbas de la variedad: Centaurea maculosa. En algunos casos actúa como herbicida e inhibe la competición existente entre las plantas de otras especies.La (-)-catechina actúa como fitotoxico inhibiendo la germinación de semillas y su crecimiento y la (-)-catechina actúa como antimicrobiano de los patógenos de la raíz.[11]
La l-Epicatequina se encuentra en las granas del cacao lo que vino a denominarse como kakaool.[12] Los diferentes enantiómeros se pueden encontrar igualmente en el chocolate a lo largo de sus procesos de elaboración que puede devenir en una epimerización por calentamiento. La nuez cola (Cola acuminata), una especie relacionada, contiene epicatequina y D-catequina. El vino también contiene cantidades considerables de catequina y epicatequina.[13] El sabor asociado a la (+)-catequina o (-)-catequina es descrita aproximadamente como una mezcla de astringente y algo amarga.[14] Se ha comprobado que encapsulando la catequinas en ciclodextrinas se enmascara el sabor, siendo empleado como aditivo.[4]
Referencias[editar]
- ↑ Número CAS
- ↑ Zheng LT, Ryu GM, Kwon BM, Lee WH, Suk K (junio de 2008). «Anti-inflammatory effects of catechols in lipopolysaccharide-stimulated microglia cells: inhibition of microglial neurotoxicity». Eur. J. Pharmacol. 588 (1): 106-13. PMID 18499097. doi:10.1016/j.ejphar.2008.04.035.
- ↑ Determination of catechin diastereomers from the leaves of Byrsonima species using chiral HPLC-PAD-CD. Rinaldo D, Batista JM Jr, Rodrigues J, Benfatti AC, Rodrigues CM, Dos Santos LC, Furlan M, Vilegas W, Chirality. 2010 Feb 8.
- ↑ a b Auzély-Velty, Rachel; Charlot, Aurélia; Imberty, Anne; Koča, Jaroslav; Kríž, Zdeňek (9 de julio de 2003). «Investigation of the complexation of (+)-catechin by β-cyclodextrin by a combination of NMR, microcalorimetry and molecular modeling techniques». Organic & Biomolecular Chemistry (en inglés) 1 (14): 2590-2595. ISSN 1477-0539. doi:10.1039/B302935M. Consultado el 18 de junio de 2019.
- ↑ Antioxidant activity of flavonoids: Efficiency of singlet oxygen (1Δg) quenching. Cécile Tournaire, Sylvie Croux, Marie-Thérèse Maurette, Irena Beck, Michel Hocquaux, André M. Braun and Esther Oliveros, Journal of Photochemistry and Photobiology B: Biology, Volume 19, Issue 3, August 1993, Pages 205-215, doi:10.1016/1011-1344(93)87086-3
- ↑ Catechin electrochemical oxidation mechanisms. Patricia Janeiro and Ana Maria Oliveira Brett, Analytica Chimica Acta, Volume 518, Issues 1-2, 2 August 2004, Pages 109-115, doi:10.1016/j.aca.2004.05.038
- ↑ Development and validation of a LC-method for determination of catechin and epicatechin in aqueous extractives from leaves of Maytenus ilicifolia. L.A.L. Soares, A.L. Oliveira, G.González Ortega and P.R. Petrovick, Journal of Pharmaceutical and Biomedical Analysis, Volume 36, Issue 4, 19 November 2004, Pages 787-790
- ↑ Neural cell protective compounds isolated from Phoenix hanceana var. formosana. Yi-Pei Lin, Tai-Yuan Chen, Hsiang-Wen Tseng, Mei-Hsien Lee and Shui-Tein Chen, Phytochemistry, Volume 70, Issue 9, June 2009, Pages 1173-1181
- ↑ Hou WC, Lin RD, Chen CT, Lee MH (agosto de 2005). «Monoamine oxidase B (MAO-B) inhibition by active principles from Uncaria rhynchophylla». J Ethnopharmacol 100 (1-2): 216-20. PMID 15890481. doi:10.1016/j.jep.2005.03.017.
- ↑ «Potentilla fragarioides PFAF Plant Database». pfaf.org. Consultado el 18 de junio de 2019.
- ↑ Bais HP, Walker TS, Stermitz FR, Hufbauer RA, Vivanco JM (abril de 2002). «Enantiomeric-dependent phytotoxic and antimicrobial activity of (±)-catechin. A rhizosecreted racemic mixture from spotted knapweed». Plant Physiol. 128 (4): 1173-9. PMID 11950966. doi:10.1104/pp.011019.
- ↑ Freudenberg, Karl; Cox, Richard F. B.; Braun, Emil (1 de mayo de 1932). «THE CATECHIN OF THE CACAO BEAN1». Journal of the American Chemical Society 54 (5): 1913-1917. ISSN 0002-7863. doi:10.1021/ja01344a026. Consultado el 18 de junio de 2019.
- ↑ Aizpurua-Olaizola, Oier; Ormazabal, Markel; Vallejo, Asier; Olivares, Maitane; Navarro, Patricia; Etxebarria, Nestor; Usobiaga, Aresatz (1 de enero de 2015). «Optimization of Supercritical Fluid Consecutive Extractions of Fatty Acids and Polyphenols from Vitis Vinifera Grape Wastes». Journal of Food Science (en inglés) 80 (1): E101-E107. ISSN 1750-3841. doi:10.1111/1750-3841.12715. Consultado el 18 de febrero de 2016.
- ↑ Oral sensations associated with the flavan-3-ols (+)-catechin and (−)-epicatechin. S. Kielhorn and J. H. Thorngate III, Food Quality and Preference, Volume 10, Issue 2, March 1999, Pages 109-116, doi:10.1016/S0950-3293(98)00049-4