Mecanismo de Grotthuss
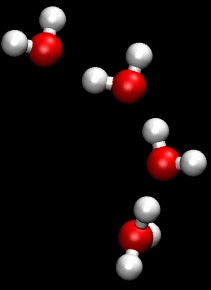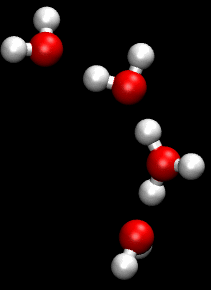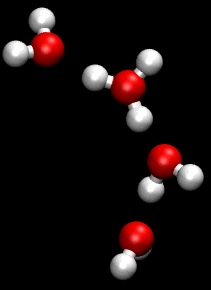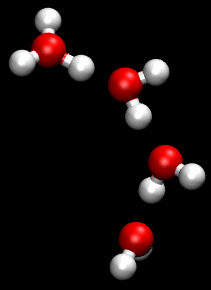
El mecanismo Grotthuss consiste en una sucesión de "saltos" de protones (H+) a través de una red de puentes de hidrógeno, de molécula a molécula.
Cuando el proceso ocurre en agua líquida, un protón es liberado por un ion hidronio inicial, e hidratado inmediatamente por una molécula de agua asociada a dicho ion hidronio mediante un puente de hidrógeno. En esto consiste el llamado salto de un protón.
El salto de un protón causa que la molécula de agua aceptora del protón se transforme en un segundo ion hidronio. Ahora, si este segundo ion hidronio se encuentra asociado mediante un puente de hidrógeno a una tercera molécula de agua, entonces el fenómeno se repite: ocurre un segundo salto de protón.
Una sucesión de saltos de protones (en inglés, proton hopping), es decir, de liberaciones e hidrataciones de cationes hidrógeno, conforma aquello que se denomina el mecanismo Grotthuss.
En su publicación de 1806, "Theory of decomposition of liquids by electrical currents", Theodor Grotthuss propuso una teoría que explicara la conductividad del agua:[1] concibió la reacción de ionización del agua como una especie de 'mecanismo cangilón' en el que cada átomo de oxígeno pasaba y, simultáneamente, recibía un átomo de hidrógeno. En su 200.º aniversario, su artículo fue revisado por Cukierman.[2]
El 'mecanismo Grotthuss' se conoce hace 200 años y es un equivalente de la expresión salto de protones o conducción de protones.
Explicación simplificada
[editar]Las moléculas de agua tienen una ligera tendencia a ionizarse reversiblemente para proporcionar un ion hidrógeno (protón) y un ion hidroxilo, dando el equilibrio
- H2O
 H+ + OH−
H+ + OH−
Aunque normalmente se muestra el producto de disociación del agua como H+, los protones libres no existen en disolución. Los iones hidrógeno formados en el agua son inmediatamente hidratados a iones hidronio (H3O+). La hidratación de los protones disociados es virtualmente instantánea gracias a los puentes de hidrógeno entre las moléculas de agua.
Ningún protón individual se mueve muy lejos a través del volumen de la disolución, pero una serie de saltos de protones entre moléculas de agua unidas por puentes de hidrógeno produce el movimiento neto de un protón a una gran distancia en un tiempo notablemente corto.
Como resultado de la elevada movilidad neta del H+, las reacciones ácido-base en disolución acuosa son, en general, excepcionalmente rápidas. El resultado del salto de protones: un protón posee un movimiento neto a gran velocidad y a una gran distancia. El salto de protones explica la elevada movilidad iónica de los iones H+ comparada con otros cationes monovalentes como el Na+ o el K+.
Está basado en la asunción de que no es un solo protón específico moviéndose de una molécula a otra, sino que el salto de un protón en la ruta de puentes de hidrógeno provoca el salto del siguiente protón de la ruta y, por ende, la escisión de un enlace covalente O-H por cada salto.
El salto de protones también desempeña un papel en las reacciones biológicas de transferencia de electrones.
Papel del salto de protones en las reacciones biológicas
[editar]Al determinar la estructura de una proteína tal como la hemoglobina por cristalografía de rayos X, es frecuente encontrar moléculas de agua unidas tan fuertemente que forman parte de la estructura cristalina. Lo mismo ocurre en cristales de RNA y DNA. Estas moléculas de agua, detectables también en disolución mediante resonancia magnética nuclear, poseen propiedades que las distinguen del resto de agua del disolvente. Son, por ejemplo, osmóticamente inactivas.
El agua fuertemente unida es esencial para la función de muchas proteínas. Por ejemplo, en una de las reacciones clave del proceso de la fotosíntesis, la energía de la luz se usa para bombear protones a través de una membrana biológica al tiempo que se produce un flujo de electrones a través de una serie de proteínas transportadoras. Una de estas proteínas, el citocromo f, tiene unida una cadena de cinco moléculas de agua que puede proporcionar una vía para el movimiento de protones a través de la membrana, es decir, mediante el salto de protones.
Casi con toda seguridad, otra bomba de protones que utiliza la energía de la luz, la bacteriorrodopsina, usa una cadena de moléculas de agua unidas y orientadas de una forma precisa para el movimiento transmembrana de los protones.
Difusión anómala de protones
[editar]El mecanismo Grotthuss, junto con la relativa ligereza y pequeño tamaño del protón, explica la inusualmente alta tasa de difusión del protón respecto a la de otros cationes comunes (Tabla 1), que se debe simplemente al movimiento térmico aleatorio, es decir, el movimiento browniano. Un túnel cuántico se vuelve más probable cuanto menor es la masa del catión, y el protón es el catión más ligero y estable posible. Por lo tanto, también hay un efecto menor de túnel cuántico, a pesar de que domina solo a bajas temperaturas.
| Catión | Movilidad / cm2 V-1 s-1 |
| NH4+ | 0,763×10-3 |
| Na+ | 0,519×10-3 |
| K+ | 0,762×10-3 |
| H+ | 3,62×10-3 |
Referencias
[editar]- ↑ de Grotthuss, C.J.T. (1806). «Sur la décomposition de l'eau et des corps qu'elle tient en dissolution à l'aide de l'électricité galvanique». Ann. Chim. 58: 54-73.
- ↑ Cukierman, Samuel (2006). «Et tu Grotthuss!». Biochimica et Biophysica Acta 1757 (8): 876-8. PMID 16414007. doi:10.1016/j.bbabio.2005.12.001.
Literatura
[editar]- Peter W. Atkins. 2001. Kurzlehrbuch Physikalische Chemie. Wiley-VCH, Weinheim, ISBN 3-527-30433-9 Linktexto = Eingeschränkte Vorschau, p. 382.
Enlaces externos
[editar]- Esta obra contiene una traducción derivada de «Grotthuss mechanism» de Wikipedia en inglés, concretamente de esta versión, publicada por sus editores bajo la Licencia de documentación libre de GNU y la Licencia Creative Commons Atribución-CompartirIgual 4.0 Internacional.
