Nanodiamantes mediante detonación
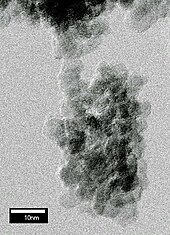
Mediante detonación se pueden formar nanocristales de diamante, a menudo también conocidos como (UDD) del inglés ultradispersed diamond. Se trata de diamantes que se originan a partir de una detonación. Cuando una mezcla de explosivos de TNT/RDX con deficiencia de oxígeno es detonada en una cámara cerrada, se forman partículas de diamante con un diámetro de aprox. 5 nm en la parte delantera de la onda de detonación al cabo de varios microsegundos.
-
estructura del trinitrotolueno (TNT)
-
estructura del hexógeno (RDX)
Historia
En 1962 un grupo de científicos soviéticos del VNIITF dirigidos por Yevgeni Zababakhin, incluyendo K.V. Volkov, Danilenko Vyacheslav, y V.I. Elina sintetizaron diamantes por la compresión mediante ondas de choque de grafito y hollín contenido en cápsulas esféricas y cilíndricas. En 1963 para aumentar el rendimiento en diamante se usaba una mezcla de grafito comprimido con metal líquido de refrigerante. En 1962, Danilenko propuso un cambio en la síntesis. En este caso, el grafito se coloca directamente en una carga cilíndrica de una mezcla de TNT/RDX, y para suprimir la grafitización y reducir la velocidad de degradación diamante, la carga está rodeada por una membrana de agua. Esto proporcionó un fuerte incremento en el rendimiento en diamantes. En julio de 1963, se realizó un experimento de control de carga sin grafito, que confirmó la suposición de la síntesis de diamante en los productos de detonación. Basándose en el diagrama de fases del carbono y los valores de P, T punto de Jouguet para la expansión de la detonación de los explosivos, se demostró que el carbono libre se debía condensar en forma de diamante. El explosivo debe tener un balance de oxígeno negativo. La principal ventaja de los productos de condensación de detonación de carbono atómico en comparación con la síntesis de grafito es que este proceso no se necesita gastar tiempo ni energía en la destrucción o conversión de la red cristalina original de grafito. El problema en este caso es preservar el diamante ultrafino (UFD) de la oxidación y la grafitización. Entre 1963 y 1965, se muestra crítico la refrigeración de los productos de detonación mediante la conversión de energía potencial en energía cinética de la membrana que rodea a la carga. La carga moldeada en forma de un cilindro alargado, dando a la salida UFD 8-12% en peso de la carga por el contenido de UFD en la carga de hasta 75% (véase balance oxígeno del TNT). En los EE.UU. la primera mención de este método no aparece hasta 1988.
Mecamismo físico
Los microcristales de diamante se generan por las reacciones químicas en la parte delantera de la onda de detonación en la explosión de altos explosivos (una mezcla de TNT y RDX). En los gases formados durante la detonación de ciertos explosivos contienen una cantidad significativa de carbono libre. Debido a las altas temperaturas y presiones alcanzadas durante la explosión, este carbono adopta la fase de diamante. La forma de nanodiamantes es termodinámicamente más estable. Hasta la fecha, no hay ninguna teoría confirmada sobre la formación de los microdiamentes. De acuerdo con la termodinámica de formación, un aspecto básico es garantizar la posibilidad de un diamante en el colapso adiabático de carbono explosivo con balance de oxígeno negativo, es el hecho de que la condensación de carbono libre en el diamante o la fase líquida. La expansión adiabática de los productos de detonación sigue la detonación. Las condiciones para la estabilidad del diamante persiste un tiempo. Si la densidad de los productos de detonación está cerca de la densidad inicial del explosivo, las condiciones de estabilidad del diamante cambian a las necesarias para la estabilidad de grafito. En una expansión adiabática la presión de detonación y temperatura productos cae más rápido, por lo que el estado termodinámico del componente de carbono se encuentra en la región de estabilidad de grafito a alta temperatura, lo que contribuye a la transición de fase de diamante a grafito. Pero a una cierta temperatura, la tasa de grafitización disminuye, y por lo tanto estas etapas de la expansión de los productos de detonación el carbono que pasa de la fase de diamante a grafito, es insignificante - la grafitización se "congela" y se mantiene en la fase de diamante. Así, la transición de grafito a diamante se produce cuando la temperatura excede grafitización congelación. Si T >> Tgraf, durante todo el tiempo los diamante se convierten en grafito, y len os productos de detonación enfriados no detectan UDD. Así, la temperatura es crucial en este proceso y esta en gran medida determinada por la configuración de la carga (la conductividad térmica del medio). Las condiciones óptimas de formación de la UDD en la onda de detonación y su conservación es una presión alta y una temperatura relativamente baja de los productos de detonación, que corresponden las condiciones de Chapman-Jouguet. Por lo tanto, los nano-diamantes de síntesis de detonación pasan 3 etapas:
- Formación de carbono libre como resultado de la detonación.
- Una rápida expansión del productos de detonación, partículas de diamante, y el enfriamiento por debajo de la temperatura de grafitización.
- Rápida transferencia del calor y masa entre los productos de detonación y el medio que rodea a la carga.
Propiedades
El rendimiento de diamante después de la detonación depende fundamentalmente de la condición de síntesis y especialmente en la capacidad de calor del medio refrigerante en la cámara de detonación (agua, aire, CO2, etc.) Cuanto mayor sea la capacidad de refrigeración, mayor será el rendimiento en diamantes, que puede alcanzar 90%. Después de la síntesis, el diamante se extrae del hollín usando alta temperatura y alta presión (autoclave) ebullición en ácido durante un largo período (ca. 1-2 días). La ebullición elimina la mayor parte de la contaminación por metales, procedentes de los materiales de cámara, y el carbono no-diamante.
Diversas mediciones, incluyendo difracción de rayos X[1] y microscopía electrónica de transmisión de alta resolución[2] reveló que el tamaño de los granos de diamante en el hollín se distribuye alrededor de los 5 nm. Los granos son inestables con respecto a la agregación y la forma espontánea de tamaño micrómetro-grupos (ver figura anterior). La adhesión es fuerte y los contactos entre unos pocos nano-granos puede contener un grupo de tamaño micras unido a un sustrato.[2]
Nanométricas de diamantes tiene un área de relativa superficie muy grande. Como resultado, su superficie espontáneamente une las moléculas de agua e hidrocarburos de la atmósfera ambiente.[3] Sin embargo, limpia la superficie nanodiamantes se puede obtener con un manejo adecuado.[2]
Los granos de detonación nanodiamantes tienen en su mayoría de diamante cúbico red y son estructuralmente imperfecto. Los principales defectos son los maclas, como lo sugiere la microscopía de transmisión de electrones de alta resolución.[2] A pesar de la fuente de carbono para la síntesis de diamante - mezcla explosiva de TNT / RDX - que es rico en nitrógeno, la concentración de nitrógeno paramagnética en el interior granos de diamante es inferior a 1 parte por millón (ppm).[1] de nitrógeno Paramagnética (átomos neutros de nitrógeno de carbono en la sustitución de la estructura del diamante) es la principal forma de nitrógeno en el diamante, y por lo tanto el contenido de nitrógeno en la NOM es probablemente muy bajo.
Síntesis alternativas
También se puede sintetizar nanocristales de diamante a partir de una suspensión de grafito en un líquido orgánico a presión atmosférica y temperatura ambiente utilizando cavitación ultrasónica. El rendimiento es de aproximadamente 10%. El costo de nanodiamantes producidos por este método se estima que sea competitivo con el proceso HPHT.[4][5]
Una técnica alternativa es la síntesis mediante irradiación de grafito con pulsos de láser de alta energía. La estructura y el tamaño de partícula del diamante obtenido es bastante similar a la obtenida en explosión. En particular, muchas partículas exhiben hermanamiento múltiple.[6]
Aplicaciones industriales
Los productos comerciales basados en nano-diamantes se encuentran disponibles para las siguientes aplicaciones:
- Lapeado y pulido (por ejemplo Sufipol);
- Aditivos para aceites de motor (por ejemplo, Addo);
- Lubricantes secos para la industria metalúrgica (Dibujo de W, Mo, V, RH-hilos);
- Refuerzo de los rellenos para plásticos y cauchos;
- Suplementos para la galvanoplastia electrolitos (por ejemplo, DiamoSilb, DiamoChrom).[7]
Véase también
Referencias
- ↑ a b "Structure and defects of detonation synthesis nanodiamond" Diamond and Related Materials 9 (2000) 861
- ↑ a b c d "High-resolution electron microscopy of detonation nanodiamond" Nanotechnology 19 (2008) 155705
- ↑ "FTIR study of the adsorption of water on ultradispersed diamond powder surface" Appl. Surf. Sci 133 (1998) 231
- ↑ "Experimental Corroboration of the Synthesis of Diamond in the Cavitation Process" Doklady Physics 49(2004) 150
- ↑ "Graphite-to-diamond transformation induced by ultrasonic cavitation" Diamond and Related Materials 17 (2008) 931
- ↑ "The formation of multiply twinning structure and photoluminescence of well-dispersed nanodiamonds produced by pulsed-laser irradiation" Diamond and Related Materials 17 (2008) 142
- ↑ "Additives to metal plating" Manufacturer's source
Enlaces externos
- http://pubs.acs.org/cgi-bin/sample.cgi/jpcbfk/asap/pdf/jp066387v.pdf
- https://web.archive.org/web/20080625214911/http://www.udayton.edu/News/Article/?contentId=2234
- http://research.ncl.ac.uk/nanoscale/research/nanodiamond.html Nanodiamond research at Newcastle University
- http://www.ioffe.rssi.ru/nanodiamond/ Ioffe Physico-Technical Institute of the Russian Academy
- http://www.cnn.com/2007/TECH/science/10/19/nanodiamonds.drugs/index.html
- http://www.plasmachem.de/overview-powders.html#diamond


