Reacción de Barton-Kellogg
La Reacción de Barton-Kellogg o Síntesis de olefinas Barton-Kellogg es un método de síntesis que efectúa un acoplamiento (o condensación) entre un diazocompuesto (Preparado a partir de una cetona) y una tiocetona con la formación de un alqueno como producto deseado.[1][2][3]

Esta reacción fue descrita por Hermann Staudinger[4] y por lo tanto la reacción también se conoce con el nombre de acoplamiento diazo-tiocetona tipo Staudinger.
Mecanismos de reacción[editar]
El método consiste en dos reacciones:
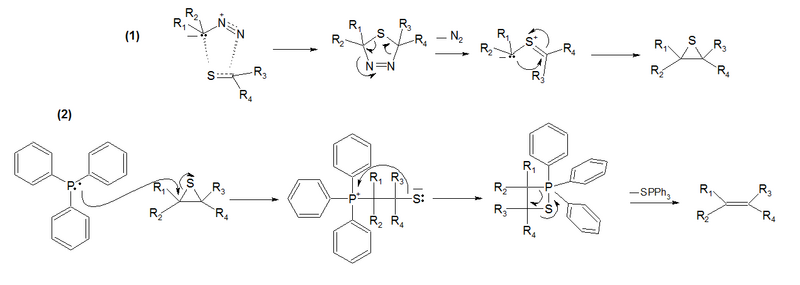
- (1) La cicloadición entre el diazocompuesto A y la tiocetona B para dar una tiadiazolina C, en donde se extruye el nitrógeno para dar un episulfuro D.
- (2) La eliminación del átomo de azufre del episulfuro con el uso de trifenilfosfina para dar el alqueno.
En el mecanismo de la reacción (1), el compuesto diazo se comporta como un dipolo 1,3 que reacciona con la tiocetona en una cicloadición dipolar-1,3 para dar la tiadiazolina. Este intermediario es inestable y por la extrusión de nitrógeno gaseoso se forma un iluro tiocarbonílico como intermediario para obtenerse un episulfuro estable.
En el mecanismo de la reacción (2), la trifenilfosfina abre el ciclo de tres miembros y luego forma un sulfafosfatano de una manera similar a la reacción de Wittig. En el paso final, el sulfuro de trifenilfosfina es expulsado para liberar el alqueno.
Aplicaciones[editar]
El diazocompuesto se puede obtener a partir de una cetona por reacción con hidracina para obtener la hidrazona, seguido de una oxidación. Existen muchos reactivos para esta conversión, por ejemplo plata (I) y óxido de bis(trifluoroacetoxi)yodobenceno [5]. La tiocetona necesaria para esta reacción se puede obtener de una cetona y pentasulfuro de fósforo. La desulfuración del episulfuro se puede lograr con fosfinas y también con polvo de cobre.

La principal ventaja de esta reacción sobre la reacción de McMurry es que la reacción se puede llevar a cabo con dos cetonas diferentes.
Referencias[editar]
- ↑ D. H. R. Barton and B. J.Willis, J. Chem. Soc. D 1970, 1225.
- ↑ Kellogg, R. M.; Wassenaar, S. Tetrahedron Lett. 1970, 11, 1987.
- ↑ R. M. Kellogg, Tetrahedron 1976, 32, 2165.
- ↑ H. Staudinger and J. Siegwart, Helv. Chim. Acta 1920, 3, 833.
